- •Часть 1. Цитология
- •Введение
- •Лабораторная работа № 1. Способы приготовления препаратов и методы их исследования Цель занятия
- •План изучения темы
- •Теоретическая часть занятия
- •1. Микроскопия
- •1.1. Световая микроскопия
- •1.1.1. Устройство микроскопа
- •1.1.2. Приготовление гистологического препарата
- •1.1.2.1. Взятие и фиксация материала
- •1.1.2.2. Обезвоживание и уплотнение материала
- •1.1.2.3. Приготовление срезов
- •1.1.2.4.1. Типы красителей
- •1.2. Электронная микроскопия
- •Вопросы для контроля
- •Практическая часть занятия
- •Лабораторная работа № 2 Общая морфология клетки и клеточных структур Цель занятия
- •План изучения темы
- •Теоретическая часть занятия
- •1. Единство и многообразие клеток
- •1.1. Клеточная теория
- •1.2. Основные положения теории
- •2. Форма клеток и их ядер под микроскопом
- •3. Клеточные мембраны и структуры клеточной поверхности
- •3.1. Клеточные мембраны
- •3.1.1. Принцип организации мембран
- •3.1.2. Особенности плазмолеммы
- •3.1.3. Функции плазмолеммы
- •3.2. Способы трансмембранного переноса
- •3.2.1. Перенос низкомолекулярных веществ через плазмолемму
- •3.2.2. Перенос в клетку крупных соединений и частиц (эндоцитоз)
- •3.2.3. Перенос из клетки крупных соединений и частиц (экзоцитоз)
- •3.3. Компоненты мембранной системы клетки
- •Вопросы для контроля
- •Практическая часть занятия
- •Самостоятельная работа
- •Теоретическая часть занятия
- •Вакуолярная система цитоплазмы
- •1.1. Эндоплазматическая сеть (эпс)
- •1.3.1. Функция лизосом
- •1.3.2. Виды лизосом
- •1.5. Глиоксисомы
- •1.6. Секреторные, транспортные везикулы
- •Вопросы для контроля
- •Практическая часть занятия
- •План изучения темы
- •Теоретическая часть занятия
- •1.1. Строение
- •1.2. Автономность метаболизма
- •1.3. Функции
- •2. Пластиды
- •2.1. Типы пластид
- •2.1.1. Хлоропласты
- •2.1.2. Лейкопласты
- •Вопросы для контроля
- •Практическая часть занятия
- •Самостоятельная работа
- •1. Рибосомы
- •1.1. Виды и структура рибосом
- •2. Цитоскелет и его производные
- •2.1.2. Микроворсинки
- •2.3. Микротрубочки и их производные
- •2.3.1. Микротрубочки
- •2.3.2. Центриоли
- •2.3.3. Реснички и жгутики
- •Вопросы для контроля
- •Практическая часть занятия
- •Самостоятельная работа
- •Демонстрационные препараты
- •Теоретическая часть занятия
- •1. Клеточное ядро
- •1.1.3. Структура ядра
- •2. Хроматин
- •II. Состояние хроматина в разных клетках
- •2.2. Половой хроматин
- •2.3. Нуклеосомная организация хроматина
- •3. Ядрышко
- •3.1. Строение
- •4. Ядерная оболочка и матрикс
- •4.1. Ядерная оболочка
- •4.2. Ядерный матрикс
- •1.1. Клеточный цикл постоянно делящихся клеток
- •1.2. Клеточный цикл для клеток, прекращающих деление
- •1.2.1. Классификация клеток по способности к делению
- •2. Деление клеток
- •2. 1. Способы деления
- •2.1.2. Митоз
- •2.1.2.1. Стадии митоза
- •II. Метафаза
- •II. Характеристика хромосом
- •2.1.2.3. Уровни укладки хромосом
- •I. Конъюгация гомологичных хромосом и кроссинговер
- •II. Образование клеток с гаплоидным набором хромосом
- •2.1.3.3.Стадии мейоза
- •Вопросы для контроля
- •Практическая часть
- •Самостоятельная работа
- •Список рекомендуемой литературы
1.1.2. Приготовление гистологического препарата
По способу изготовления и характеру взятого материала различают следующие виды гистологических препаратов:
срезы фиксированных тканей (толщиной 5–15 нм);
препараты свежезамороженных срезов; мазки (крови, костного мозга и т. д.) и отпечатки (например, селезенки); пленки (брюшины, мягкой мозговой оболочки) или тотальные препараты.
Чаще всего используются срезы.
По длительности хранения:
временные препараты;
постоянные препараты.
Приготовление препарата обычно включает следующие этапы:
взятие и фиксация материала;
обезвоживание и уплотнение материала; приготовление срезов; окрашивание препаратов и заключение в консервирующую среду.
1.1.2.1. Взятие и фиксация материала
Взятие материала от исследуемого объекта. Образец получают несколькими путями:
- у живого объекта в результате оперативного иссечения кусочков тканей (биопсия),
- от животных, умерщвленных специально для этих целей;
- от трупов.
Из соответствующего органа вырезают небольшие кусочки (0,5 x 1,0 x 1,0 см) и погружают их в фиксатор (формалин, метанол и т. д.) обычно на сутки.
Фиксация производится для предупреждения процессов аутолиза тканей. После фиксации образцы промывают проточной водой в течение нескольких часов.
1.1.2.2. Обезвоживание и уплотнение материала
Затем образцы уплотняют, чтобы в последующем их можно было резать на микротоме. Часто в качестве уплотнителя используют парафин или целлоидин. Предварительно образцы обезвоживают (иначе гидрофобный уплотнитель не сможет проникнуть в ткань). Для этого их “проводят” по батарее спиртов – 70 %-ный, 80 %-, 96 %-ный, 100 %-ный этанол – по 24 часа в каждом спирте. Так как парафин нерастворим и в этаноле, образцы выдерживают затем в смеси этанол-ксилол и в чистом ксилоле. Заливка: помещают образцы в смесь ксилол-парафин и затем в жидкий парафин на 1–2 ч при 52–56 оС. Дают парафину, остывая, затвердеть, затем вырезают из него блок с заключенным образцом и закрепляют на деревянном кубике. |
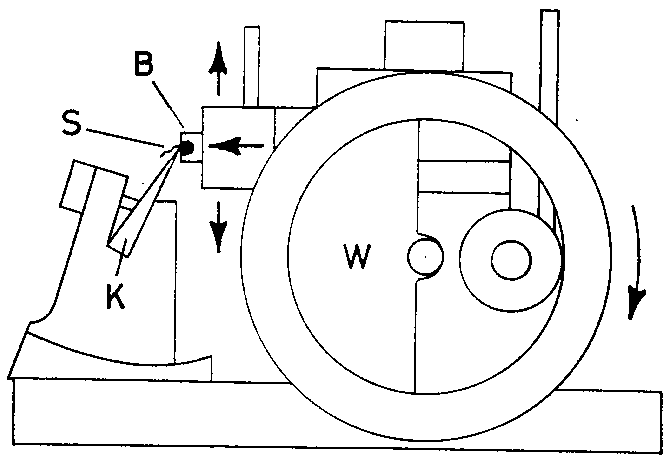
1.1.2.3. Приготовление срезов
Кубики (В) вставляют в специальный прибор – микротом, служащий для приготовления срезов. С помощью микрометрической механической системы (W) объектодержатель вместе с кубиком перемещается за каждый шаг на определённое расстояние (10 мкм). Микротомный нож (К), направляемый под углом к поверхности парафинового блока, срезает с него тонкой слой органа (S) (срез) заданной толщины. Срезы помещают на поверхность теплой воды для их расправления, а затем – на предметное стекло. |
|
1.1.2.4. Окрашивание препаратов и заключение в консервирующую среду
Перед окрашиванием образцы освобождают от парафина, проводя по батарее растворителей: ксилол, спирт 100 %-ный, 96 %-, 80 %-, 70 %-, 60 %-ный, вода (по 2–5 мин). Этот ряд заканчивается водой в том случае, если затем используется водорастворимый краситель. Для окрашивания предметные стекла со срезами помещают на короткое время в раствор красителя, промывают водой, обрабатывают раствором другого красителя (если таковой используется тоже) и вновь промывают водой. Препарат снова обезвоживают, проводя по батарее спиртов с возрастающей концентрацией, а затем просветляют в карбол-ксилоле и ксилоле для удаления лишней краски. |