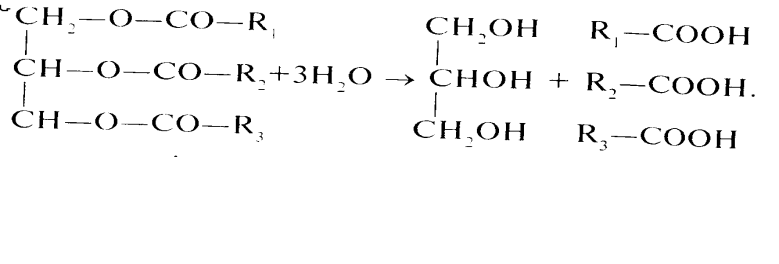- •Растворы1.Соль активного металла и бескислородной кислоты
- •3. Поняття про якісний та кількісний аналіз. Їх значення для сільськогосподарського виробництва та агроекологічного контролю.
- •5. Поняття про буферні системи. Буферна ємність.
- •6. Предмет, завдання аналітичної хімії. Якісний аналіз та його методи.
- •7. Специфічність та чутливість реакцій.
- •8))) Буферність грунтів
- •10. Гравіметричний метод кількісного аналізу
- •Органика
- •4) Аминокислоты — органические амфотерные соединения, в состав которых входят карбоксильные группы – соон и аминогруппы -nh2. Номенклатура
- •Физические свойства
- •I. Общие свойства
- •II. Свойства корбоксильной группы (кислотность)
- •III. Свойства аминогруппы (основность)
- •1. С сильными кислотами → соли:
- •I. Общие свойства
- •II. Свойства корбоксильной группы (кислотность)
- •III. Свойства аминогруппы (основность)
- •1. С сильными кислотами → соли:
- •6. Ліпіди, їх склад і хімічна будова. Властивості і знаходження в природі.
- •7.Карбонові кислоти та їх похідні, естери. Знаходження цих сполук у природі та об’єктах агросфери зокрема.
- •8. Вуглеводи, їх класифікація, будова, знаходження в природі. Вміст окремих видів вуглеводів у рослинах.
- •9.Дисахариди. Відновлюючі та невідновлюючі дисахариди. Мальтоза, лактоза, целобіоза, сахароза.
- •10. Високомолекулярні полісахариди. Крохмаль, глікоген, клітковина. Пектинові речовини.
Органика
1)Одноосновні насичені кислоти — похідні алканів, у молекулі яких атом Гідрогену заміщений на карбоксильну групу. Іноді їх називають кислотами жирного ряду, оскільки окремі з них виділені з продуктів гідролізу жирів.
Ізомерія і номенклатура. Загальна формула СnH2n+1— СООН.
Для кислот існує ізомерія вуглецевого ланцюга: кислоти з нормальною будовою карбонового ланцюга та кислоти з розгалуженим карбоновим ланцюгом, або з ізобудовою. Для найменування карбонових кислот користуються трьома номенклатурами — історичною, раціональною і ІЮПАК. Так, згідно з історичною номенклатурою карбонові кислоти, як правило, називають, виходячи з назви продуктів, з яких вони вперше були одержані. Наведемо назву карбонових кислот гомологічного ряду: Н — СООН — мурашина, СН3—СООН — ацетатна, СЛН5—СООН — пропіонова, С3Н7—СООН —- масляна, С4НЧ— СООН — валеріанова, С5НП—СООН — капронова, С6Н,,— СООН- енантова С7Н,5-СООН - каприлова, С8Н|7 - СООН — пеларгонова, С9Н]4—СООН — капринова, СІ0Н^)—СООН — ундеканова, СПНПЗ—СООН — лауринова, СрН,,—СООН — ди- деканова, С|3Н,7—СООН — міристинова, С]4Н,9—СООН — пентадецилова, С]5Н31—СООН — пальмітинова, С,6Н33—СООН — маргаринова, С|7Н35—СООН — стеаринова кислоти.
Раціональною номенклатурою користуються зрідка. За її основу береться ацетатна кислота, в молекулі якої один або кілька атомів Гідрогену радикала заміщені на інший або інші радикали. Наприклад, пропіонову кислоту СН,—СН,—СООН згідно з раціональною номенклатурою називають метилоцтовою кислотою.
За номенклатурою ІЮПАК назви карбонових кислот походять від відповідних алканів, до яких додають суфікс -ова. Нумерацію ланцюга починають з атома Карбону карбоксильної
групи. Наприклад, мурашина кислота називається .метановою кислотою, ацетатна — етановою тощо.
Залишки кислот після відняття групи —ОН від карбоксилу називають кислотними, або ацильними радикалами. Назви утворюються від кореня кислоти, з доданням суфіксу -ил, -іл (-оіл). Так, радикал мурашиної кислоти- Н—СО— називається формілом, ацетатної СН3—СО— — ацетилом.
Загальний спосіб добування карбонових кислот — окиснення альдегідів або спиртів із гідроксигрупою біля першого атома Карбону:
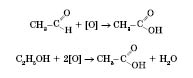
2) Фізичні властивості. Перші чотири гомологи одноосновних насичених карбонових кислот— безбарвні рідини з гострим запахом, змішуються з водою в різних співвідношеннях. Наступні представники (до капринової кислоти) — малорухливі рідини з неприємним запахом, решта — тверді речовини без запаху, майже не розчиняються у воді. Температура кипіння карбонових кислот з нормальним карбоновим ланцюгом вища, ніж відповідних їм кислот з розгалуженим ланцюгом. Кислоти з непарним числом атомів Карбону плавляться при нижчих температурах на відміну від найближчих сусідів у гомологічному ряду з парною кількістю атомів Карбону. Високі температури плавлення та кипіння кислот зумовлюються міжмолекулярними водневими зв'язками.
Головні хімічні реакції, в які вступають карбонові кислоти, пов'язані з їх кислотними властивостями, що базуються на рухливості атома Гідрогену карбоксильної групи; заміною групи — ОН карбоксильної групи на різні атоми й атомні групи з утворенням функціональних похідних кислот.
Утворення солей: 2СH3COOH + 2Na → 2CH3COONa + H2;
2СH3COOH + Na2O → 2CH3COONa + H2O;
СH3COOH + NaOH → CH3COONa + H2O;
Утв. Естерів:
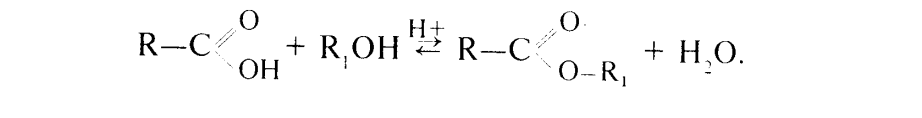
Реакція оки-ня:
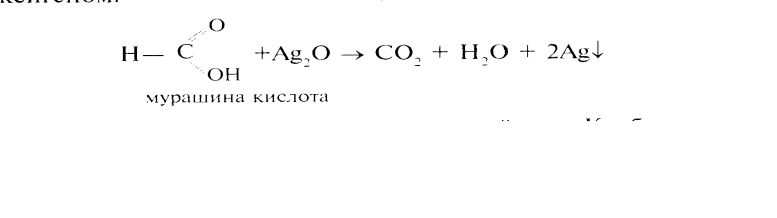
3) Ліпіди — це жири і жироподібні речовини, які відносяться до біологічно важливих сполук, що входять до складу кожної клітини живого організму. Як правило, більшість ліпідів є похідними вищих жирних кислот (ВЖК), вищих жирних спиртів (ВЖС) або альдегідів. Ліпіди є компонентами біологічних мембран, джерелом хімічної енергії і виконують захисні функції.
Ліпіди не розчиняються у воді, розчиняються у органічних розчинниках, деякі з них. самі є відмінними органічними розчинниками. Більшість ліпідів за будовою своїх молекул — естери. Розрізняють прості і складні ліпіди. Молекули простих ліпідів утворено залишками ВЖК (або альдегідів) і спиртів. До таких ліпідів відносяться нейтральні жири (григліцериди), діольні ліпіди, воски. Деякі автори до групи простих ліпідів відносять стерини і сгериди. Молекули складних ліпідів утворюються залишками молекул ВЖК, спиртів (часто ВЖС), неорганічних кислот (найчастіше Н2$04 і Н3Р04), нітрогенних основ (холін, коламін) і моносахаридів (галактози, глюкози, манози тощо). До складних ліпідів відносяться фосфатиди (фосфоліпіди), гліко- ліпіди і сульфатидн, іноді близькі до них хімічні сполуки, зокрема ВЖК, простагландини, деякі жиророзчинні вітаміни тощо.
Класифікація ліпідів Прості ліпіди:
Гліцериди,стероли,стерини,воски,діяльні сполуки. Складні ліпіди (основні класи) Фосфоліпіди ,Гліколіпіди ,сульфоліпіди
Прості ліпиди
Нейтральні жири — суміш тригліцеридів, молекули яких утворені триатомним спиртом гліцерином і ВЖК:
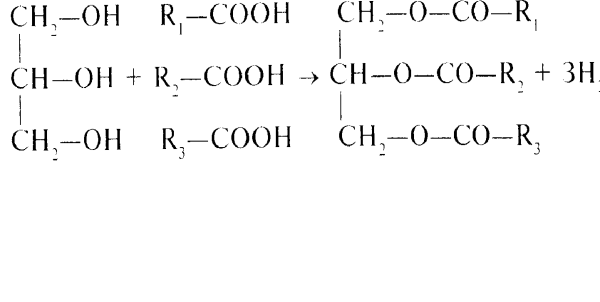
Тригліцериди найчастіше називають за ВЖК, що брали участь в утворенні їх молекул: тристеарин, триолеїн, стеароолеопаль- мітин, дистеаролінолен і т. д. Тваринні жири (крім вершкового масла) називають салами, рослинні — оліями, маслами.
ВЖК нейтральних жирів представлені насиченими, нена- сиченими і циклічними кислотами, а в деяких випадках і гідрок- сикислотами. Основу структури молекул жирів складають залишки жирних кислот, що мають 4—26 атомів Карбону.
Насичені карбонові кислоти найчастіше мають парну кількість атомів Карбону, наприклад: масляна С3Н7СООН, капронова С5Н11СООН, лауринова С11Н23СООН, міристинова С13Н27СООН, пальмітинова С15Н31СООН, стеаринова С17Н35СООН.
Ненасичені карбонові кислоти, залишки яких входять у молекули жирів, у складі радикалів можуть мати 1—4 подвійних зв'язків. Наприклад, олеїнова СН3(СН2)7СН ==СН(СН2)7СООН,
У молекулах деяких жирів виявлено залишки циклічних кислот, наприклад, хаульмугрової С17Н29СООН. У молекулах жирів зустрічаються і залишки гідроксикислот.априклад, тристеарин, трипальмітин, триолеїн) і складні (дистеаропальмітин, олеос- теаропальмітин).
Способи одержання і виділення жирів. Жири, як правило, одержують з природної сировини, іноді — синтетично. Тваринні жири виділяють із жирової тканини (наприклад, підшкіряна клітковина, сальник) витоплюванням на пару або відкритому вогні, рослинні — пресуванням або екстрагуванням. Екстрагентами найчастіше виступають діетиловий етер і ацетон.
Фізичні властивості. Рослинні жири, або олії — переважно рідини, а тваринні жири в більшості випадків тверді речовини і їх називають салами. Густина жирів менша одиниці (0,9— 0,96). Деякі фізичні та хімічні властивості наведено в табл. 27. Встановлено, що тварини одного і того ж виду, які живуть в північних широтах, мають жири з нижчими температурами плавлення, ніж тварини того ж виду, що живуть на півдні.
Чотири останні константи є показниками аналітичної характеристики жирів. Зокрема число омилення — кількість міліграмів їдкого калі, яка витрачається на омилення одного грама жиру кип'ятінням його з надлишком їдкого калі у спиртовому розчині. Число омилення визначається зворотним титруванням.
Омилення жирів: