
- •Раздел I общая микробиология: морфология, физиология и генетика микроорганизмов
- •Тема 1 ветеринарно-бактериологическая лаборатория. Техника микроскопирования. Основные формы бактерий. Определение размеров микроорганизмов
- •Тема 2 бактериологические красители. Приготовление бактериальных препаратов для световой микроскопии. Простые методы окраски бактерий
- •Задание для самостоятельной работы
- •Контрольные вопросы
- •Тема 3 сложные методы окраски бактерий: окраска по методам грама и циля-нильсена
- •Тема 4 окраска бактерий с целью выявления спор, капсул, цитоплазматических включений. Методы обнаружения жгутиков. Метод прямого флуорохромирования бактерий
- •Тема 5 микроскопические грибы
- •Тема 6 стерилизация
- •Тема 7 питательные среды и культивирование микроорганизмов
- •Тема 8 техника посева, методы выделения чистых культур и культуральные свойства микроорганизмов. Определение количества бактерий
- •Контрольные вопросы
- •Тема 9 ферментативные (биохимические) свойства и принципы идентификации микроорганизмов
- •Тема 10 бактериофаги
- •Тема 11 антибиотики. Определение чувствительности микроорганизмов к антибиотикам
- •Методические указания
- •Тема 12 генетика и генетические методы идентификации микроорганизмов
- •Раздел II инфекция и методы прикладной иммунологии
- •Тема 13 экспериментальное заражение лабораторных животных. Определение вирулентности и факторов патогенности микроорганизмов
- •Тема 14 методы определения факторов неспецифической резистентности и оценки иммунного статуса макроорганизма
- •Тема 15 серологические реакции: агглютинации (ра), непрямой гемагглютинации (рига), кумбса (рк). Оборудование для постановки серологических реакций
- •Тема 16 реакции преципитации (рп): кольцепреципитации (ркп), диффузионной преципитации (рдп); иммуноэлектрофорез
- •Тема 17 реакция связывания комплемента (рск)
- •Тема 18 метод флуоресцирующих антител (мфа). Иммуноферментный анализ (ифа)
- •Тема 19 реакция нейтрализации (рн)
- •Тема 20 средства специфической профилактики, терапии и диагностики инфекционных болезней
- •Тема 21 отбор, консервирование, транспортировка и хранение материала для микробиологического исследования. Принципиальная схема микробиологической диагностики инфекционных болезней
- •Раздел III частная микробиология
- •Тема 22
- •Лабораторная диагностика стафилококкозов и стрептококкозов. Биопрепараты
- •Тема 23 лабораторная диагностика рожи свиней и листериоза. Биопрепараты
- •Тема 24 лабораторная диагностика туберкулеза, паратуберкулеза, актиномикоза. Биопрепараты
- •Тема 25 лабораторная диагностика сибирской язвы. Биопрепараты
- •Тема 26 лабораторная диагностика злокачественного отека, анаэробной дизентерии ягнят, брадзота, инфекционной энтеротоксемии, эмфизематозного карбункула. Биопрепараты
- •Тема 27 лабораторная диагностика столбняка, ботулизма. Биопрепараты
- •Тема 28 лабораторная диагностика некробактериоза и копытной гнили. Биопрепараты
- •Тема 29
- •Тема 30 лабораторная диагностика сальмонеллеза. Биопрепараты
- •Тема 31 лабораторная диагностика чумы верблюдов и человека, псевдотуберкулеза. Биопрепараты
- •Тема 32 лабораторная диагностика бруцеллеза, туляремии.
- •Тема 33 лабораторная диагностика пастереллеза, гемофилезного полисерозита и актинобациллезной пневмонии свиней. Биопрепараты
- •Тема 34 лабораторная диагностика сапа, мелиоидоза и псевдомоноза норок. Биопрепараты
- •Тема 35 лабораторная диагностика лептоспироза, кампилобактериоза и дизентерии свиней. Биопрепараты
- •Тема 36 лабораторная диагностика микоплазмозов, риккетсиозов и хламидиозов. Биопрепараты
- •Тема 37 лабораторная диагностика дерматомикозов, микозов, вызываемых плесневыми и дрожжеподобными грибами. Биопрепараты
- •Тема 38 лабораторная диагностика микотоксикозов, вызываемых грибами родов aspergillus, penicillium, fusarium, stachybotrys, dendrodochium
- •Тема 39 санитарно-микробиологическое исследование воды, воздуха и почвы
Тема 14 методы определения факторов неспецифической резистентности и оценки иммунного статуса макроорганизма
Цель занятия. Ознакомить студентов с методами тестирования факторов неспецифической резистентности и методами оценки иммунного статуса животного организма.
Оборудование и материалы. Культура Е. coli на МПА стерильный МПБ, стерилизатор, шприцы и иглы, спиртово-водный раствор метиленового синего, нормальная и иммунная (противо-эшерихиозная) кроличьи сыворотки, стерильные пастеровские пипетки, 1%-й агар Дифко, ацетоновый порошок М. lysodeicticus (или культура), стерильные чашки Петри, кристаллический лизо-цим, фосфатно-солевой буферный раствор с рН 7,2...7,4, эритроциты барана, стерильный физиологический раствор, веронал-мединаловый буферный раствор с рН 7,3...7,4, гемолизин, комплемент морской свинки, дистиллированная вода, фотоэлектроколориметр, пластины с результатами радиальной иммунодиффузии по определению иммуноглобулинов разных классов в сыворотке крови, калибровочная кривая для определения содержания иммуноглобулинов разных классов; препараты для подсчета Е-РОК и ЕАС-РОК.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
Методы определения факторов неспецифической резистентности макроорганизма. Защиту макроорганизма от возбудителей инфекционных болезней обеспечивает не только иммунная система, но и механизмы неспецифического порядка: непроницаемость слизистых и кожных покровов, фагоцитоз, бактерицидное действие лизоцима, а также гуморальные факторы: комплемент, пропердин и др. Все эти механизмы (факторы неспецифической резистентности) представляют собой первую линию противоинфекционной защиты, поскольку при первичном контакте с возбудителем иммунный ответ развивается только спустя некоторое время.
Количественное определение лизоцима в сыворотке крови. Лизоцим — гидролитический фермент, расщепляющий высокомолекулярные полисахариды бактерий (пептидогликан), находится в тканях, секретах, экскретах (за исключением пота и мочи), действует бактерицидно на многие бактерии. Присутствие и активность лизоцима определяют по его способности вызывать лизис бактерии Micrococcus lysodeicticus.
Готовят 1%-й агаровый гель (Дифко) на 1/15 М фосфатно-солевом буферном растворе (ФСБР). В расплавленный агар температурой 60...70°С вносят ацетоновый порошок биомассы М. lysodeicticus из расчета 10 мг на 100 мл геля. Компоненты перемешивают и разливают в чашки Петри (толщина слоя 4 мм). В застывшем агаре делают лунки диаметром 5 мм.
Параллельно определяют активность стандартного лизоцима, кристаллизованного из яичного белка. Для этого лизоцим разводят в 1/15 М ФСБР, чтобы получить разведения с концентрацией 0,5; 1; 3; 5, 10; 20; 40 и 70мг/мл. По 0,05 мл каждого разведения лизоцима вносят в лунки. Чашки Петри выдерживают 48 ч во влажной камере при 37 °С и измеряют диаметр зоны лизиса М. lysodeicticus вокруг лунок.
По полученным данным строят калибровочную кривую, откладывая на осях координат значения концентрации лизоцима и диаметра зоны лизиса.
Сыворотку крови разводят в ФСБР в соотношении 1:5, вносят по 0,03 мл в лунки и далее поступают, как при определении активности стандартного лизоцима. Измерив диаметр зоны лизиса, по калибровочной кривой вычисляют содержание лизоцима в исследуемой пробе.
Количественное определение комплемента в сыворотке крови. Комплемент (С) представляет собой сложную систему главным образом неактивных белков крови. Процесс их активации (по классическому пути) запускается образованием комплекса антиген — антитело (АГ — AT) и происходит в виде цепной реакции: комплекс АГ • АТ+С1+С4+С2+Сз+С5+С6+С7+С8+С9. В процессе активации образуется литический комплекс, который делает мембрану клетки проницаемой, внутрь клетки осмотически по ступает вода, в результате клетка набухает и лопается. Такое разрушение клеток (антигенов) под влиянием антител и комплемента получило название иммунного лизиса. Наиболее эффективно комплемент действует на бактериальные клетки в сочетании с лизоцимом. Кроме того, бактериальные клетки (антигены) после взаимодействия с антителами и комплементом легче поглощаются фагоцитами.
Количество комплемента в крови (сыворотке крови) определяют в реакции иммунного лизиса с использованием эритроцитов барана и гемолизина в качестве антител к эритроцитам барана. Приготовление этих компонентов изложено в теме 17. Эритроциты барана, обработанные гомологичными антителами и чувствительные в таком состоянии к литическому действию комплемента, называют гемолитической системой. Количество комплемента измеряют в 50 % гемолитических единицах (СН50). За единицу комплемента принимают такое его количество в объеме 0,5 мл, которое за 30 мин при 37 °С обусловливает лизис 50 % эритроцитов в 0,5 мл гемолитической системы (5%-я суспензия эритроцитов барана в веронал-мединаловом буферном растворе с рН 7,3...7,4+ гемолизин в тройном титре).
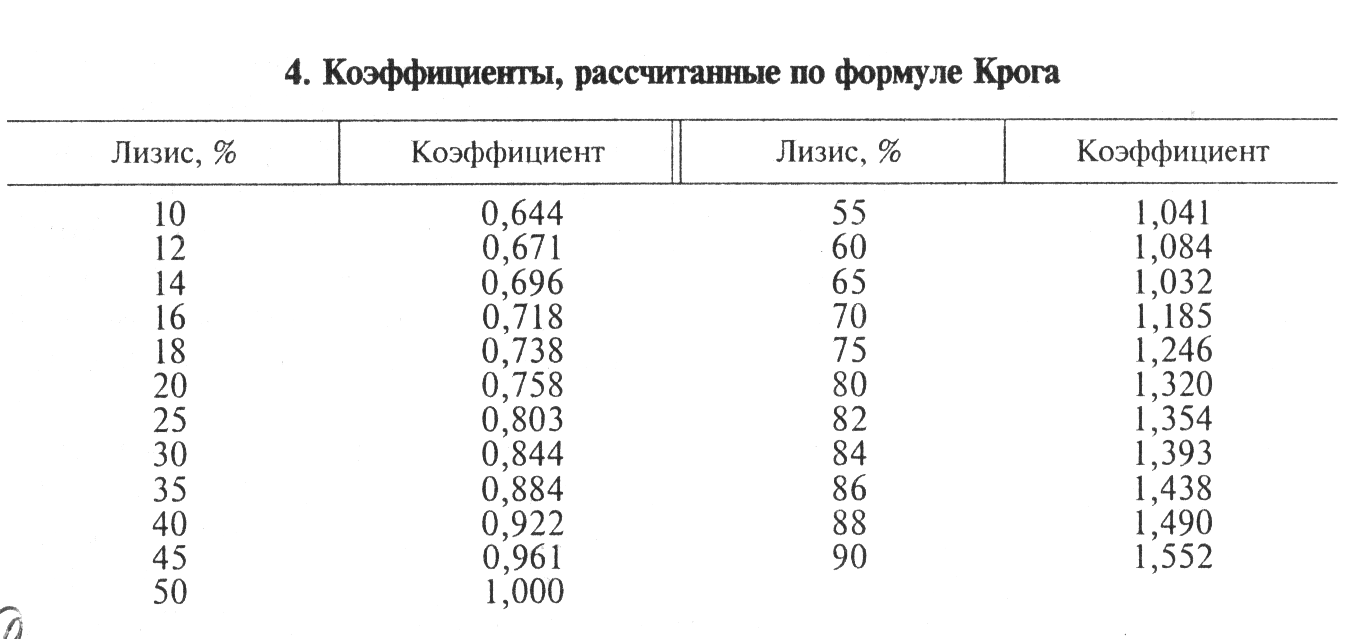
Исследуемую сыворотку в возрастающих дозах разливают по пробиркам (например, 0,02; 0,03; 0,04; 0,05; 0,08; 0,1 мл), добавляют ФСБР до 0,5;мл, вносят во все пробирки по 0,5 мл стандартизированной гемсистемы. Одновременно ставят контроль на резистентность эритроцитов (0,5 мл ФСБР + 0,5 мл гемсистемы). Пробирки встряхивают и выдерживают при 37°С 30 мин, охлаждают при 2...4'°С 10 мин, центрифугируют при 3000 мин-1 15...20 мин, насадочную жидкость колориметрируют и по коэффициенту экстинкции определяют процент гемолиза при помощи заранее построенной калибровочной кривой. Калибровочную кривую строят следующим образом: к 1 мл 5%-й суспензии эритроцитов добавляют 3 мл дистиллированной воды, эритроциты при этом полностью лизируются (100%-й гемолиз). Из полученного лизата путем добавления буферного раствора готовят пробы с 10-, 20-, 30-, 40-, 50-, 60-, 70-, 80-, 90%-м гемолизом. На фотоэлектроколориметре определяют оптическую плотность каждой пробы (кювета шириной 1 мм, синий светофильтр), затем на оси абсцисс откладывают процент гемолиза, а на оси ординат — коэффициент экстинкции. СН5о вычисляют по дозе сыворотки, дающей гемолиз, наиболее близкий к 50 %. Для этого используют специальную формулу (Крога) или, что проще, коэффициенты, рассчитанные по этой формуле (табл. 4).
Например, если исследуемая сыворотка в разведении 1 : 25 дает 30%-й лизис, то СН50 в 1 мл составит 25 • 0,844 = 21,1 ед.
Демонстрация фагоцитоза бактерий. К фагоцитирующим клеткам относят полиморфноядерные лейкоциты крови. Поглощение микробной клетки фагоцитом может не сопровождаться гибелью микроорганизма (незавершенный фагоцитоз) или приводить к внутриклеточному перевариванию захваченных бактерий (завершенный фагоцитоз).
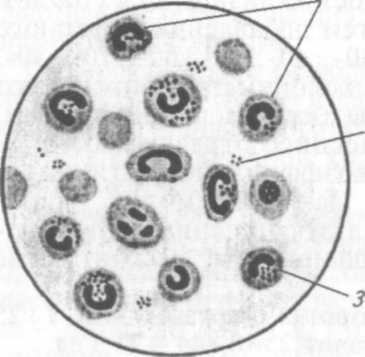
Белой мыши внутрибрюшинно сначала вводят 2 мл стерильного МПБ, через два-три часа — 0,5 мл культуры эшерихий. Спустя 20...40 мин шприцем из брюшной полости отбирают экссудат, делают мазки на предметном стекле, фиксируют спирт-эфиром, окрашивают метиленовым синим (экспозиция 2...3 мин). При микроскопировании можно наблюдать различные стадии фагоцитоза: поглощение, деструкцию (переваривание) клеток (рис. 55).
Методы оценки активности фагоцитирующих клеток. Для оценки активности фагоцитов используют следующие показатели:
1) фагоцитарный показатель — процент фагоцитирующих клеток от общего числа учтенных нейтрофильных лейкоцитов;
2) фагоцитарное число — среднее число микробных клеток, поглощенных одним лейкоцитом (характеризует интенсивность фагоцитоза).
Рис.
55. Фагоцитоз стафилококков:
1
— фагоциты; 2 — свободные
стафилококки; 3 — фагоцитированные
стафилококки
Определение фагоцитарного числа: в мазках, которые были приготовлены для определения фагоцитарного показателя, подсчитывают 100 нейтрофильных лейкоцитов и суммарное количество захваченных ими бактериальных клеток, затем определяют фагоцитарное число. Например, 100 лейкоцитов поглотили 500 бактериальных клеток, следовательно, фагоцитарное число равно 500 : 100 = 5.
Определение опсоно – фагоцитарного индекса. Интенсивность фагоцитоза повышается благодаря антителам — опсонинам, взаимодействующим с микробными клетками. Чтобы определить опсоно-фагоцитарный индекс, сравнивают активность фагоцитов в нормальной и исследуемой (иммунной) сыворотках.
Пастеровской пипеткой набирают на высоту капилляра около 2 см сначала суспензию бактериальных клеток (0,5 • 109/мл), затем лейкоцитов и, наконец, исследуемую сыворотку. На предметном стекле компоненты перемешивают при помощи пипетки, затем вновь набирают в капилляр, конец которого запаивают. Капилляр помещают в термостат при 37 °С на 30 мин. После инкубирования смесь выливают на предметное стекло, готовят мазок и окрашивают его метиленовым синим (1 мл насыщенного спиртового раствора на 30 мл дистиллированной воды).
Аналогичным образом готовят препарат с нормальной (контрольной) сывороткой. Оба препарата микроскопируют, просматривают 100 нейтрофильных лейкоцитов, определяют количество фагоцитированных бактерий, рассчитывают фагоцитарное число в каждой сыворотке и затем опсоно-фагоцитарный индекс исследуемой сыворотки. Например, в 100 лейкоцитах нормальной сыворотки фагоцитировано 200 бактерий, следовательно, фагоцитарное число 200: 100 = 2. В 100 лейкоцитах исследуемой иммунной сыворотки захвачено 500 бактерий и фагоцитарное число 500 : 100 = 5.
Опсоно-фагоцитарный индекс показывает, во сколько раз процесс фагоцитоза в иммунной сыворотке интенсивнее, чем в нормальной. Его вычисляют делением фагоцитарного числа иммунной сыворотки на фагоцитарное число нормальной сыворотки. В приведенном примере опсоно-фагоцитарный индекс составит 5,0:2,0 = 2,5.
Методы оценки иммунного статуса макроорганизма. Работа иммунной системы, как и любой другой системы организма, может нарушаться, что неизбежно повысит восприимчивость животного к инфекционным заболеваниям.
Методы оценки Т-системы иммунитета (клеточный иммунитет). Из числа существующих методов оценки Т-иммунитета наиболее известны следующие.
Метод «спонтанных розеток» (Е—РОК). Т-Лимфоциты несут на своей поверхности рецепторы, реагирующие с мембранными структурами эритроцитов барана. После сорбции эритроцитов Т-клетки приобретают форму «розетки», что позволяет выявлять их в популяции лимфоцитов. Реакцию проводят в три этапа.
Выделение лимфоцитов барана: в центрифужную пробирку наливают 2 мл разделяющего раствора, состоящего из 9%-го водного раствора фиколла и визотраста-370, доведенного до плотности 1,077 г/мл (соотношение 8:2). Затем на разделяющий раствор осторожно наслаивают 2...4 мл крови с гепарином (100 МЕ/мл), разведенной средой Игла в соотношении 1 : 2...1:4. Смесь центрифугируют при 600g и температуре 20 °С. Лимфоциты, сконцентрированные в виде беловатого слоя над разделяющим раствором, отсасывают пастеровской пипеткой и отмывают средой Игла (при 600g— 10 мин два раза, 200g — 10 мин один раз).
Инкубация: средой Игла концентрацию лимфоцитов доводят до 3 • 106/мл. Готовят суспензию эритроцитов барана, эритроциты отмывают 0,15 М раствором хлорида натрия (три раза), затем из них готовят 0,5%-ю суспензию в среде Игла. Далее смешивают по 0,5 мл суспензии лимфоцитов и эритроцитов, смесь центрифугируют при 200g 5 мин и оставляют при 4 °С на 18 ч.
Учет реакции: осторожно покачивая пробирку, ресуспендиру-ют осадок (не перемешивая), каплю суспензии вносят в счетную камеру и исследуют методом фазово-контрастной микроскопии. Просматривают не менее 200 лимфоцитов и подсчитывают те клетки, к поверхности которых прикреплено более трех эритроцитов (рис. 56), — естественные розеткообразующие клетки (Е— РОК).
Технология выращивания животных отражается на их физиологическом состоянии и на количестве Т- и В-клеток в частности (табл. 5).

Выявление Т-хелперов и Т-супрессоров. Т-хелперы и Т-супрессоры несут на своей поверхности специфические антигены, которые можно обнаружить при помощи мышиных моноклональных антител (см. тему 20) в реакции непрямой иммунофлуоресценции (см. тему 18). Лимфоциты, связавшие моноклональные антитела, светятся по периферии клеток, что позволяет определить их количество при микроскопическом исследовании.
Методы оценки В-системы иммунитета (гуморальный иммунитет). Включают в себя оценку В-лимфоцитов (общее содержание в крови, анализ антигенных детерминант) и вырабатываемых ими антител.
2 оличественное
определение иммуноглобулинов разных
классов
методом радиальной иммунодиффузии (по
Манчини). Количество и соотношение
иммуноглобулинов отдельных классов
в биологических жидкостях отражают
состояние В-системы. Методика постановки
реакции изложена согласно Ю. Н. Федорову
(1981).
оличественное
определение иммуноглобулинов разных
классов
методом радиальной иммунодиффузии (по
Манчини). Количество и соотношение
иммуноглобулинов отдельных классов
в биологических жидкостях отражают
состояние В-системы. Методика постановки
реакции изложена согласно Ю. Н. Федорову
(1981).
Иммунную сыворотку против антител определенного класса (IgG, IgM, IgA) вносят в расплавленный агаровый гель. После застывания агара антитела в нем равномерно распределены. Внесенный в лунку исследуемый материал (антиген) радиально диффундирует в толщу геля. Поскольку концентрация антител везде одинакова, то в результате реакции антиген — антитело в зоне эквивалентности образуются не полосы преципитации, а кольцо преципитации вокруг лунки с антигеном (рис. 57). Диаметр кольца преципитации прямо пропорционален концентрации антигена в исследуемой жидкости.
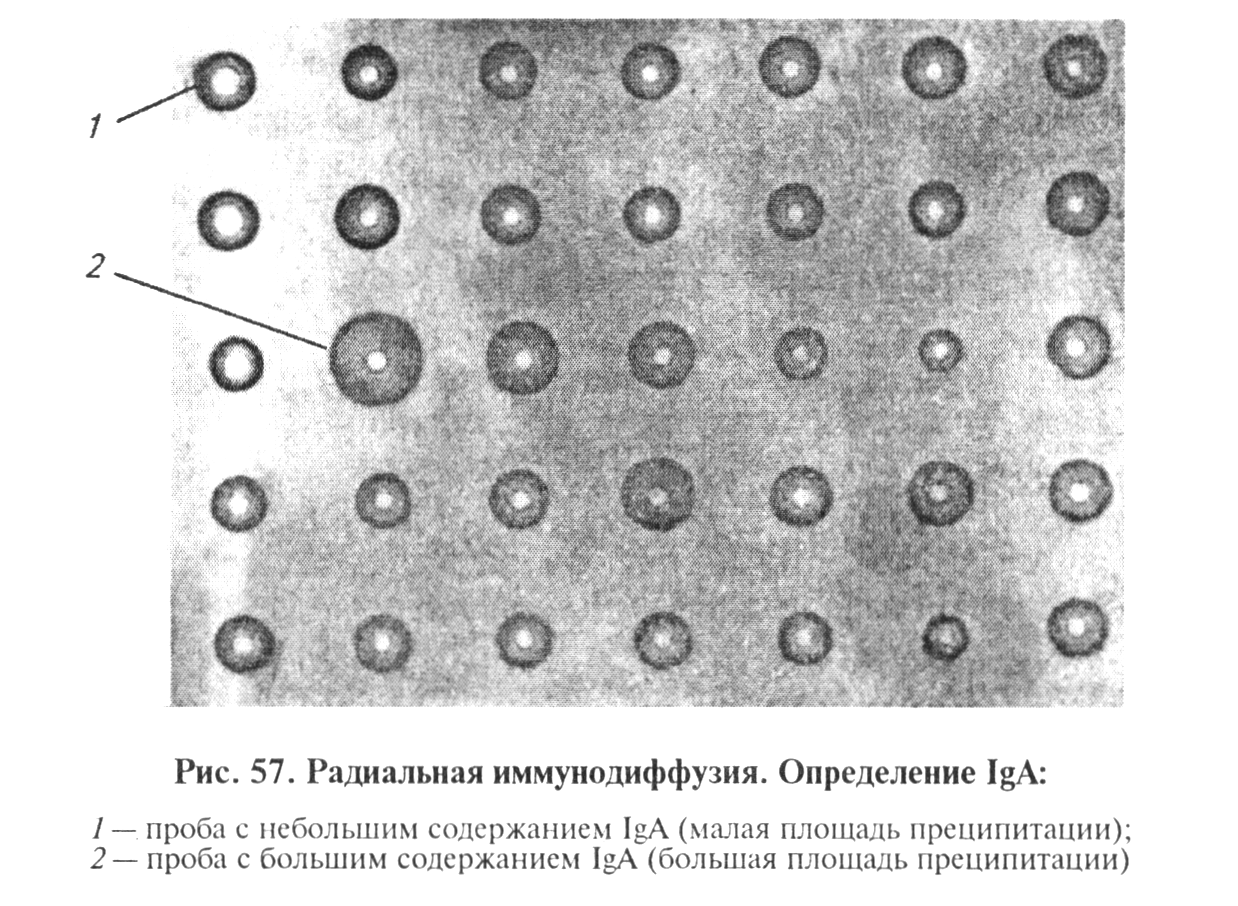
В предварительных опытах определяют оптимальное (рабочее) разведение антисывороток к иммуноглобулинам каждого класса. В каждом опыте устанавливают количество иммуноглобулинов в В агаре пробойником вырезают лунки диаметром 2 мм (5 рядов по 7 лунок в каждом). В лунки первого ряда вносят разведения стандартной сыворотки, в остальные — исследуемые пробы по 1 мкл. Пластинку выдерживают во влажной камере 24 ч (IgG, IgA) или 48 ч (IgM).
 Строят
калибровочную кривую. На оси абсцисс
откладывают значения диаметров колец
преципитации разведенной стандартной
сыворотки, на оси ординат — значения
концентраций иммуноглобулинов (% или
мг/мл). Измеряют диаметр колец преципитации
в пробах и по калибровочной кривой
устанавливают концентрацию
соответствующего иммуноглобулина.
Строят
калибровочную кривую. На оси абсцисс
откладывают значения диаметров колец
преципитации разведенной стандартной
сыворотки, на оси ординат — значения
концентраций иммуноглобулинов (% или
мг/мл). Измеряют диаметр колец преципитации
в пробах и по калибровочной кривой
устанавливают концентрацию
соответствующего иммуноглобулина.
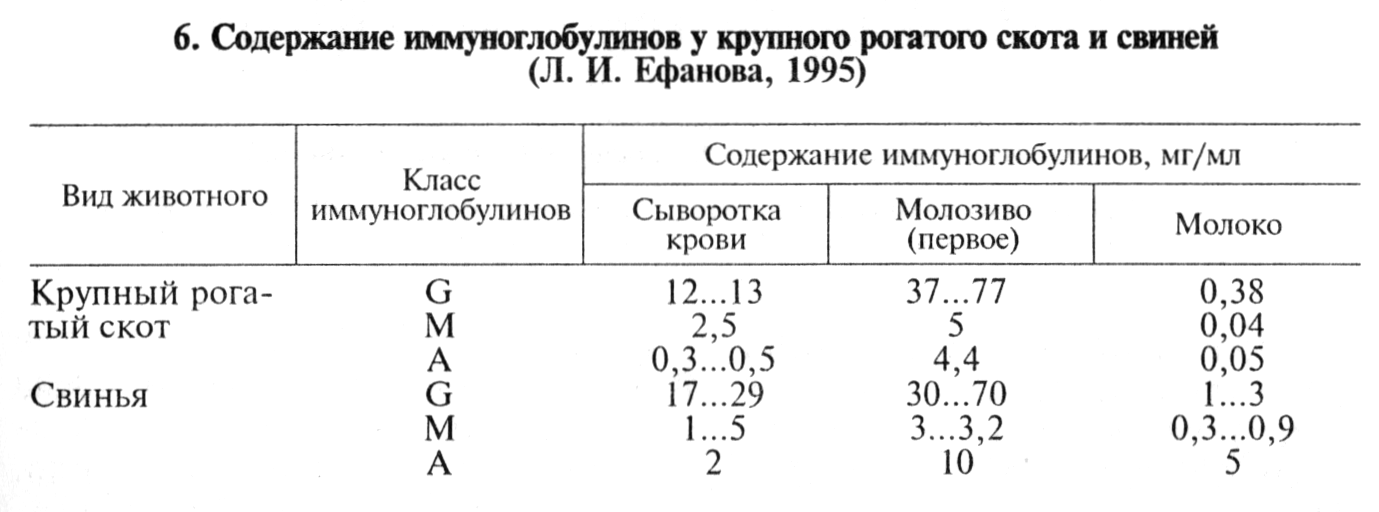
Количество иммуноглобулинов разных классов в биологических жидкостях варьирует в широких пределах (табл. 6).
Все методы определения В-лимфоцитов в крови основаны на выявлении на поверхности В-лимфоцита структур, специфических только для В-клеток: рецепторы к Fc-фрагменту иммуноглобулинов, рецепторы к С3-фракции комплемента, иммуноглобу- линовые рецепторы, а также специфические В-антигены.
Метод розеткообразования (ЕАС—РОК): эритроциты барана обрабатывают антителами гемолизина, затем комплементом. Образуется комплекс АГ—AT—С, содержащий компонент комплемента С3. Далее смешивают лимфоциты животного и обработанные эритроциты барана. Эритроциты за счет присутствующих на их поверхности молекул С3 избирательно сорбируются на В-лимфоцитах, образуя «розетки».
Другие методы основаны на выявлении рецепторов к Fc-фрагментам иммуноглобулинов и иммуноглобулиновых детерминант на поверхности В-клеток. Рецептор к Fc-фрагменту иммуноглобулинов способен связывать агрегированный γ-глобулин, меченный флуорохромом, что можно в последующем установить при помощи флуоресцентного анализа.
Используя меченные флуорохромом антиглобулиновые сыворотки или антисыворотки против иммуноглобулинов отдельных классов, например моноклональные антитела (см. тему 21), можно определить общее содержание В-клеток и дифференцировать клетки, несущие IgG-, IgA-, IgM-детерминанты.
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
Ознакомиться с фагоцитозом методом микроскопии мазков из перитонеального экссудата мышей после введения в брюшную полость культуры эшерихий.
Определить опсоно-фагоцитарный индекс иммунной сыворотки против Е. coli.
3. Оценить результаты титрования лизоцима в крови.
Ознакомиться с иммунным лизисом эритроцитов, определить содержание комплемента в сыворотке крови морской свинки.
Подсчитать количество Е—РОК лимфоцитов в готовых препаратах.
Оценить результаты реакции радиальной иммунодиффузии и рассчитать, используя готовую калибровочную кривую, содержание иммуноглобулинов разных классов в сыворотке крови.
Контрольные вопросы
1. Из каких стадий состоит процесс фагоцитоза?
2. Что такое фагоцитарное число, фагоцитарный показатель, опсоно-фагоцитарный индекс?
3. Как определяют активность комплемента?
4. Какими методами определяют количество иммуноглобулинов разных классов в биологических жидкостях?
5. Какие методы применяют для оценки В- и Т-систем иммунитета?
