
- •Химическая термодинамика
- •Часть 1
- •Термохимия
- •Цель работы
- •Теоретическая часть
- •Экспериментальная часть
- •Порядок выполнения работы
- •Обработка результатов эксперимента
- •Расчет теплоты образования твердого раствора kCl . RBr
- •Определение изменения температуры в калориметрическом опыте
- •Расчет теплоты образования кристаллогидрата
- •Контрольные вопросы
- •II. Изучение равновесия гомогенной реакции в растворе
- •Цель работы
- •Теоретическая часть
- •Экспериментальная часть
- •Порядок выполнения работы
- •Обработка экспериментальных данных
- •Контрольные вопросы
- •III. Определение коэффициента распределения иода между органическим и неорганическим растворителями
- •Цель работы
- •Теоретическая часть
- •Экспериментальная часть
- •3.2. Порядок выполнения работы
- •Обработка результатов эксперимента
- •Контрольные вопросы
- •IV. Изучение взаимной растворимости в трехкомпонентных системах
- •Цель работы
- •Теоретическая часть
- •Экспериментальная часть
- •Порядок выполнения работы
- •Обработка экспериментальных данных
- •Контрольные вопросы
- •Литература
- •Содержание
- •Термохимия
Контрольные вопросы
Как влияет температура на константу равновесия? Что является мерой этого влияния? Напишите соответствующее уравнение.
Выразите в общем виде Кз для реакции:
СО + 2Н2 СН3ОН(газ),
Если при данной температуре Т и давление Р равновесное количество моль метанола равно Х, а начальные количества компонентов, взятых для реакции, составляют 1 моль СО и 3 моль Н2.
Как изменится равновесный выход водорода по уравнению:
СН4 + 2Н2S CS2 + 4H2
При повышении общего давления в системе, если все вещества находятся в идеальном газовом состоянии? Ответ мотивировать.
Напишите уравнение изотермы для реакции: Н2 + Br2 2HBr.
Все вещества находятся в идеальном газообразном состоянии.
Нарисуйте графики зависимости ln К от обратной температуры для экзотермической и эндотермической реакций.
Теплота образования (
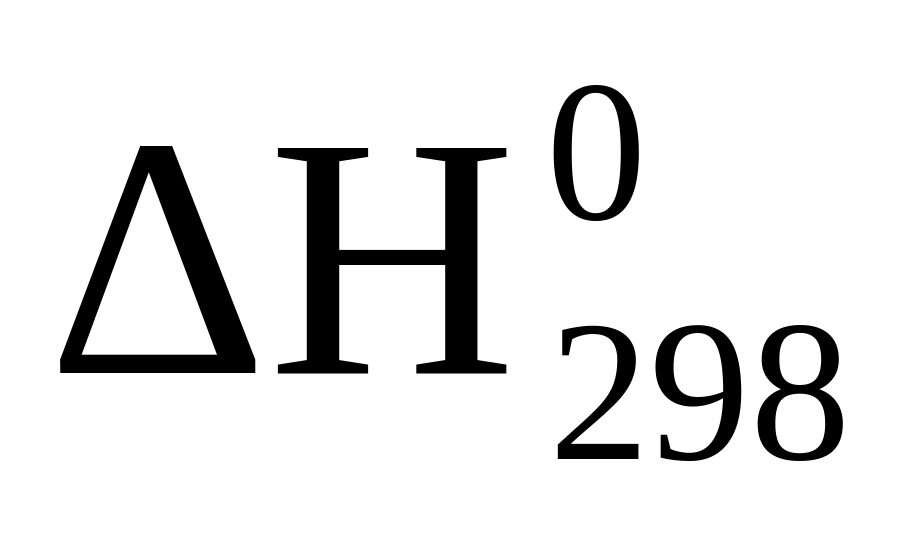 )
HCl5(тв)
равна -463,5 кДж/моль.
)
HCl5(тв)
равна -463,5 кДж/моль.
Как нужно изменить давление и температуру, чтобы увеличить равновесный выход пентахлорида фосфора в реакции его образования?
Для каких реакций константа равновесия Кр равна равновесному давлению в системе при данной температуре? Приведите пример.
Для реакции N2 + O2 2NO зависимость константы равновесия от температуры выражается уравнением:
lgKp
= -
![]() - 0,02 lgT
+ 1,43
- 0,02 lgT
+ 1,43
Выведите уравнение зависимости ΔН этой реакции от температуры.
В каком соотношении находятся величины Кр и Кс для реакции:
S2(тв) + 4Н2О 2SO2(газ) + 4Н2(газ)?
Напишите уравнение, связывающее стандартное сродство ΔG и константу равновесия Кр при постоянных Р и Т, если давление выражено в паскалях.
Изменится ли и как значение константы равновесия Кр реакции
А + 2В АВ2, если общее давление в системе увеличить в 2 раза? Все вещества находятся в идеальном газообразном состоянии.
5.12. Зависимость константы равновесия реакции
2Cl2 + 2H2O(газ) 4НСl(газ) + О2
от температуры можно выразить уравнением: lg Kp = - 6007/T + 5,407. Выделяется или поглощается тепло в этой реакции?
Степень диссоциации HBr не зависит от давления, но в то же время увеличивается с ростом температуры. Объясните эти факты.
Сопоставьте равновесный выход продуктов двух реакций, протекающих в одинаковых условиях (Р, Т) в газовой фазе
А + В АВ (1) и С + D CL (2), если ΔG1 > ΔG2.
5.15. Можно ли и в каких случаях по знаку изменения энтальпии в ходе химической реакции судить о возможности ее протекания при постоянных давлении и температуре?
5.16. Укажите, какие из факторов:
а) давление; б) температура; в) присутствие инертного газа; г) природа реагирующих веществ; д) парциальные давления взятых для реакции веществ- влияют на константу равновесия реакции Кр, если она протекает между веществами в идеальном газообразном состоянии.
5.17. Чему равна при 298 К константа равновесия реакции
2Ag(тв) + 1/2О2 Ag2O(тв)
если давление диссоциации Ag2O при этой температуре равно 5 . 10-9 Па?
5.18. Выразите в общем виде величину Кс для реакции
2SO 3 2SO2 + O2,
если диссоциации подвергаются n моль SO3. Общий объем равновесной смеси равен V, а степень диссоциации SO3 равна α.
