
- •«Реакции поликонденсации и полиприсоединения. Способы проведения полимеризации и поликонденсации».
- •Взаимодействие фенола с формальдегидом идет по схеме:
- •Получение полиорганосилоксанов с линейными цепями молекул (органосилоксановых эластомеров):
- •Получение полиорганосилоксанов с разветвленными и циклическими цепями
- •5) Полиалкилсилоксаны с алкильными радикалами с4 и более у атома Si.
«Реакции поликонденсации и полиприсоединения. Способы проведения полимеризации и поликонденсации».
№1. Классификация реакций поликонденсации.
Поликонденсация - это процесс образования ВМС из
мономеров, сопровождающийся выделением простейших низкомолекулярных соединений (вода, аммиак, галогенводород и др.).
В качестве мономеров в данном случае выступают би- или полифункциональные соединения. При их взаимодействии отщепляется молекула простого вещества и образуется новая группа, связывающая остатки реагирующих молекул. Поэтому в отличие от полимеризации в данном случае состав элементарного звена полимера не соответствует составу исходных мономеров.
В общем виде реакцию поликонденсации можно представить схемой:
n (a–A–a) + n (в–В–в) а–(А–В)х–в + (2n-1)ав
мономер мономер полимер
Здесь А и В – радикалы, входящие в состав мономеров, а и в- их функциональные группы, ав – низкомолекулярное вещество, выделяющееся в результате реакции.
Реакции поликонденсации всегда идут по ступенчатому механизму, т.е. с образованием устойчивых димеров, тримеров, тетрамеров и т.д., а рост цепи происходит постепенно. Это роднит их с реакциями ступенчатой полимеризации. Прекращение роста цепи наступает вследствие резкого снижения концентрации исходных мономеров и достижения равновесия между полимерными продуктами и низкомолекулярными веществами. Промежуточные продукты реакции поликонденсации устойчивы, и их можно выделить. При этом они сохраняют свою реакционную способность по причине наличия непрореагировавших функциональных групп.
Классификация реакций поликонденсации:
1 участвуют разнородные молекулы молекулы 
участвуют однородные молекулы Пример: синтез полимера полигексаметилендиамида (полиамида-6,6) из гексаметилендиамида и адипиновой кислоты. Полимер используют для формования волокна анид:
Пример: синтез полимера ω-аминоэнантовой кислоты, из которого формуют синтетическое волокно полиамид-7 (энант, найлон-7). Механизм ступенчатой поликонденсации этого полимера можно представить следующим образом:
1 n HOOC (CH2)4 COOH + HNH (CH2)6 NH2 мономер мономер
(2n-1 ) H2O + + HO C (CH2)4 CO NH (CH2)6 NH H O n полимер (полиамд-6,6)
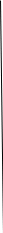 .
H2N (CH2)6 COOH + HNH (CH2)6 COOH
.
H2N (CH2)6 COOH + HNH (CH2)6 COOH
ϖ-аминоэнантовая кислота (мономер) H2N (CH2)6 CO NH (CH 2)6 COOH Димер 2. H2 N (CH2)6 CO NH (CH2)6 COOH + HNH (CH2)6 COOH димер
H2 N (CH2)6 CO NH (CH2)6 CO NH (CH2)6 COOH + H2O тример и т.д.
Повторяющимся структурным элементом полимера является звено ( NH (CH2)6 CO ), которое содержит 7 атомов углерода, поэтому формулу полимера ω-аминоэнантовой кислоты можно изобразить так: H NH (CH2)6 C OH O n полиамд-7 (найлон-7)
|
|
2 . На линейную и трехмерную:
п В случае поликонденсации соединений, содержащих более двух функциональных групп, образуются полимеры с разветвленной и пространственной структурами. Пример: реакция поликонденсации трехатомного спирта – глицерина с двухосновной терефталевой кислотой: n CH2 CH CH2 + n HOOC COOH OH OH OH глицерин терефталевая кислота
... O CH2 CH CH2 O C C O CH2 CH CH2 O C C O ... OOC O O OOC O O
OOC OOC ... O CH2 CH CH2 O C C O CH2 CH CH2 O C C O ... O O O O полимер сетчатой структуры 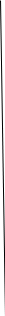 олучают
при поликонденсации
олучают
при поликонденсации
бифункциональных соединений
3. На обратимые и необратимые. Реакции поликонденсации часто бывают обратимыми. Скорость реакции сдвигают в нужную сторону выведением из реакции побочных продуктов (например воды), повышая тем самым концентрации реагирующих вещ еств.
|
|
4. Важнейшие реакции
Синтез полиуретанов, из которых формуют высокоэластичные полиуретановые волокна (спандекс-волокна). Их получают путем поликонденсации дихлоругольных эфиров гликолей (n Cl C O R O C Cl) О О с диаминами (Н2N – R – NH2) или сополимеризацией гексаметилендиизоционата(O=C=N–(CH2)6–N=C=O) с тетраметиленгликолем. Полиуретаны широко применяют в различных отраслях промышленности, например, для получения синтетических волокон, пенистых пластиков (поролонов), пленочных материалов, клеев, лаков и т.д.
|
Синтез мочевиноформальдегидных смол линейного и разветвленного строения. Получают по реакции поликонденсации мочевины и формальдегида в присутствии щелочных и кислотных катализаторов. В начальной стадии одна или две молекулы формальдегида присоединяются к молекуле мочевины, образуя низкомолекулярные соединения моно- и диметилолмочевину: H H N NH CH2 OH NH CH2 OH C O + CH 2 O C O + CH2 O C O NH2 формальдегид NH2 NH CH2 OH мочевина диметилол- метилолмочевина мочевина Эта реакция протекает в щелочной среде. Смесь образующихся продуктов получила название предконденсаты термореактивных смол. Их используют в отделочном производстве для улучшения потребительских свойств текстильных изделий и в швейном производстве для придания изделиям устойчивой формы. В кислой среде молекулы моно- и диметилолмочевины взаимодействуют друг с другом по реакции поликондесации, образуя высокомолекулярную смолу линейной или разветвленной структуры: ... HN CH2 OH HN CH2 OH C O + C O + ... -n H O 2 NH CH2 OH NH2
... CH2 N CH2 N CH2 N CH2 N ... C O C O C O C O NH CH2 OH NH2 NH2 NH CH2 OH
Линейныйполимер При дальнейшей поликонденсации выделяется вода за счет групп –NH– и –СН2–ОН разных цепей. При этом образуется пространственный полимер с сетчатой структурой: ... N ... ... N ... C O C O ... N CH2 N CH2 N CH2 N CH2 N ... C O C O C O ... N CH2 N CH2 N ... ... CH2 N CH2 N CH2OH C O C O ... N ... ... N ... Указанные реакции могут протекать в структуре волокнообразующих полимеров, изменяя их свойства, что используется в практике текстильного и швейного производств для придания изделиям свойств малосминаемости, малоусадочности, при изготовлении искусственной кожи, деталей машин и т.д. |
№2. Особенности реакций ступенчатой полимеризации, их отличия от реакций
полимеризации.
Реакции полимеризации - химические реакции, в которых получают полимеры. Существует много различных типов этих реакций, но все из них обладают одним общим свойством: все они начинаются с маленьких молекул и соединяются в большие, даже гигантские молекулы. Исходные маленькие молекулы называются мономерами.
Эта система подразделяет реакции получения полимеров на два типа.
Полимеризация и поликонденсация.
Реакция полимеризации - если молекула мономера целиком становится частью молекулы полимера.
Реакция поликонденсации - если некоторая часть молекулы мономера оказывается лишней, когда мономер становится частью молекулы полимера. Эта часть, которая оказывается лишней - как правило, небольшая молекула вроде молекулы воды или газообразного хлористого водорода HCl.
Рассмотрим несколько примеров, чтобы прояснить этот вопрос.
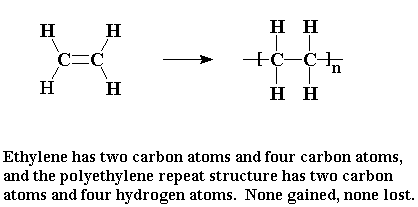
Когда этилен полимеризуется с образованием полиэтилена, то каждый атом из молекулы этилена становится частью полимера. Мономер просто напрямую присоединяется к молекуле полимера. Вы можете сказать, что полимер, полученный в результате такого присоединения, похож на хорошего друга, который принимает вас такими, какие вы есть - не разделяя ваши черты на достоинства и недостатки.
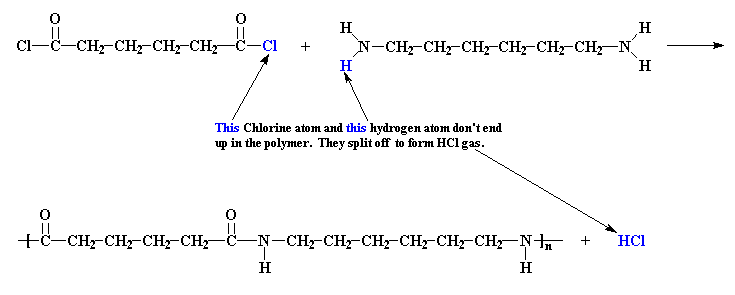
Но полимер, получаемый при реакции поликонденсации, скорее похож на высокомерное общество, которое заявляет вам: "Конечно, вы можете присоединиться, но только при условии, если вы избавитесь от этих ваших знакомых". Видите ли, при поликонденсации некоторые атомы из молекулы мономера, в конце концов, оказываются за пределами молекулы полимера. Когда из хлорангидрида адипиновой кислоты и гексаметилендиамина образуется найлон 6,6, то атомы хлора из молекулы хлорангидрида адипиновой кислоты, каждый в компании с одним атомом водорода из молекулы амина, высвобождаются в виде газообразного HCl.
 И
поскольку масса полимера меньше, чем
масса исходных мономеров, то мы говорим,
что полимер конденсируется по отношению
к своим мономерам. Побочный продукт
этой реакции, будь то вода, газобразный
хлористый водород HCl или что бы то ни
было, называется продукт конденсации.
И
поскольку масса полимера меньше, чем
масса исходных мономеров, то мы говорим,
что полимер конденсируется по отношению
к своим мономерам. Побочный продукт
этой реакции, будь то вода, газобразный
хлористый водород HCl или что бы то ни
было, называется продукт конденсации.
Вывод: При реакции поликонденсации образуются побочные продукты, а при реакции полимеризации - нет.
Существует система классификации реакций полимеризации на реакции цепной полимеризации и реакции ступенчатой полимеризации.
Различие между реакциями цепной полимеризации и ступенчатой полимеризации несколько более запутано, чем между реакциями полимеризации и поликонденсации. Это различие заключается примерно в следующем:
При цепной полимеризации мономеры становятся частью молекулы полимера постепенно, одна за другой, так что в данный момент времени к молекуле полимера присоединяется только одна молекула мономера.
Пример
картины цепной полимеризации, анионной
полимеризации стирола с образованием
полистирола: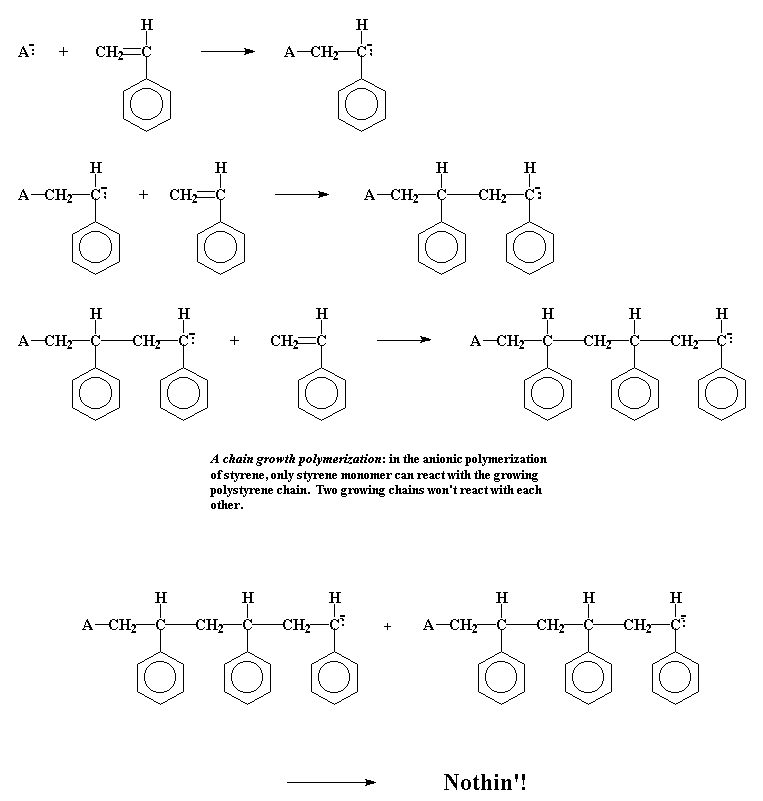
Но при ступенчатой полимеризации все происходит несколько более сложным образом. Посмотрим на ступенчатую полимеризацию двух мономеров, хлорангидрида терефталевой кислоты и этиленгликоля, с образованием полиэфира под названием полиэтилентерефталат. Первое, что происходит при этой реакции, это взаимодействие двух мономеров с образованием димеров. Звучит достаточно просто.
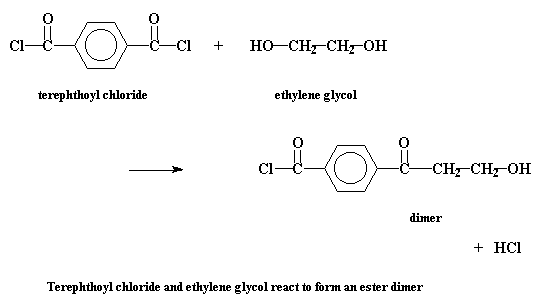
Будь эта система такой, в которой происходит цепная полимеризация, на этой стадии реакции могло бы произойти только одно: третья молекула мономера присоединилась бы к димеру, чтобы образовать тример, затем четвертая - чтобы образовать тетрамер и так далее. Но в свободной стране ступенчатой полимеризации с этим димером может произойти много разных процессов. Конечно же, он может прореагировать с одним из мономеров, чтобы образовать таким образом тример:
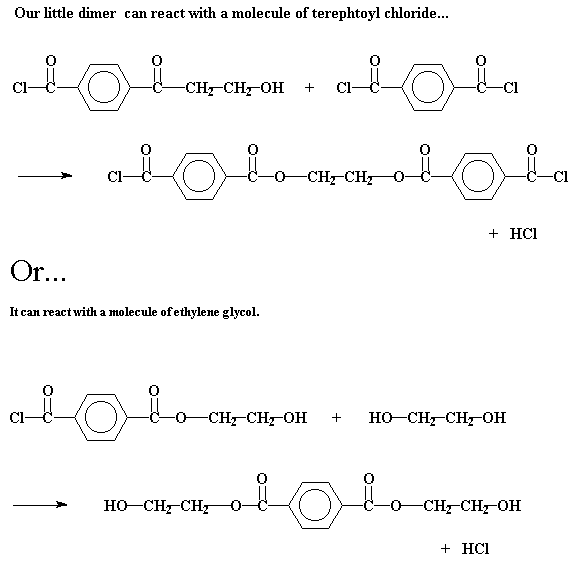
Но он может также поступить иначе. Он может провзаимодействовать с другим димером, чтобы образовать тетрамер:
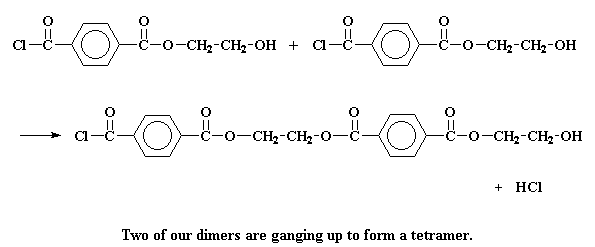
Или он может поступить совсем сумасшедшим образом и вступить в реакцию с тримером с образованием пентамера.
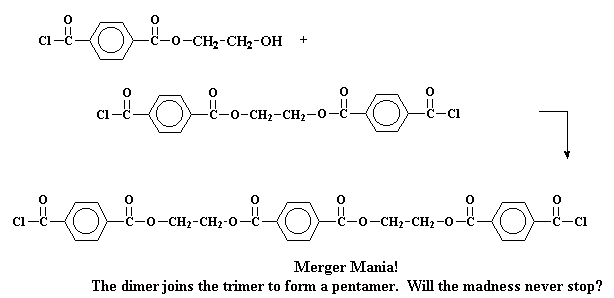
Делая процесс все более и более запутанным, эти тетрамеры и пентамеры могут провзаимодействовать между собой и образовать олигомеры еще больших размеров. И, таким образом, они продолжают расти и расти, пока олигомеры не становятся достаточно большими, чтобы иметь уже право называться полимерами.
Вы просто подумайте о том, как банки постоянно сливаются с другими банками и становятся при этом все крупнее и крупнее. Это поможет вам лучше представить процесс ступенчатой полимеризации.
Вывод: Основное отличие заключается в том, что при ступенчатой полимеризации растущие молекулярные цепи могут взаимодействовать между собой, образуя еще более длинные цепи. И это справедливо для цепей любой длины. Мономер или димер может вступить в реакцию точно также, как и цепочка, состоящая из сотен мономерных звеньев. Но при цепной полимеризации только мономеры могут взаимодействовать с растущей цепочкой макромолекулы. Сами растущие цепочки не могут взаимодействовать между собой так, как это они могут делать при ступенчатой полимеризации.
Непримиримые противоречия:
Ступенчатая полимеризация для получения полиэфира привела к образованию побочного продукта, газообразного хлористого водорода HCl. Вследствие этого, конечно же, эту реакцию ступенчатой полимеризации можно отнести к типу реакции поликонденсации.
Вы также могли заметить, что наша реакция цепной полимеризации не привела к образованию побочного продукта. Да, конечно, эта ступенчатая реакция полимеризации является также реакцией полимеризации (а не поликонденсации), то есть реакцией присоединения.
Довольно легко из этого сделать вывод о том, что ступенчатая полимеризация и поликонденсация - это одно и то же, а также о том, что полимеризация присоединения и цепная полимеризация - тоже ничем друг от друга не отличаются. Однако это будет как раз неверно. Ведь существуют реакции полимеризации присоеднинения, которые являются ступенчатыми реакциями полимеризации. Одним из примеров может служить полимеризация, в результате которой образуются полиуретаны. Кроме того, существуют также реакции поликонденсации, которые являются цепными реакциями полимеризации. Попытки как-то примирить между собой систему классификации на реакции цепной и ступенчатой полимеризации и систему классификации на реакции полимеризации и поликонденсации - это пустая трата времени. У каждой из этих систем свои критерии, и различия, характерные для одной системы, не всегда будут тождественны различиям, характерным для другой системы классификации.
Поэтому и не думайте связать эти две системы. Просто надо знать, что реакции образования полимеров могут быть либо цепными, либо ступенчатыми, с одной стороны, а с другой стороны, они могут быть либо реакциями полимеризации, либо поликонденсации.
№3. Побочные реакции, осложняющие поликонденсацию.
В общем виде схема основной реакции П.-роста цепи-м. б. представлена след, образом.:
![]()
(n и m-любое целое число, включая единицу, X и Y-исходные функц. группы, А-низкомол. продукт поликонденсации.). При этом взаимодействии мономеров друг с другом или с образовавшимися олигомерами и последних между собой подчиняется практически одним и тем же законам.
Поскольку при поликонденсации мономеры исчерпываются уже при невысоких степенях завершенности реакции, рост цепи высокомолекулярного полимера происходит преимущественно в результате многократного соединения между собой олигомерных или полимерных молекул по концевым функц. группам (принцип многократного удвоения), при этом число молекул в системе уменьшается (в этом ступенчатый характер поликонденсации.). Уменьшается в ходе поликонденсации и количество исходных функц. групп-реакционных (активных) центров, хотя в ряде случаев образующиеся при поликонденсации связи реагируют как между собой, так и с исходными реакц. центрами. Росту полимерной цепи при равновесной поликонденсации сопутствует обратная реакция полимера с выделяющимся низкомол. продуктом, что ограничивает мол. массу полимера.
При поликонденсации функц. группы мономеров, олигомеров и полимерных цепей расходуются не только на рост цепи, но и на побочные реакции (реакции с примесями или со специально введенными в процесс веществами, декарбоксилирование карбоновых кислот и др.), что также лимитирует мол. массу образующегося полимера. При поликонденсации возможны также циклизация и обменные реакции. Циклизация м. б. внутримолекулярной, когда кольца образуются при р-ции функц. групп одной молекулы, или межмолекулярной при взаимод. двух или более молекул одинаковой или разл. природы, напр.:
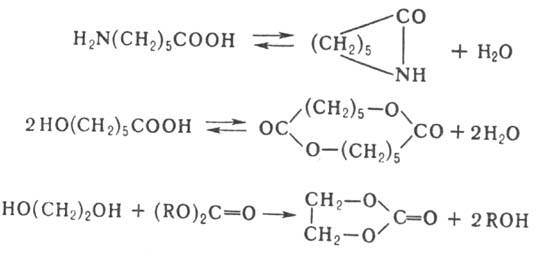
Возможность циклизации определяется соотношением двух факторов:
1) снижения вероятности образования цикла по мере увеличения его размера (увеличение энтропии активации);
2) напряженности цикла, к-рая уменьшается при увеличении его размера вплоть до 6-членного, затем возрастает при изменении числа членов в цикле от 6 до 9-11, а затем вновь снижается при переходе к еще большим циклам. В результате совместного действия обоих этих факторов при получении методом поликонденсации различных полимеров возможно образование больших циклов (20-40-членных). Циклообразованию способствует проведение реакции в сильно разб. р-рах (см. Краун-эфиры ).
Обменные реакции особенно эффективны при повышенных температурах поликонденсации. Их делят на два основных типа:
1) реакции обмена образовавшихся при поликонденсации групп (сложноэфирной, амидной или др.) и даже некоторых циклов (напр., имидного) с функц. группами мономеров или примесей (напр., алкоголиз, ацидолиз, аминолиз);
2) реакции межцепного обмена между образовавшимися при поликонденсации одно- или разнотипными группами (напр., эфиролиз, амидолиз). Эффективность обменных реакций зависит от соотношения скоростей основной и побочных реакций. Обменные реакции могут существенно влиять на мол. массу и MMP поликонденсац. полимера, микроструктуру сополимера. В ряде случаев обменные реакции положены в основу получения поликонденсац. гомо- и сополимеров, напр, синтез поли-этилентерефталата переэтерификацией диметилтерефталата этиленгликолем.
Ограничение роста полимерной цепи м. б. обусловлено и чисто физическими причинами, напр. преждевременным выпадением полимера из реакционной среды в осадок при поликонденсации в растворе (особенно если это сопровождается его кристаллизацией), однако если выпадающий из раствора полимер набухает в реакц. среде, рост цепи часто не прекращается.
№4. Механизмы реакций поликонденсации в кислой и щелочной среде фенола и формальдегида.
Фенолформальдегидные смолы - продукты поликонденсации фенола с формальдегидом. Реакция проводится в присутствии кислых (соляная, серная, щавелевая и другие кислоты) или щелочных катализаторов (аммиак, гидроксид натрия, гидроксид бария). При избытке фенола и кислом катализаторе образуется линейный полимер – новолак, цепь которого содержит приблизительно 10 фенольных остатков, соединенных между собой метиленовыми мостиками:
![]()
Новолаки – термопластичные полимеры, которые сами по себе не способны переходить в неплавкое и нерастворимое состояние. Но они могут превращаться в трехмерный полимер при нагревании их с дополнительной порцией формальдегида в щелочной среде.
При использовании щелочных катализаторов и избытка альдегида в начальной стадии поликонденсации получаются линейные цепи резола, которые при дополнительном нагревании "сшиваются" между собой за счет групп CH2OH, находящихся в пара-положении фенольного кольца, с образованием трехмерного полимера – резита:
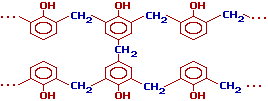
Таким образом, резолы являются термореактивными полимерами.
Фенолоформальдегидные полимеры применяются в виде прессовочных композиций с различными наполнителями, а также в производстве лаков и клея.
Свойства: Отвержденные смолы характеризуются высокими тепло-, водо- и кислостойкостью, а в сочетании с наполнителями и высокой механической прочностью.
Применение: Из фенолформальдегидного полимера, добавляя различные наполнители, получают фенолформальдегидные пластмассы, т. н. фенопласты. Их применение очень широко. Это: шарикоподшипники, шестерни и тормозные накладки для машин; хороший электроизоляционный материал в радио- и электротехнике. Изготовляют детали больших размеров, телефонные аппараты, электрические контактные платы. Для склеивания пенополистирольных плит, применяемых для изготовления моделей в литейном производстве.
Получение фенолформальдегидной смолы:
1. В пробирку помещают 10 капель жидкого фенола и 8 капель 40% формальдегида. Смесь нагревают на водяной бане до растворения фенола. Через 3 минуты в пробирку добавляют 5 капель концентрированной соляной кислоты и помещают ее в стакан с холодной водой. После образования в сосуде двух четких фаз следует слить воду и вылить полимер из пробирки. В течение нескольких минут образовавшаяся новолачная смола затвердевает.
2. В небольшую колбочку помещают 15 г фенола и 25 мл концентрированного раствора формалина и нагревают (под тягой) на горелке, периодически встряхивая содержимое колбы. Добавляют 1-2 мл соляной кислоты и продолжают нагревание. Вначале реакция идет бурно и смесь в колбе становится однородной. Через некоторое время (около 10 минут) на дне колбы образуется смолистый осадок. Верхний слой жидкости сливают и быстро извлекают смолу, которая на воздухе густеет и постепенно затвердевает.
Фенолформальдегидные смолы [-C6H3(OH)-CH2-]n – продукты поликонденсации фенола C6H5OH с формальдегидом CH2=O.

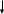 .
На гомополиконденсацию и
гетерополиконденсацию:
.
На гомополиконденсацию и
гетерополиконденсацию: поликонденсации:
поликонденсации: