
- •Переваривание и всасывание липидов………………………………..9
- •Введение
- •Перечень основных вопросов темы
- •Основные сведения по биохимии обмена липидов
- •Переваривание и всасывание липидов
- •3.Нарушение метаболизма кетоновых тел
- •4. Гиповитаминозы
- •Контрольные вопросы по теме «Обмен липидов» (5 часов)
- •1Занятие
- •2 Занятие
- •3 Занятие
Переваривание и всасывание липидов
Переваривание и всасывание триацилглицеринов. Триацилглицерины (ТАГ), являются основной фракцией липидов пищи, покрывают от 25 до 35 % суточных энерготрат. Триацилглицерины поступают в организм большей частью с продуктами животного происхождения.
Переваривание триацилглицеринов пищи заключается в их эмульгировании с последующим гидролитическим расщеплением и солюбилизацией продуктов гидролиза.
Наиболее сильным эмульгирующим действием обладают желчные кислоты, поступающие в двенадцатиперстную кишку с желчью. В двенадцатиперстную кишку вместе с пищевой массой переносится некоторое количество желудочного сока, содержащего соляную кислоту, которая в двенадцатиперстной кишке нейтрализуется в основном бикарбонатами, содержащимися в панкреатическом соке и желчи. Образующиеся при разложении бикарбонатов пузырьки углекислого газа разрыхляют пищевую кашицу и способствуют более полному перемешиванию ее с пищеварительными соками. Одновременно начинается эмульгирование жира (ТАГ). Соли желчных кислот адсорбируются в присутствии небольших количеств свободных жирных кислот (ЖК) и моноацилглицеринов (МАГ) на поверхности капелек жира в виде тончайшей пленки, препятствующей слиянию этих капелек. Кроме того, соли желчных кислот, уменьшая поверхностное натяжение на поверхности раздела двух фаз — воды и жира, способствуют расчленению больших капелек жира на меньшие. Создаются условия для образования тонкой и устойчивой жировой эмульсии с размером частиц 0,5 мкм и меньше. Дополнительными эмульгаторами являются свободные жирные кислоты, моноацилглицерины и фосфолипиды. В результате эмульгирования резко увеличивается поверхность жиров, что облегчает взаимодействие их с липазой, т. е. ускоряется ферментативный гидролиз. (рис.3).
Вследствие низкой липолитической активности желудочного сока, а также отсутствия в рационе значительных количеств эмульгированных жиров переваривание триацилглицеринов в желудке взрослого человека не имеет практического значения.
Основная масса пищевых ТАГ подвергается расщеплению в верхних отделах тонкой кишки при действии липазы панкреатического сока. Она расщепляет ТАГ, находящиеся в эмульгированном состоянии. Фермент катализирует гидролиз эфирных связей в α-положениях, в результате чего образуется 2-моноацилглицерин и освобождаются две ЖК. (рис.4) Примерно 1/3 образовавшихся моноацилглиринов изомеризуются в 1- или 2-моноацилглицерины, которые гидролизуются поджелудочной липазой. Остальные моноацилглицерины и свободные жирные кислоты переходят в мицеллярную фазу, т.е. солюбилизируются (растворяются), что является необходимой предпосылкой последующего всасывания липидов.
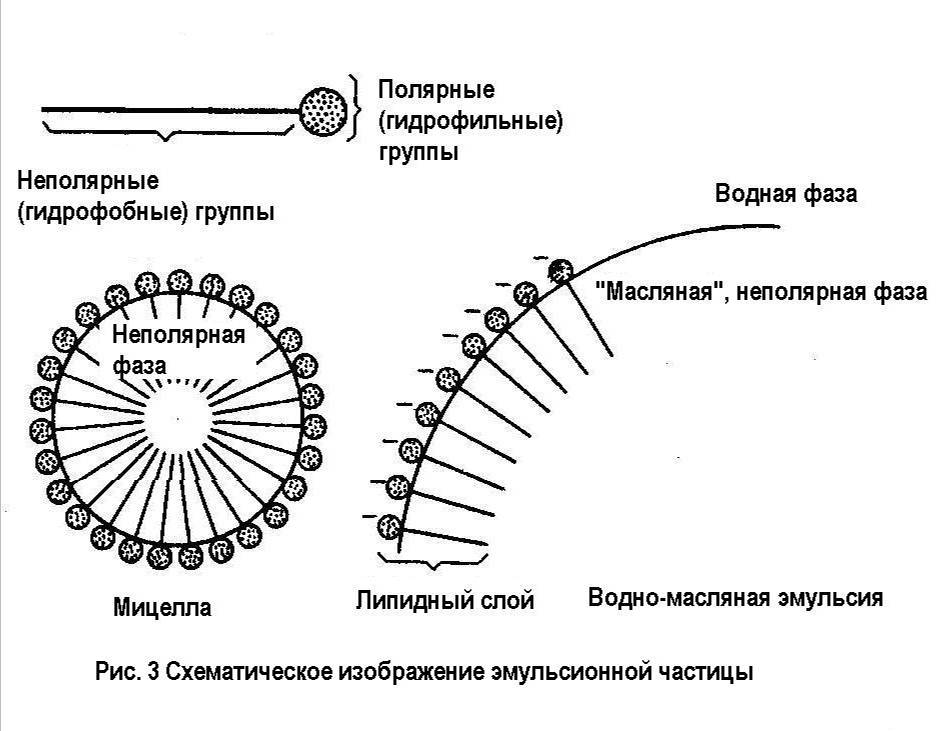
Рис.3 Схематическое изображение эмульсионной частицы
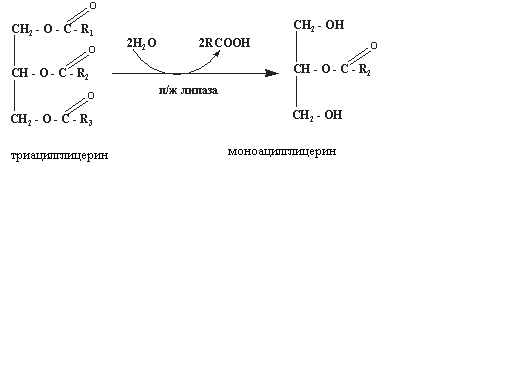
Рис.4 Схема гидролиза триацилглицеринов
Панкреатическая липаза, поступает в верхний отдел тонкой кишки в виде неактивной пролипазы. Превращение пролипазы в активную липазу происходит при участии желчных кислот и еще одного белка панкреатического сока — колипазы. Колипаза секретируется также в виде проколипазы. Ее превращение в активную колипазу происходит под действием трипсина поджелудочного сока и сопровождается выделением пентапептида энтеростатина. Энтеростатин рассматривается как своеобразный «кишечный гормон», вызывающий чувство сытости при приеме и переваривании жирной пищи.
У младенцев в отличие от взрослых нейтральный жир подвергается перевариванию в желудке благодаря действию следующих факторов: с желудочным соком поступает желудочная липаза, рН желудочного сока детей соответствует рН-оптимуму липазы, в молоке содержится эмульгированный жир.
Переваривание глицерофосфолипидов. Подавляющая часть фосфолипидов содержимого тонкой кишки приходится на фосфатидилхолин (лецитин), основная масса которого поступает в кишечник с желчью (11-12 г/сут) и меньшая (1-2 г/сут) — с пищей.
Переваривание глицерофосфолипидов осуществляется в тонком кишечнике в две фазы : вначале происходит гидролиз, а затем солюбилизация его продуктов Основными энзимами, участвующим в переваривании глицерофосфолипидов, являются панкреатические фосфолипаза А2 и лизофосфолипаза. Фосфолипаза А2 гидролизует ацилэфирную связь в глицерофосфолипидах во втором положении с образованием жирной кислоты и 1-лизофосфоглицерида. Лизофосфолипиды – эффективные эмульгаторы жира. Жирная кислота в первом положении лизофосфолипидов отщепляется под действием панкреатической лизофосфолипазы, а образовавшейся глицеролфосфорноосновный скелет хорошо растворяется в воде и всасывается из кишечника в кровь (рис.5). Сфингомиелины всасываются без предварительного гидролиза в интактном виде.
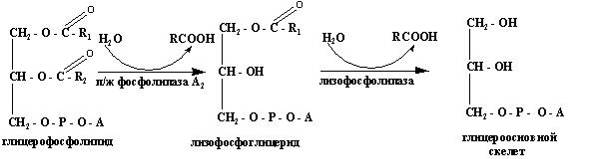
Рис. 5 Схема переваривания фосфолипидов
Переваривание эфиров холестерола (ЭХС) заключается в их солюбилизации и последующим гидролитическом расщеплении. Гидролиз ЭХЛ происходит в тонком кишечнике под действием поджелудочной холестеролэстеразы с образованием свободного холестерола и жирной кислоты. (рис.6)

Рис.6 Схема переваривания эфиров холестерола
Липиды крови
Общие липиды 4,0 - 8,0 гл
Холестерол (ХС) 3,64 - 6,.76 ммольл
Фосфолипиды 2,52 - 2,91 ммольл
Триацилглицерины (ТАГ) 0,44 - 1,82 ммольл
Свободные жирные кислоты 640 - 880 мкмольл
- липопротеины 35,0 - 55,0 ус. ед.
Жирные кислоты - строение, биологическая роль
Строение. Свободные жирные кислоты содержатся в различных тканях животного организма в значительном количестве. Основная масса жирных кислот в качестве важнейшего структурного элемента входит в состав различных классов ацилсодержащих липидов (фосфоглицеридов, сфинголипидов, ацилглицеринов и эфиров холестерола).
Молекулы жирных кислот – это алифатические карбоновые кислоты, представленные гидрофобной углеводородной цепью с концевой гидрофильной карбоксильной группой. Биполярность придает жирным кислотам и, особенно, мылам поверхностно-активные свойства.
Гетерогенность жирных кислот обусловлена различием длины цепи и числом двойных связей. Почти все жирные кислоты животного организма представляют собой неразветвленные цепи с четным числом углеродных атомов – от 14 до 24, что обусловлено особенностями их синтеза. Чаще всего встречаются жирные кислоты с 16 или 18 атомами углерода.
Число двойных связей в жирных кислотах колеблется от 0 до 6. Почти во всех природных ненасыщенных жирных кислотах двойные связи имеют цис-конфигурацию. Ненасыщенные жирные кислоты, в свою очередь, делятся на моноеновые, т.е. содержащие одну двойную связь, и полиеновые – содержащие несколько двойных связей (диеновые, триеновые, тетраеновые и т.д.
Жирные кислоты, имеющие важное физиологическое значение приведены в таблице 1
Таблица 1
Характеристика основных жирных кислот
Кислота |
Число атомов углерода, число и положение двойных связей |
Систематическое название |
Источники |
Пальмитиновая
|
160 |
Гексадекановая |
Встречаются во всех животных и растительных жирах |
Стеариновая |
180 |
Октадекановая |
|
Арахидиновая |
200 |
Эйкозановая |
Арахисовое масло |
Пальмитолеиновая |
161; 9 |
Цис-9-гексадеценовая |
Почти во всех жирах |
Олеиновая |
181; 9 |
Цис-9-октадеценовая |
|
Линолевая |
182; 9, 12 |
Цис-9,12-октадекадиеновая |
Почти во всех жирах растительного происхож-дения |
Линоленовая |
183; 9, 12, 15 |
Цис-9,12,15-октадекатриеновая |
Почти во всех жирах растительного происхож-дения |
Арахидоновая |
204; 5, 8, 11, 14 |
Цис-5,8,11,14-эйкозатетраеновая |
Почти во всех жирах растительного происхож-дения |
Эйкозапентаеновая |
205; 5, 8, 11, 14, 17 |
Цис-5,8,11,14,17-эйкозапентаеновая |
Рыбий жир, фосфолипиды мозга |
Позицию двойной связи обозначают знаком ∆, после которого указывают номер атома углерода, ближайшего к карбоксилу, у которого находится двойная связь. Например 18 2 ∆9,12 означает, что жирная кислота содержит 18 атомов углерода и две двойные связи у 9 и 12 атомов углерода, считая от углеродного атома карбоксильной группы. Позиция двойной связи может быть указана и другим способом – по расположению первой двойной связи, считая от метильного -атома углерода жирной кислоты. Например, арахидоновая кислота (В6) может быть обозначена как С20 : 4 ∆ 4,8,11,14 или С20 : 4 6. По положению первой двойной связи от метильного углерода полиеновые жирные кислоты делятся на семейства -3 и -6 (рис.7).
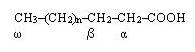
Рис.7 Строение жирной кислоты
Биологическая роль. Жирные кислоты в организме выполняют несколько функций. Прежде всего это энергетическая функция, так как именно при их окислении выделяется основная масса энергии, заключенная в химических связях большей части липидов. Так, при окислении до конечных продуктов 1 моля стеариновой кислоты (1М – 284 г) выделяется 2632 ккал энергии. Энергетическая ценность жирных кислот реализуется в процессе -окисления и последующего окисления образующегося ацетил-КоА в ЦТК.
Жирные кислоты выполняют также структурную функцию, поскольку они входят в состав разнообразных более сложных по химическому строению липидов таких как триацилглицерины, глицерофосфолипиды, эфиры холестерола и сфинголипиды. В биологических мембранах жирнокислотные остатки фосфоглицеринов и сфинголипидов формируют непрерывную углеводородную фазу липидного бислоя. Агрегатное состояние мембран определяется соотношением насыщенных и ненасыщенных жирнокислотных остатков, входящих в ее состав липидов. Дефицит незаменимых полиненасыщенных жирных кислот – линолевой, линоленовой и арахидоновой приводит к изменению жирнокислотного состава мембранных липидов, сопровождающемуся нарушением функции биомембран.
Кроме того, жирные кислоты выполняют в организме метаболическую функцию, поскольку остатки арахидоновой и линоленовой кислот в составе фосфатидилхолинов и особенно фосфатидилэтаноламинов является основными субстратами перекисного окисления. Ряд полиеновых С20-жирных кислот в составе фосфоглицеринов, в частности арахидоновая кислота может быть использована для синтеза биорегуляторов: простагландинов, простациклинов, тромбоксанов и лейкотриенов.
Особо следует отметить, что ряд полиненасыщенных высших жирных кислот относятся к незаменимым компонентам пищи, поскольку они не синтезируются в организме. Обычно к эссенциальным высшим жирным кислотам относят линолевую (А6 здесь и далее координаты на метаболической карте «Обмен липидов»), линоленовую (А4) и арахидоновую (В6) кислоты (витамин F).
Ацилглицерины: строение, биороль, синтез, роль гормонов в мобилизации из жировой ткани
Строение. Ацилглицерины или нейтральные жиры являются сложными эфирами, образованными трехатомным спиртом глицеролом и жирными кислотами. (рис.8)
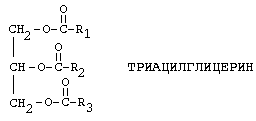
Рис.8 Строение триацилглицерина
Гетерогенность ацилглицеринов определяется числом, природой и расположением жирнокислотных остатков. В зависимости от количества жирнокислотных остатков, входящих в структуру ацилглицеринов различают триацилглицерины (Б4), диацилглицерины (Б3) и моноацилглицерины (Б1). В животном организме ацилглицерины представлены в основном триацилглицеринами. Почти все триацилглицерины являются смешанными, т.е. в их состав входят различные жирнокислотные остатки. Жирнокислотный состав триацилглицеринов организма в гораздо большей степени, чем состав других ацилсодержащих липидов зависит от характера питания, изменений температуры среды и других условий.
Биологическая роль. Триацилглицерины выполняют в организме энергетическую, резервную, терморегуляторную и защитную функции. Энергетическая функция. Триацилглицерины служат важнейшим источ-ником энергии в организме. С энергетической точки зрения наибольшее значение имеют жирнокислотные компоненты. Энергетическая ценность триацилглицеринов составляет более 9 ккалг, что заметно превышает таковую углеводов и белков.
Резервная функция. В форме триацилглицеринов депонируются запасы метаболического топлива. У человека на долю триацилглицеринов приходится в среднем 10-20% массы тела. Этого количества вполне достаточно для обеспечения энергетических потребностей организма на протяжении 6 недель голодания. Запасные жиры могут использоваться в качестве источника энергии не только в условиях продолжительного голодания , но также для поддержания мышечной активности. В различных органах и тканях триацилглицерины локализуются в цитоплазме клеток в виде изолированных капелек. Наиболее высокое содержание триацилглицеринов в жировой ткани, где на их долю приходится около 80% ее массы.
Терморегуляторная функция. Триацилглицерины жировой ткани выполняют функцию теплоизолирующего слоя, так как жир плохо проводит тепло. Кроме того, при охлаждении организма происходит активирование термогенеза за счет ускорения окисления триацилглицеринов.
Защитная функция. Триацилглицерины под кожной жировой клетчатки амортизируют внешние механические воздействия на внутренние органы.
Синтез триацилглицеринов может осуществляться -глицерофосфатным и моноглицеридным путями. Независимо от пути, в ходе синтеза триацилглицеринов используются активированные жирные кислоты. Активирование жирной кислоты – это образование эфиров с КоА (ацил-КоА) осуществляется ацил-КоА-синтетазой (А3). Реакция сопровождается расходованием АТФ.
-глицерофосфатный путь (рис.9). Исходным субстратом этого пути является глицерол-3-фосфат (Б2). Глицерол-3-фосфат образуется двумя путями.
1.При фосфорилировании глицерина глицеролкиназой (А1) за счет фосфатной группы АТФ. Этот путь имеет место в печени. Глицерол поступает в печень из крови как продукт гидролиза триацилглицеринов жировой ткани, а также хиломикронов и ЛПОНП липопротеинлипазой.
2.При восстановлении дигидроацетонфосфата (Б2) (продукт гликолиза) НАД-зависимой глицерол-3-фосфатдегидрогеназой. Этот путь имеет место в жировой ткани, которая не имеет активной глицеролкиназы.
В ходе синтеза глицерол-3-фосфат дважды ацилируясь в реакциях с ацил-КоА через стадию 1-лизофосфатидата превращается в фосфатидат (А3). Последний гидролизуется специфической фосфатазой до диацилглицерина (Б3), который затем взаимодействует с ацил-КоА с образованием триацилглицерина (Б4).
Моноглицеридный путь. В тонком кишечнике в синтезе триацилглицеринов в качестве исходного субстрата используется моноацилглицерин (Б1), являющийся продуктом неполного гидролиза жиров в кишечнике. В ходе моноглицеридного пути моноацилглицерины двукратно ацилируясь в реакциях с ацил-КоА, через стадию диацилглицерина (Б3) превращаются в триацилглицерин (Б4).
Мобилизация триацилглицеринов происходит в цитоплазме путем последовательного ступенчатого гидролитического отщепления жирных кислот. Этот процесс является необходимым этапом использования жиров в качестве энергетического материала.
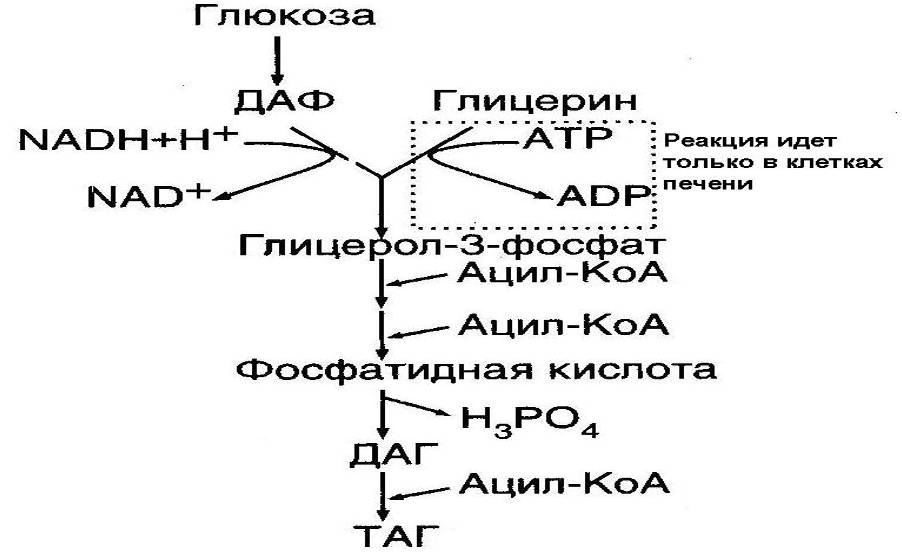
Рис.9 Схема синтеза триацилглицеринов в печени и жировой ткани (ДАФ – дигидроацетонфосфат)
Гидролиз триацилглицеринов инициирует триацилглицерол-липаза. Этот фермент является гормончувствительным и активируется некоторыми гормонами. (рис.10). Под его влиянием триацилглицерин расщепляется на диацилглицерин и жирную кислоту. Дальнейший процесс гидролиза катализирует диацилглицероллипаза, активность
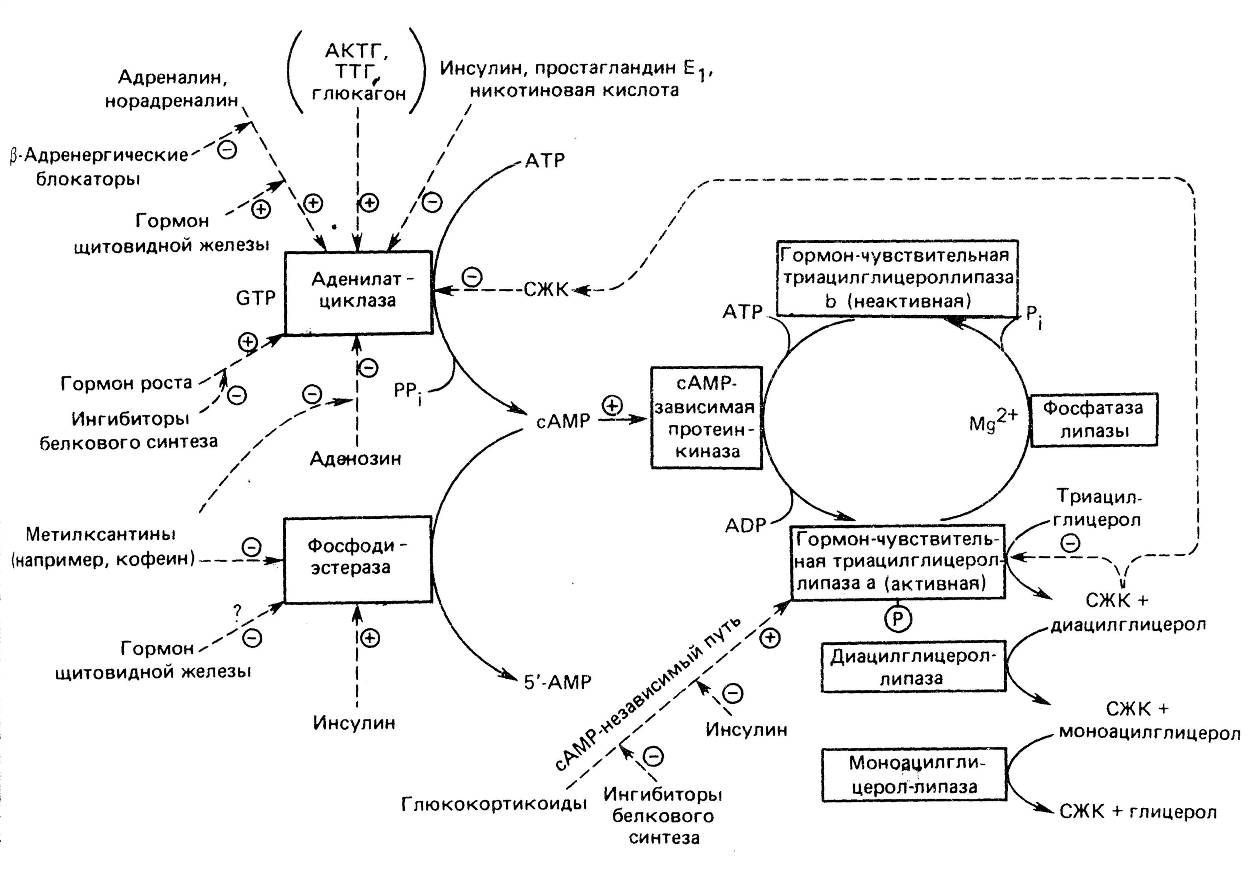
Рис.10. Схема мобилизации триацилглицеринов из жирового депо
которой зависит от количества субстрата, т.е. по сути от активности триацилглицероллипазы. Образующийся моноацилглицерин расщеп-ляется моноацилглицероллипазой с образованием глицерола и жирной кислоты. Жирные кислоты в комплексе с альбуминами плазмы доставляются в ткани, где используются как энергетические субстраты. Глицерол используется печенью в реакциях глюконеогенеза.
ФОСФОЛИПИДЫ
Фосфолипиды – это гетерогенный класс липидов, содержащий в качестве структурного элемента остаток фосфорной кислоты. Большая часть фосфолипидов представлена глицерофосфолипидами. Фосфо-липиды входят в состав всех клеток. Особенно богат фосфолипидами головной мозг – около 6% от сырой массы, в плазме содержится около 0,2%.
Глицерофосфолипиды:строение,синтез, распад
Строение.Глицерофосфолипиды (ГФЛ) являются производными глицеро-3-фосфата (Б2), гидроксильные группы которого замещены при С1 и С2 остатками длинноцепочных жирных кислот, а остаток фосфорной кислоты этерифицирован гидроксильной группой спиртового компонента (рис.11 )
У большинства глицерофосфолипидов во
втором положении, как правило, находятся
остатки ненасыщенных жирных кислот,
тогда как первое положение занимают
остатки насыщенных жирных кислот.
большинства глицерофосфолипидов во
втором положении, как правило, находятся
остатки ненасыщенных жирных кислот,
тогда как первое положение занимают
остатки насыщенных жирных кислот.
Рис.11 строение глицерофосфолипдов
Гетерогенность глицерофосфолипидов обусловлена прежде всего различиями спиртового компонента. В составе глицерофосфолипидов остаток фосфорной кислоты может быть этерифицирован холином (В2), этаноламином (В3), серином (Г3), инозитом (Г4), глицеролом (Б1) и его производными. В соответствии с характером спиртового компонента глицерофосфолипидам присваивается соответствующее название. Основными из них являются фосфатидилхолины (Е3), фосфатидилсерины (Е4), фосфатидилэтаноламины (Е3), фосфатидилинозитиды (Д4) и дифосфатидилглицерины (Б4).
Все фосфолипиды относятся к числу амфипатических или полярных липидов. Длинные углеводородные хвосты, характеризующиеся низким сродством к воде (гидрофобностью) образуют объемную липофильную область. Гидрофильная полярная группа представлена остатком фосфорной кислоты, этерифицированной спиртом. Наличие у фосфолипидов двух частей – сильно полярной и неполярной имеет отношение к их способности образовывать мембраны. Практически все фосфолипиды клетки сосредоточены в ее мембранах.
Биороль. Глицерофосфолипиды выполняют в организме человека структурную, транспортную метаболическую и защитную функции
1Структурная функция. Глицерофосфолипиды наряду с другими полярными липидами формируют бимолекулярный липидный слой, составляющий основу биомембран. В бимолекулярном липидном слое углеводородные цепи жирных кислот обращены внутрь (хвост к хвосту), образуя непрерывную углеводородную фазу, а полярные головы молекул обращены к водной фазе.
2. Транспортная функция. Глицерофосфолипиды принимают участие в формировании наружного слоя липопротеиновых частиц и таким образом выполняют функцию транспорта нейтральных липидов.
3.Метаболическая функция. Ненасыщенные жирнокислотные остатки, в частности арахидоновая кислота, мембранных ГФЛ, используются как субстрат в синтезе простагландинов и лейкотриенов. Ненасыщенные жирнокислотные остатки мембранных ГФЛ являются также субстратом перекисного окисления липидов.
4. Защитная функция. Глицерофосфолипиды являются важнейшим компонентом сурфактанта, покрывающего внутреннюю поверхность альвеол легких и предупреждающего их слипание.
Синтез ГФЛ осуществляется в различных органах и тканях, особенно интенсивно в печени, головном мозге и тонком кишечнике. Все типы глицерофосфолипидов синтезируются на мембранах эндоплазматического ретикулума.
Ключевое положение в синтезе большей части глицерофосфолипидов занимают фосфатидные кислоты (А3), т.е. до образования фосфатидных кислот синтез триацилглицеринов и глицерофосфолипидов совпадает. В дальнейшем пути синтеза различных типов ГФЛ расходятся (рис.12).
Синтез дифосфатидилглицеринов (Б4) и фосфатидилинозитидов (Д4) связан с превращением фосфатидных кислот в реакции с ЦТФ в липонуклеотиды, а именно в ЦДФ-диглицерины (Б3). Дифосфатидилглицерины синтезируются путем конденсации двух молекул ЦДФ-диглицерина с глицерол-3-фосфатом. Фосфатидилинозитиды образуются в результате присоединения к ЦДФ-диглицерину инозита.
Использованию фосфатидных кислот для синтеза фосфатидилхолинов (Е3) и фосфатидилэтаноламинов (Е3) предшествует их дефосфорилирование до диацилглицеринов (Б3) (рис.10). Фосфатидилхолины и фосфатидилэтаноамины синтезируются путем присоединения к диацилглицерину активной формы соответственно ЦДФ-холина (Д3) и ЦДФ-этаноламина (Д3). Образование фосфатидилхолина происходит также в результате трехкратного метилирования этаноламина в составе фосфатидилэтаноламина (донором метильных групп в данном случае служит S-аденозилметионин Д3) или в реакции замещения этаноламина на холин (Е3). Фосфатидилсерин (Е4) образуется в результате замещения этаноламина серином (Е4). Фосфатидилсерин в ходе реакции декарбоксилирования превращается в фосфатидилэтаноламин.

Рис.12 Схема синтеза глицерофосфолипидов
Распад глицерофосфолипидов осуществляется в различных тканях двумя альтернативными путями. В ходе первого пути гидролитический распад глицерофосфолипидов начинается с отщепления жирных кислот под влиянием фосфолипаз А1 или А2 (Д2). Образующиеся при этом 1 (или 2)-лизофосфоглицерины (Г2) теряют оставшуюся жирную кислоту независимо от ее положения под действием лизофосфолипазы. Освободившийся глицерофосфорноспиртовый скелет расщепляется на глицерол-3-фосфат и соответствующее спиртовое основание.
Распад глицерофосфолипидов по второму пути начинается с гидролиза эфирной связи между диацилглицеринами и замещенной фосфорной кислотой под действием фосфолипазы С с образованием диацилглицерина и фосфорилированной формы спиртового основания. Диацилглицерины подвергаются дальнейшему распаду на жирные кислоты и глицерин.
Сфинголипиды: строение, биороль
Сфингомиелины (Д6) являются производными ненасыщенного аминоспирта сфингозина (Е6). В составе сфингомиелинов (Д6) жирнокислотный остаток связан с остатком сфингозина амидной связью, а первичная гидроксильная группа замещена остатком фосфорилхолина (Рис.13).
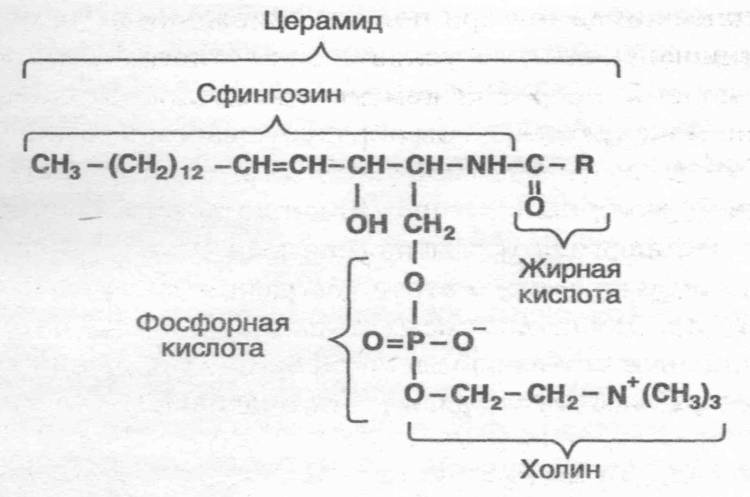
Рис.13 Строение сфингомиелина
На долю сфингомиелинов в различных тканях приходится от 5 до 25% всех мембранных фосфолипидов. Особенно велико содержание сфингомиелинов в нервной ткани, где они являются основным структурным элементом миелиновых оболочек.
Сфингомиелины относятся к числу амфипатических липидов. По своей конформации сфингомиелины весьма сходны с фосфоглицеринами: их молекулы содержат полярную голову, образованную фосфорилхолином, и два неполярных хвоста, одним из которых служит длинная алифатическая цепь сфингозина, а другим — остаток длинноцепочной жирной кислоты. При физиологических значениях рН фосфорилхолиновая голова представляет собой биполярный цвиттерион с суммарным зарядом, равным нулю (отрицательный заряд обусловлен фосфатной группой, положительный — азотом остатка холина).
Функция сфингомиелинов сводится к тому, что они являются структурным элементом большинства биологических мембран. Наиболее богаты сфингомиелинами плазматические мембраны, а также мембраны комплекса Гольджи, лизосом и секреторных гранул. Указанные мембраны характеризуются также высоким содержанием холестерола. В ядерных мембранах и эндоплазматической сети сфингомиелины присутствуют в незначительных количествах, а в мембранах митохондрий они практически отсутствуют.
В плазме крови сфингомиелины являются наиболее представительным в количественном отношении типом фосфолипидов после фосфатидилхолинов. Особенно велико содержание сфингомиелинов в липопротеидах низкой плотности — ЛПНП.
Гликосфинголипиды – гликолипиды, в состав которых входят церамид и углеводный компонент. В зависимости от его строения различают цереброзиды, содержащие в качестве углеводной группировки остаток галактозы или глюкозы. У ганглиозидов углеводный компонент представлен гетерополисахаридом, одним из звеньев которого является сиаловая кислота. В больших количествах гликосфинголипиды представлены в мозге. Они локализованы в плазматических мембранах клеток таким образом, что углеводная часть молекулы располагается на поверхности клеток т.е. входят в состав гликокаликса. Гликокаликс – это обогащенная углеводами периферическая зона на поверхности большинства эукариотических клеток, участвующая в межклеточных взаимодействиях. Ганглиозиды эпителия кишечника являются рецепторами холерного токсина.
Нарушения обмена липидов
1. Нарушение переваривания и всасывания липидов
2.Жировая дегенерация печени.
.
Гиперхолестеролемии.
Нарушение метаболизма кетоновых тел.
Авитаминозы (F, D3).
Лизосомные болезни.
1. Нарушение переваривания и всасывания. Стеаторея – повышенное содержание липидов и СЖК в кале. Возможные причины развития стеатореи приведены на рис.14. При стеаторее кал бело-серого цвета с крупными (если нет желчи) или мелкими (если нет липазы) включениями жировых капель (непереваренные жиры).

Рис.14. Биохимические основы стеаторреи
2. Жировая дегенерация печени – отложение в печени триацилглицеринов (ТАГ), из-за невозможности синтеза фосфолипидов, необходимых для формирования ЛПОНП. Нарушение образования ЛПОНП приводит к невозможности экспорта синтезированных триацилглицеринов и их накоплении в печени. Одной из причин может быть недостаток липотропных веществ – этаноламина, холина, серина и метионина.
