
Чистота.
Парацетамол подвергают контролю на содержание примесей промежуточных продуктов синтеза. Обнаруживают допустимое содержание примеси п-хлорацетанилида методом ТСХ на пластинках Силуфол УФ-254 или Сорбфил по отношению к СОВС п-хлорацетанилида в смеси растворителей хлороформ-ацетон-толуол (65:25:10). Оценку пятен на хроматограммах выполняют в УФ-свете при длине волны 254 нм. Устанавливают также содержание примеси свободного п-аминофенола (не более 0,005%). Для выполнения испытания предварительно готовят для контроля парацетамол, не содержащий п-аминофенола (перекристаллизацией из воды). Затем растворяют испытуемый и контрольный парацетамол в смеси метанола и воды (1:1). В качестве реактива используют свежеприготовленный раствор нитропруссида натрия. Окраска раствора испытуемого парацетамола не должна быть интенсивнее, чем у контрольного раствора.
Парацетамол при кипячении (2 мин) с разведенной хлороводородной или серной кислотой вследствие гидролиза выделяет уксусную кислоту, которую можно обнаружить по запаху:
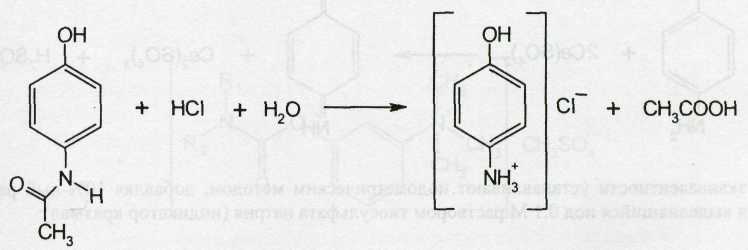
Реакцию кислотного гидролиза используют для испытания на подлинность и в различных способах количественного определения.
Парацетамол количественно определяют по образующемуся при кипячении с обратным холодильником в течение 1 часа продукту кислотного гидролиза — гидрохлориду п-аминофенола, используя нитритометрический метод:
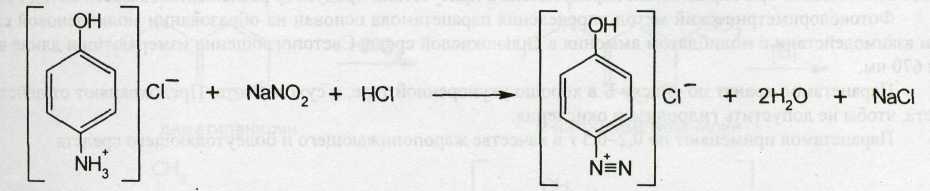
Эквивалентную точку устанавливают потенциометрически или с помощью внешнего индикатора — иодкрахмальной бумаги (ФС), которая синеет от выделившегося при добавлении избытка титранта иода:

![]()
Эквивалентную точку при нитритометрическом определении парацетамола можно также установить со смешанным внутренним индикатором, содержащим 0,1%-ный раствор тропеолина 00 и 0,15%-ный раствор метиленового синего.
Парацетамол, являющийся слабой кислотой (рКа = 9,92), можно количественно определить в неводной среде. Растворителем служит безводный ацетон, титрантом — гидроксид калия в изопропиловом спирте. Эквивалентную точку устанавливают потенциометрическим методом в электрохимической ячейке со стеклянным электродом сравнения и сурьмяным индикаторным электродом.
Способ обратного цериметрического определения парацетамола основан на предварительном кислотном гидролизе и последующем окислении п-аминофенола избытком 0,1 М раствора сульфата церия. Процесс идет по схеме:
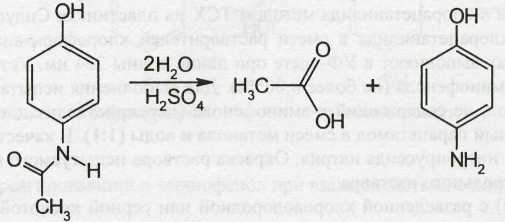
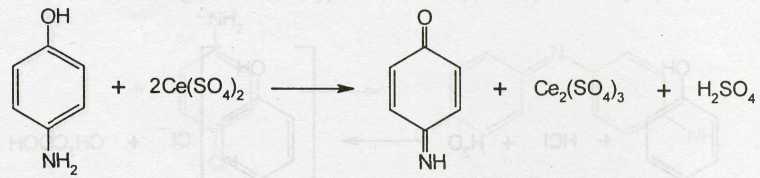
Точку эквивалентности устанавливают иодометрическим методом, добавляя 10%-ный раствор иодида калия и титруя выделившийся йод 0,1 М раствором тиосульфата натрия (индикатор крахмал):
![]()
В лекарственных формах парацетамол определяют спектрофотометрическим методом в максимуме поглощения (при 257 нм) с использованием в качестве растворителя 0,1 М раствора гидроксида натрия. Разработан способ спектрофотометрического определения парацетамола в таблетках, основанный на использовании в качестве стандартного образца дихромата калия (при длине волны 243 нм). Положительные результаты при анализе парацетамола в лекарственных формах были достигнуты методом производной спектрофотометрии. Более селективным при определении парацетамола в присутствии продуктов разложения оказался метод ГЖХ.
Фотоколориметрический метод определения парацетамола основан на образовании молибденовой сини при взаимодействии с молибдатом аммония в сильнокислой среде. Светопоглощение измеряют при длине волны 670 нм.
Хранение и применение.
Парацетамол хранят по списку Б в хорошо укупоренной таре, в сухом месте. Предохраняют от действия света, чтобы не допустить гидролиза и окисления.
Парацетамол применяют по 0,2-0,5 г в качестве жаропонижающего и болеутоляющего средств.
Производные диметилфенилацетамида.
Кроме сложных эфиров п-аминобензойной кислоты местноанестезирующую активность проявляют производные диметилфенилацетамида (I). Среди них тримекаина гидрохлорид, лидокаина гидрохлорид, являющиеся производными диалкиламиноацетанилида (II).
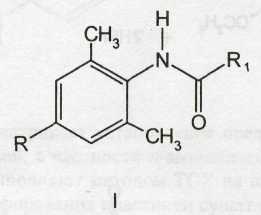
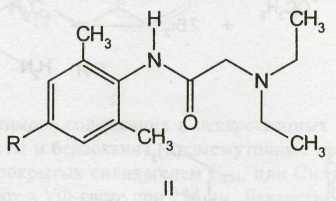
Получение.
Синтез тримекаина осуществляют по схеме:
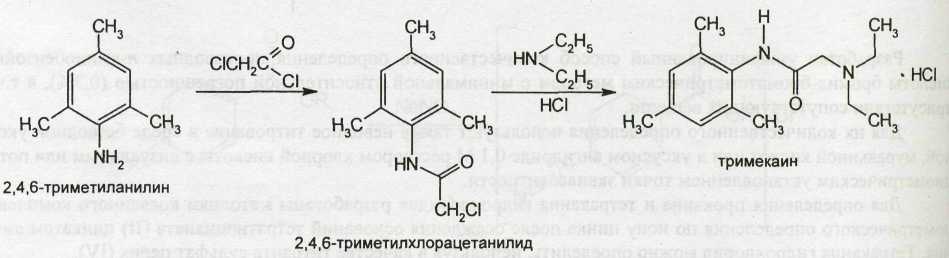
По такой же схеме синтезируют лидокаина гидрохлорид из 2,6-диметиланилина.
Физические свойства.
Trimecaine Hydrochloride — тримекаина гидрохлорид
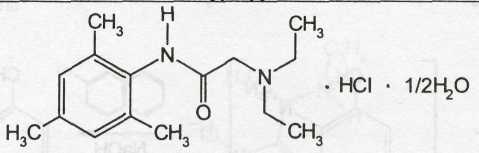
Белый или со слегка желтоватым оттенком кристаллический порошок. Т.пл. 139-142 °С.
Lidocaine Hydrochloride — лидокаина гидрохлорид
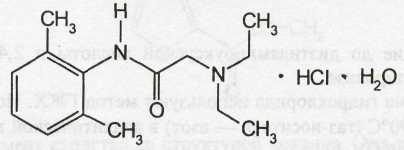
2-диэтиламино-2',6'-ацетоксилидида гидрохлорида моногидрат
Белый или почти белый кристаллический порошок, без запаха. Т.пл. 74-79 °С.
Тримекаина и лидокаина гидрохлориды очень легко растворимы в воде, легко растворимы в этаноле и хлороформе, практически нерастворимы в эфире.
Подлинность.
Установить подлинность тримекаина гидрохлорида можно по ИК-спектру, снятому в вазелиновом масле. Он должен в области от 4000 до 700 см-1 иметь те же полосы поглощения, что и спектр стандартного образца. УФ-спектр раствора тримекаина гидрохлорида в водно-спиртовой смеси, подкисленной хлороводородной кислотой имеет в области 250-300 нм максимумы поглощения при 262,5 нм и при 271 нм, а при 255 нм — минимум поглощения.
Тримекаина гидрохлорид даёт цветную реакцию с раствором ацетата меди (зеленое окрашивание). При добавлении к кристаллическому тримекаину гидрохлориду 2 капель концентрированной серной кислоты и 1 капли пергидроля появляется кроваво-красное окрашивание. Небольшая масса тримекаина гидрохлорида (0,001 г) при нагревании с несколькими каплями реактива Марки на водяной бане в течение 10 мин приобретает красное окрашивание. После добавления 10 капель воды появляется голубая флуоресценция.
Лидокаина гидрохлорид переводят в основание, растворяют в этаноле и испытывают на подлинность с помощью цветной реакции с раствором хлорида кобальта. Образуется синевато-зеленый осадок. Пикрат лидокаина гидрохлорида, промытый и высушенный после осаждения пикриновой кислотой, должен иметь температуру плавления около 230 °С.
При нагревании тримекаина и лидокаина гидрохлоридов с растворами щелочей или кислот образуются исходные продукты синтеза — 2,4,6-триметиланилин и 2,6-диметиланилин соответственно. Они вступают в реакции диазотирования и образования азокрасителя, характерные для первичных ароматических аминов:
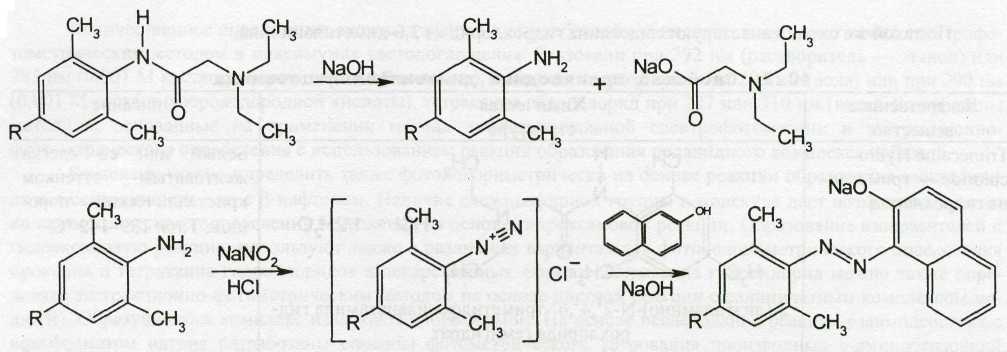
Гидролитическое расщепление до диэтиламиноуксусной кислоты и 2,4,6-триметиланилина или 2,6-диметиланилина происходит и при пиролизе.
Для идентификации лидокаина гидрохлорида используют метод ГЖХ.
Для отличия тримекаина гидрохлорида от других местноанестезирующих средств (тетракаина, прокаина) используют различные способы. Один из них основан на окислении тримекаина гидрохлорида при нагревании до 155-165 °С (масляная баня) в смеси сульфата меди (II) и концентрированной серной кислоты. После охлаждения смеси и добавления концентрированного раствора аммиака появляется синее окрашивание, а при УФ-облучении наблюдается красно-розовая флуоресценция.
Второй способ, рекомендованный ФС, заключается в выполнении микрокристаллоскопической реакции, которую проводят на предметном стекле, смешивая по 1 капле растворов тримекаина гидрохлорида, 0,1 М раствора дихромата калия и серной кислоты. Через 5-10 мин по краям смеси появляются кристаллы в виде игл, собранных в пучки или веточки.
Лекарственные вещества являются гидрохлоридами, поэтому дают положительную реакцию на хлорид-ион.
Чистота.
При испытании на чистоту в тримекаина гидрохлориде обнаруживают посторонние примеси методом ТСХ на пластинках Силуфол УФ-254, а в лидокаина гидрохлориде определяют наличие примеси первичных ароматических аминов (не более 0,01%) по цветной реакции с п-диметиламинобензальдегидом.
Количественное определение.
Количественное определение тримекаина и лидокаина гидрохлоридов выполняют методом неводного титрования, используя в качестве растворителя смесь муравьиной кислоты и уксусного ангидрида (1:20). Титрантом служит 0,1 М раствор хлорной кислоты, индикатор кристаллический фиолетовый или судан III (лидокаин). Химизм этого процесса подробно рассмотрен на примере эфедрина гидрохлорида.
Для определения тримекаина и лидокаина гидрохлоридов применимы также методы кислотно-основного титрования в водной среде (по связанной хлороводородной кислоте) и аргентометрии (по хлорид-иону).
Известны также способы спектрофотометрического определения тримекаина гидрохлорида в одном из максимумов поглощения и экстрационно-фотометрического анализа на основе реакции с салицилатным комплексом меди (II).
