
ЛЕКЦИЯ № 7
ТЕМА: «ЛЕКАРСТВЕННЫЕ СРЕДСТВА ИЗ ГРУППЫ ПРОИЗВОДНЫХ ПИРАЗОЛА»
Лекарственные средства, рассматриваемые на лекции:
анальгин, антипирин, бутадион.
План лекции.
1. Общая характеристика.
2. Синтез производных пиразола.
3. Свойства производных пиразола.
4. Испытания на подлинность и чистоту.
5. Количественное определение.
6. Хранение и применение.
Общая характеристика.

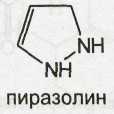
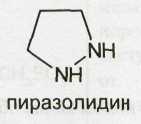
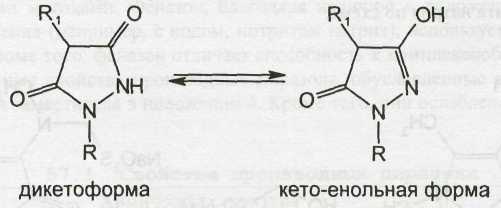
Применяют лекарственные вещества феназон (антипирин), метамизол-натрий (анальгин), структура которых содержит молекулу пиразолона-5. Для этого соединения возможно существование нескольких таутомерных форм:
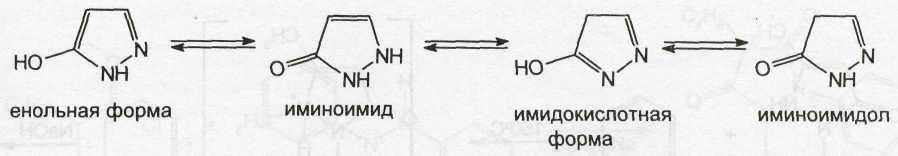
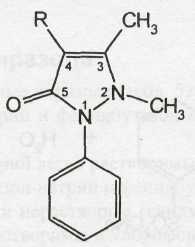
Феназон, метамизол-натрий можно рассматривать как производные пиразолина или пиразолона-5, находящегося в форме иминоимида (для простоты изложения в последующем они будут именоваться просто производными пиразолона). Общая формула этой группы лекарственных веществ:
Фенилбутазон (бутадион) и другие производные пиразолидиндиона, подобно пиразолону, могут существовать в виде нескольких таутомерных форм, в частности:
Синтез производных пиразола.
Феназон впервые был синтезирован в 1883 г. Кнорром из ацетоуксусного эфира и фенилгидразина. Современное промышленное производство феназона осуществляют из дикетена, который является продуктом пиролиза ацетона (при 500-600 °С над оксидом алюминия). Дикетен конденсируют с фенилгидразином:
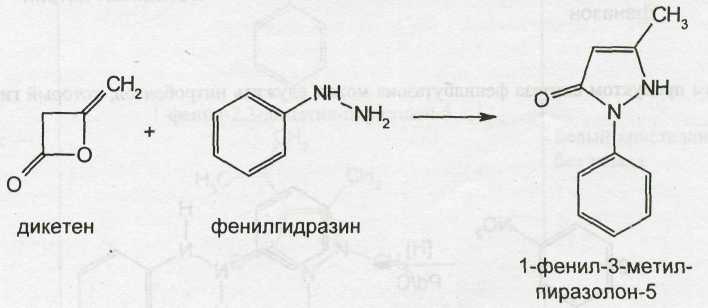
Образовавшийся 1-фенил-3-метилпиразолон-5 метилируют, применяя в качестве метилирующего агента метиловый эфир бензолсульфокислоты, который дает возможность увеличить выход феназона до 90%, не используя при этом высокое давление:
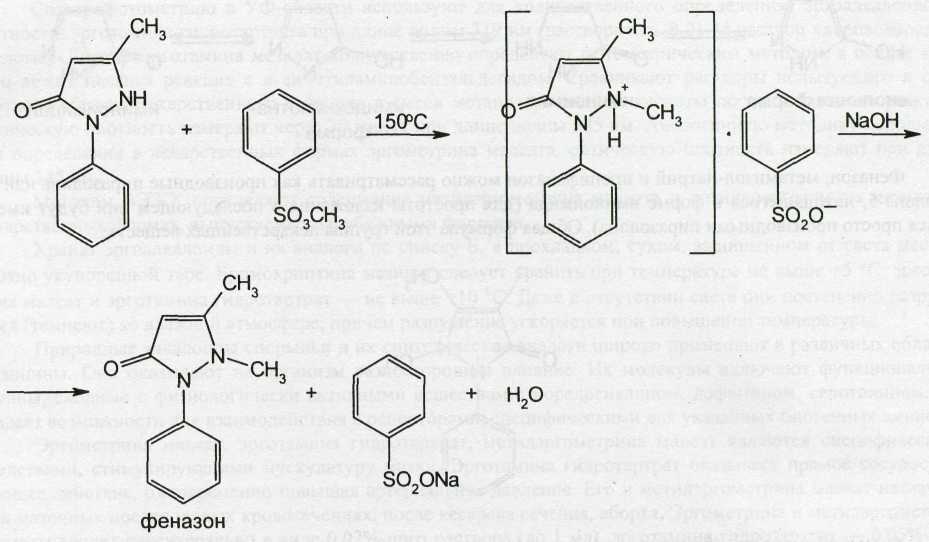
Синтез метамизола-натрия в промышленных условиях осуществляют из монометиламинофеназона и формальдегид-гидросульфита натрия по схеме:
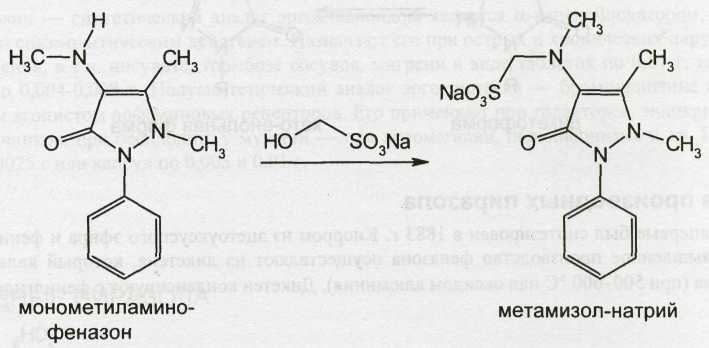
Исходным продуктом синтеза фенилбутазона может служить нитробензол, который гидрируют до гидразобензола:
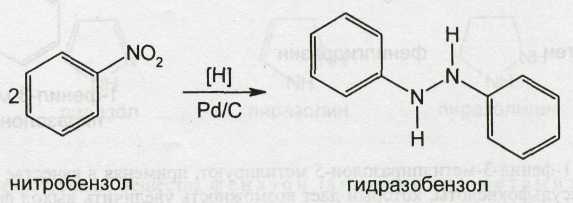
Гидразобензол конденсируют с хлорангидридом малоновой кислоты:
Свойства производных пиразола.
По физическим свойствам производные пиразола (табл. 57.1) представляют собой белые или бесцветные кристаллические вещества (метамизол-натрий и фенилбутазон могут иметь желтоватый оттенок), без запаха, горького вкуса.
Феназон очень легко, метамизол-натрий легко растворимы в воде, а фенилбутазон нерастворим в воде. В этаноле феназон легко растворим, а метамизол-натрий и фенилбутазон трудно или мало растворимы. В эфире и хлороформе метамизол-натрий практически нерастворим (ввиду наличия гидрофильной группы в молекуле). Остальные производные пиразола легко растворимы в хлороформе. Феназон мало растворим в эфире. Фенилбутазон легко растворим в эфире и ацетоне.
Несмотря на сходство химической структуры, производные пиразола отличаются друг от друга по химическим свойствам. Метамизол-натрий проявляет восстановительные свойства, которые используют для выполнения ряда цветных реакций с окислителями и количественного определения окислительно-восстановительными методами. Феназон, благодаря наличию в положении 4 подвижного водорода, вступает в реакции замещения (например, с йодом, нитритом натрия), используемые для качественного и количественного анализа. Кроме того, феназон отличает способность к комплексообразованию, например, с хлоридом железа (III). Основные свойства производных пиразола, обусловленные наличием двух гетероатомов азота, зависят от характера заместителя в положении 4. Кроме того, они ослаблены вследствие сопряженности с фенильным радикалом.
Phenazone — феназон (Антипирин)
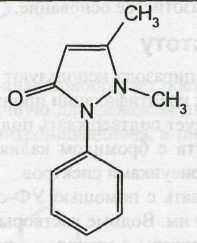
Бесцветные кристаллы или белый кристаллический порошок без запаха. Т. пл. 110—113°С.
Metamizole Sodium — метамизол-натрий (Анальгин)
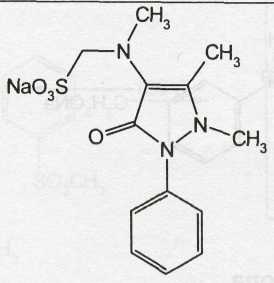
Белый с едва заметным желтоватым оттенком кристаллический порошок без запаха.
Phenylbutazone — фенилбутазон (Бутадион)
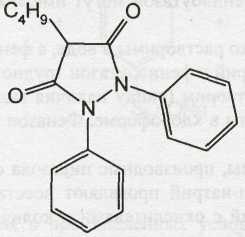
1,2-дифенил-4-бутилпиразолидиндион-3,5
Белый или белый со слегка желтоватым оттенком порошок. Т. пл. 104-107°С.
Поэтому феназон является практически нейтральным соединением. Метамизол-натрий ввиду наличия в молекуле остатка сульфита натрия образует водные растворы нейтральной реакции (на лакмус). Фенилбутазон обладает в ацетоновых растворах кислотными свойствами вследствие наличия подвижного атома водорода в положении 4. Это позволяет получать соли фенилбутазона с гидроксидом натрия и с солями тяжелых металлов. В среде концентрированных минеральных кислот он ведет себя как азотистое основание.
