
- •Развитие производства благородных металлов
- •Производство серебра
- •Применение благородных металлов
- •Поведение благородных металлов в различных средах
- •Азотно-кислые среды
- •Солянокислая среда
- •Аммиачные системы
- •Нитритные системы
- •Гидроксиды пм
- •Руды и минералы Au, Ag. Формы нахождения Au, Ag в рудах
- •Формы нахождения
- •Пробность
- •Схемы переработки кварцевых руд
- •Блок-схема переработки кварцево-сульфидных руд
- •Механическая подготовка руды
- •I. Метод амальгамации
- •II. Плавка золотой головки
- •III. Гидрометаллургичесие методы
- •Цианирование золотосодержащих руд
- •Химизм процесса
- •Термодинамика процесса
- •Кинетика процесса
- •Факторы, влияющие на процесс цианирования
- •III. Влияние температуры
- •IV. Вязкость пульп
- •VI. Крупность частиц руды и золота
- •VII. Состав золотин
- •Электрохимическая природа цианирования
- •Потери цианида
- •Практика цианирования
- •Схемы цианирования
- •II. Метод кучного выщелачивания
- •Хвостывосты
- •П ачуки. Рисунок 17.
- •Разделение золотосодержащих пульп
- •Цементация Zn
- •Электрохимическая природа цементации
- •Влияние примесей на процесс
- •Практика цементации
- •Переработка Au-Zn осадков (цианшламов)
- •Методы переработки
- •Свойства смол-сорбентов
- •Свойства смол. К смолам предъявляются следующие требования :
- •Закономерности сорбционного выщелачивания
- •Кинетика и механизм сорбции
- •Практика сорбционного выщелачивания
- •Параметры сорбционного выщелачивания
- •Аппаратура сорбционного цианирования
- •Регенерация смолы
- •Электролитическое выделение Au из тиомочевинного элюата
- •Устройство электролизной ванны
- •Сорбция на активированных углях
- •Особенности углеродистых сорбентов
- •Области применения активированных углей
- •Обезвреживание сточных вод зиф
- •Аффинаж золота и серебра
- •Хлорный процесс
- •Ag выделяют двумя способами:
- •Поведение примесей
- •Аппаратурное оформление
- •Ванны с горизонтальным расположением электродов
- •Электролитическое рафинирование Au
- •Поведение примесей
- •Аппаратура
Электролитическое выделение Au из тиомочевинного элюата
Электрохимическую ячейку для выделения Au можно представить:

А(Pt) [Au(Thio)2]+, K(Ti,C) [Ag(Thio)2]+
Thio, H+, SO42-,
H2O, примеси,
[Cu(Thio)3]2+ и др.
На аноде – окисление наиболее электроотрицательных элементов .
На катоде – наиболее электроположительных.
Рассмотрим электродные потенциалы наших элементов :
0 Au/Au(Thio)2+ = +0,38 (B); 0 Ag/Ag(Thio)2+ = +0,023 (B);
0 Cu/Cu(Thio)43+ = -0,12 (B); 0 Zn/Zn(Thio)22+ = -0,78 (B).
Отсюда видно, что на катоде протекают следующие процессы :
[Au(Thio)2]+ + e Au + 2Thio;
[Ag(Thio)2]+ + e Ag + 2Thio.
2H+ + 2e H2 – степень развития реакции высока из-за высокой концентрации H2SO4.
Поэтому к=10-20%.
На аноде возможно протекание 2-х реакций:
1. 2H2O = 4H+ + O2 + 4e;
2. Окисление Thio:
2CS(NH2)2 – 2e CS2(NH2)2(NH)2 + 2H+
формамидиндисульфид
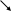
S CNNH2
Цианамид
Этот процесс происходит при повышенной плотности тока и является вредным, так как:
1. Происходит потери Тhio ;
2. Образуется элементарная сера, загрязняющая катодное Аu;
3. Bозможно обратное растворение золота с катода.
Поэтому на практике принимают все меры для предотвращения на аноде окисления Thio. Это достигается разделением катодного и анодного пространства с помощью ионитовой мембраны.
Использование в качестве анолита просто раствора H2SO4, в качестве католита – золото содержащий элюат (Au(Thio)2+ ).
Могут использоваться либо катионитовые, либо анионитовые мембраны (пластины из ионнообменных смол). Рисунок. 51.
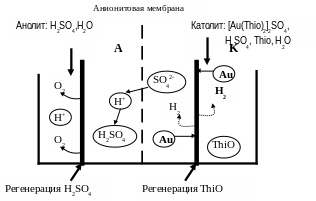
Рис.51.
Исследованиями установлено, что выделение Au лимитируется величиной предельного тока, т.е. процесс ограничивается диффузией [Au(Thio)2]+ к поверхности катода. Рисунок 52.
Рис. 52.
Пути интенсификации :
1. Увеличение интенсивности перемешивания;
2. Повышение температуры ;
3.Увеличение катодной поверхности.
Перемешивание oсуществляется:
1. Н2;
2. Принудительным движением элемента по катодной камере.
Температура: до 40500С.
Увеличение катодной поверхности достигается двумя путями:
1. Использование пластинчатых электродов, выполненных из Ti ;
2. Использование волокнистых углеграфитовых материалов (углеродистый ватин);
- толщина нитей 5 10мкм;
удельная поверхность 1кг ватина до 300 м2 (0,2 0,3м2/г).
