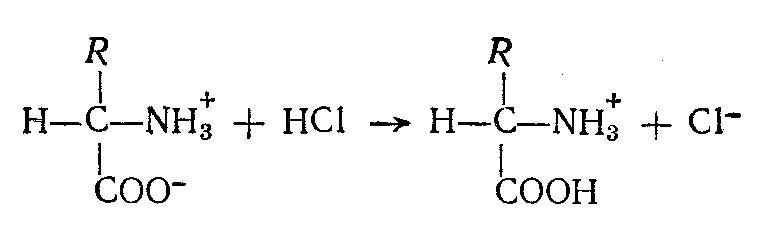- •Моносахариды
- •Олигосахариды
- •Полисахариды
- •Биохимия липидов
- •1. Химический состав и биологическая роль липидов
- •2. Характеристика классов липидов
- •Нейтральные жиры
- •Структурная организация белков
- •Форма белковых молекул
- •Свойства белков
- •Нуклеиновые кислоты
- •Ферменты
- •Строение ферментов и коферментов
- •Свойства ферментов
Нейтральные жиры
К нейтральным жирам относится группа липидов, состоящих из трехатомного спирта — глицерина и трех остатков жирных кислот, поэтому они называются триглицеридами.
В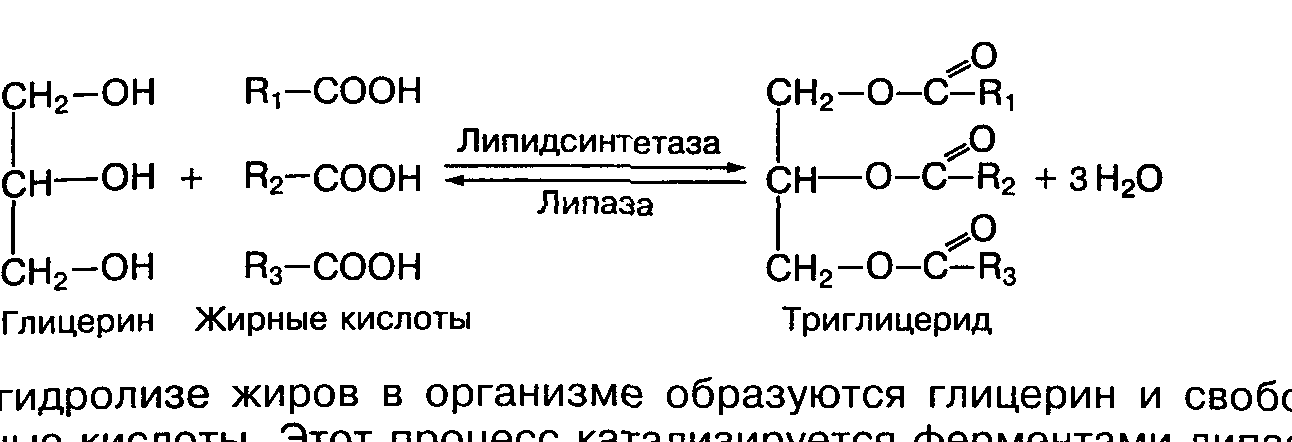 состав нейтральных жиров могут входить
одинаковые жирные кислоты, например
пальмитиновая. В таком случае образуется
сложный эфир - триглицерид трипальмитин.
Это простые жиры. Если жиры содержат
остатки разных жирных кислот, то
образуются смешанные жиры.
состав нейтральных жиров могут входить
одинаковые жирные кислоты, например
пальмитиновая. В таком случае образуется
сложный эфир - триглицерид трипальмитин.
Это простые жиры. Если жиры содержат
остатки разных жирных кислот, то
образуются смешанные жиры.
В данном уравнении реакции показаны обратимые процессы синтеза (верхняя стрелка) и гидролиза (нижняя) жира.
Природные жиры отличаются большим разнообразием входящих в их состав жирных кислот, их различным расположением в молекуле и степенью ненасыщенности. Потенциально могут существовать миллионы изомеров триглицеридов.
Жирные кислоты — органические кислоты с длинной углеводородной цепью (радикалом R), содержащей от 4 до 24 и более атомов углерода, и одной карбоксильной группой. Общая формула жирных кислот имеет вид
СnН2n+1СООН, или R-COOH.
Для многих жирных кислот характерно наличие четного числа атомов углерода, что обусловлено, по-видимому, их синтезом путем прибавления двууглеродных звеньев к растущей углеводородной цепи.
В состав жиров организма человека чаще всего входят жирные кислоты с 16 или 18 атомами углерода, которые называются высшими жирными кислотами. Высшие жирные кислоты разделяются на насыщенные предельные) и ненасыщенные (непредельные)
-
Насыщенные кислоты
Ненасыщенные кислоты
С3Н7СООН Масляная (бутановая)
С17Н33СООН Олеиновая
С11Н23СООН Лауриновая
С17Н31СООН Линолевая
С15Н31СООН Пальмитиновая
С17Н29СООН Линоленовая
С17Н35СООН Стеариновая
С19Р31СООН Арахидоновая
В насыщенных жирных кислотах все свободные связи углеродных атомов заполнены водородом. Такие жирные кислоты не имеют двойных или тройных связей в углеродной цепи. Ненасыщенные жирные кислоты имеют в углеродной цепи двойные связи (-С=С-), первая из которых возникает между девятым и десятым атомами углерода от карбоксильной группы. Жирные кислоты с тройными связями встречаются редко. Жирные кислоты, содержащие две и более двойных связей, называются полиненасыщенными.
С увеличением числа углеродных атомов в молекулах жирных кислот температура их плавления увеличивается. Жирные кислоты могут быть твердыми веществами (например, стеариновая) либо жидкими (например, линолевая, арахидоновая); они не растворимы в воде и весьма слабо растворимы в спирте.
Твердые жиры — это жиры животного происхождения, за исключением рыбьего жира. Жидкие жиры — это растительные масла, за исключением кокосового и пальмового масел, которые затвердевают при охлаждении. В организме животных и у растений ненасыщенных жирных кислот в два раза больше, чем насыщенных.
Ненасыщенные жирные кислоты более реакционноспособны, чем насыщенные. Они легко присоединяют два атома водорода по месту двойных связей, превращаясь в насыщенные:
Этот процесс называется гидрогенизацией. Вещества, подвергнутые гидрогенизации, изменяют свои свойства. Например, растительные масла превращаются в твердый жир. Реакция гидрогенизации широко используется для получения твердого пищевого жира — маргарина из жидких растительных масел.
Особое значение для человека имеют полиненасыщенные жирные кислоты. В организме они не синтезируются. При их недостатке или отсутствии в пище нарушается обмен жиров, в частности холестерина, наблюдаются патологические изменения в печени, коже, функции тромбоцитов. Поэтому такие ненасыщенные жирные кислоты, как линоленовая и линолевая, — незаменимые факторы питания. Кроме того, они способствуют выходу из печени жиров, которые синтезируются в ней, и предупреждают ее ожирение. Такое действие ненасыщенных жирных кислот называется липотропным эффектом. Ненасыщенные жирные кислоты служат предшественниками синтеза биологически активных веществ — простагландинов. Суточная потребность человека в полиненасыщенных кислотах в норме составляет примерно 15 г.
Нейтральные жиры накапливаются в жировых клетках (адипоцитах), под кожей, в молочных железах, жировых капсулах вокруг внутренних органов брюшной полости; незначительное их количество находится в ске¬летных мышцах. Образование и накопление нейтральных жиров в жировых тканях называется депонированием. Триглицериды составляют основу резервных жиров, которые являются энергетическим запасом организма и используются при голодании, недостаточном употреблении жиров, длительных физических нагрузках.
Нейтральные жиры входят также в состав клеточных мембран, сложных белков протоплазмы и называются протоплазматическими. Протоплазматические жиры не используются в качестве энергетического источника даже при истощении организма, так как выполняют структурную функцию. Их количество и химический состав постоянны и не зависят от состава пищи, тогда как состав резервных жиров постоянно изменяется. У человека протоплазматические жиры составляют около 25 % всей массы жира в организме (2—3 кг).
В различных клетках организма, особенно в жировой ткани, постоянно протекают ферментативные реакции биосинтеза и распада нейтральных жиров:
При гидролизе жиров в организме образуются глицерин и свободные жирные кислоты. Этот процесс катализируется ферментами липазами. Процесс гидролиза жиров в тканях организма называется липолизом. Скорость липолиза значительно увеличивается при физических нагрузках на выносливость, а активность липаз повышается в процессе тренировки.
Если реакцию распада жира проводить в присутствии щелочей (NaOH, КОН), то образуются натриевые или калиевые соли жирных кислот, которые называются мылами, а сама реакция — омылением. Эта химическая реакция лежит в основе производства мыла из различных жиров и их смесей.
Фосфолипиды
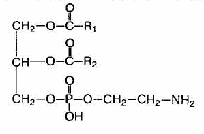
Фосфолипиды — это жироподобные вещества, состоящие из спирта (чаще глицерина), двух остатков жирных кислот, остатка фосфорной кислоты и азотсодержащего вещества (аминоспирта — холина или коламина).
Если в молекулы фосфолипида входит холин, они называются лецитины, а если коламин – кефалины.
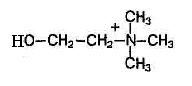
![]()
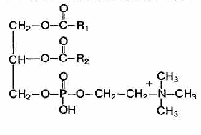
 Холин
Коламин
Холин
Коламин
Альфа-лецитин Альфа-кефалин
Строение бета-изомеров отличается тем, что остатки фосфорной кислоты и аминоспирта расположены у второго (среднего) углеродного атома глицерина.
Фосфатиды, особенно лецитин в большом количестве содержатся в желтке яиц. В организме человека они широко распространены в нервной ткани. Фосфолипиды играют важную биологическую роль, являясь структурным компонентом всех клеточных мембран, поставщиками холина, необходимого для образования нейропередатчика — ацетилхолина. От фосфолипидов зависят такие свойства мембран, как проницаемость, рецепторная функция, каталитическая активность мембраносвязанных ферментов.
Фосфолипиды доминируют в мембранах животной клетки, они содержатся также во многих ее субклеточных частицах.
Биологическая роль фосфолипидов в организме значительна и разнообразна. В качестве непременного компонента биологических мембран фофолипиды принимают участие в их барьерной, транспортной, рецепторной функциях, в разделении внутреннего пространства клетки на клеточные органеллы — «цистерны», отсеки. Эти функции мембран относят в настоящее время к важнейшим регуляторным механизмам жизнедеятельности клеток. Присутствие фосфолипидов в мембранах необходимо и для функционирования мембранносвязанных ферментных систем.
СТЕРОИДЫ
С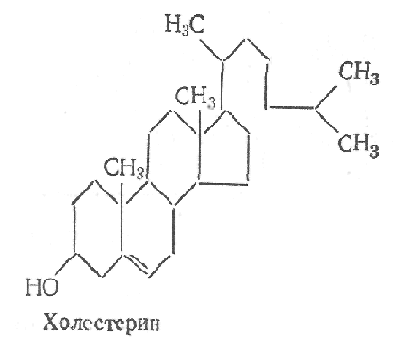 тероиды
относятся к неомыляемым липидам. По
химической природе стероиды - производные
циклопентанпергидрофенантрена. Их
разделяют на стерины и стериды. Стерины
— высокомолекулярные циклические
спирты, имеющие в составе молекулы ядро
циклопентанпергидрофенантрена.
тероиды
относятся к неомыляемым липидам. По
химической природе стероиды - производные
циклопентанпергидрофенантрена. Их
разделяют на стерины и стериды. Стерины
— высокомолекулярные циклические
спирты, имеющие в составе молекулы ядро
циклопентанпергидрофенантрена.
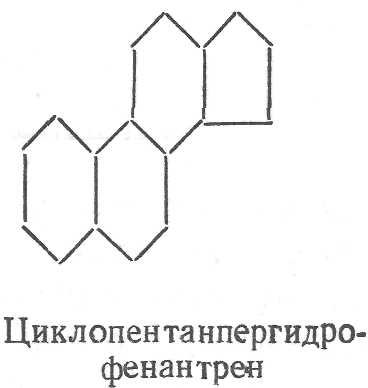
В состав различных тканей входят также стериды — сложные эфиры, образованные стеринами и жирными кислотами. Стерины и их производные выполняют разнообразные функции в организме. Большое биологическое значение в животном организме имеет холестерин. Нарушение его обмена может повлечь патологические изменения сосудов — атеросклероз. Холестерин служит биологическим предшественником желчных кислот, стероидных гормонов. Желчные кислоты имеют большое значение в процессе расщепления липидов в кишечнике. Стероидные гормоны регулируют многочисленные процессы обмена веществ.
БЕЛКИ
Наиболее важными соединениями каждого организма являются белки. Они обязательно обнаруживаются во всех клетках организма, в большинстве из них на долю белка приходится более половины сухого остатка. Все основные проявления жизни связаны с белками. «Жизнь, — писал Ф. Энгельс, — есть способ существования белковых тел... Повсюду, где мы встречаем жизнь, мы находим, что она связана с каким-либо белковым телом, и повсюду, где мы встречаем какое-либо белковое тело, не находящееся в процессе разложения, мы без исключения встречаем и проявления жизни».
Белки - высокомолекулярные азотосодержащие органические соединения, состоящие из остатков аминокислот. В составе некоторых белков наряду с аминокислотами обнаруживают и другие соединения.
Для живых организмов характерно большое разнообразие белков, которые составляют основу структуры организма и обеспечивают множество его функций. Полагают, что в природе существует примерно 1010—1012 различных белков, что и объясняет большое многообразие живых организмов. В одноклеточных организмах насчитывают около 3000 различных белков, а в организме человека — около 5000000.
Несмотря на сложность строения и многообразие, все белки построены из сравнительно простых структурных элементов — аминокислот. Белки представляют собой полимерные молекулы, в состав которых входит 20 различных аминокислот. Изменение числа аминокислотных остатков и последовательности их расположения в молекуле белка обеспечивает возможность образования громадного количества белков, отличающихся своими физико-химическими свойствами, структурной или функциональной ролью в организме.
Для любого организма белки играют решающую роль во всех процессах жизнедеятельности. С ними связаны такие свойства живого организма, как раздражимость, сократимость, пищеварение, способность к росту, размножению, движению. Следовательно, белки являются главными носителями жизни. В неживой природе соединения, подобные белкам, не встречаются.
Химический состав и биологическая роль белков
Белки — высокомолекулярные азотсодержащие вещества, при гидролизе которых образуются аминокислоты. Иногда белки называют протеинами (от греч. proteus — первый, главный), определяя тем самым их важнейшую роль в жизнедеятельности всех организмов. Белок в организме человека составляет в среднем 45 % сухой массы тела (12—14 кг). Содержание его в отдельных тканях различное. Наибольшее количество белка содержится в мышцах, костях, коже, пищеварительном тракте и других плотных тканях.
Суточная потребность в белке взрослого человека, не занимающегося спортом, составляет в среднем 1,3 г на 1 кг массы тела или около 80 г. При больших энерготратах потребность в них увеличивается примерно на 10 г на каждые 2100 кДж увеличивающихся затрат энергии.
Белки поступают в организм преимущественно с пищей животного происхождения. В растениях белков содержится значительно меньше: в овощах и фруктах — всего 0,3—2,0 % массы свежей ткани; наибольшее количество белков — в бобовых — 20—30 %, злаках — 10—13 и грибах — 3—6 %.
Элементарный состав белков. Важнейшими химическими элементами всех белков являются углерод (50—55 %), кислород (21—23 %), водород (6,5— 7,3%), азот (15—18%), сера (0,3—2,5%). В составе белков обнаружены также фосфор, железо, йод, медь, марганец и другие химические элементы.
Содержание белкав в органах и тканях человека
-
Органы и ткани
Содержание белка, %
от сухой ткани
от общего белка тела
Скелетные мышцы
80
34,7
Кожа
60
11,5
Кости (твердые ткани)
20
18,7
Пищеварительный тракт
63
1,8
Мозг и нервная ткань
45
2,0
Печень
57
3,6
Сердце
60
0,7
Легкие
82
3,7
Селезенка
84
0,2
Почки
72
0,5
Поджелудочная железа
47
0,1
Жировая ткань
14
6,4
Остальные ткани:
жидкие
85
1,4
плотные
54
14,6
Все тело
45
100,0
Количественный и качественный состав отдельных белков различен. Все белки содержат постоянное количество азота, равное в среднем 16%. Поэтому по количеству азота, поступившего с пищей (процентное содержание азота пищи умножают на пересчетный коэффициент 6,25), определяют потребление белка организмом.
Аминокислотный состав. Белки состоят из аминокислот. Известно около 200 различных аминокислот, однако для построения белков в животных и растительных тканях используются только 20. Называются эти аминокислоты основными.
Наряду с основными в состав отдельных белков входят другие аминокислоты — неосновные. Каждая такая аминокислота происходит от одной из 20 основных аминокислот. Например, 4-гидроксипролин и 5-дигидро-ксилизин являются производными пролина и лизина и входят в состав коллагена — белка соединительной ткани:
Простые и сложные белки. В зависимости от химического состава белки делятся на простые и сложные. Простые белки состоят только из аминокислот, среди которых есть растворимые в воде (гистоны, альбумины, фибриноген) и не растворимые (глобулины, миозин, коллаген, осеин, кератин). Сложные белки состоят из белковой и небелковой частей. Небелковая часть может быть представлена углеводами, нуклеиновыми кислотами, липидами, фосфорной кислотой, окрашенными (хромо-) веществами. В зависимости от природы небелковой части сложные белки делятся на гликопротеиды, нуклеопротеиды, липопротеиды, фосфопротеиды, хромопротеиды. Все они выполняют разнообразные функции в организме.
Биологические функции белков
Структурная (пластическая). В комплексе с липидами белки составляют структуру всех клеточных мембран и основу цитоплазмы клеток. Структурной основой соединительной ткани являются такие белки, как коллаген (входит в состав хрящей и сухожилий), кератин (входит в состав кожи), эластин (входит в состав связок и стенок сосудов).
Каталитическая. Эту функцию выполняют специфические белки-ферменты, регулирующие обмен веществ и энергии в организме. Если ферменты не работают в клетке, то биохимические реакции не протекают и живая клетка может погибнуть.
Сократительная. Все виды сокращения и движения скелетных мышц, миокарда и других сокращающихся тканей обеспечивают сократительные белки актин и миозин.
Транспортная. Белки способны связывать и транспортировать с током крови или через клеточные мембраны отдельные молекулы и ионы. Например, гемоглобин эритроцитов крови переносит кислород от легких к тканям и углекислый газ — от тканей к легким; миоглобин мышц переносит кисло род в мышечной ткани к местам его использования. Отдельные белки кро ви транспортируют жирные кислоты, липиды, железо, некоторые гормоны.
Защитная. Белки иммунной системы гаммаглобулины "узнают" и связывают чужеродные вещества, поступающие в организм, защищая тем самым его от вирусов, бактерий и клеток других организмов. Защитную функцию выполняет также белок интерферон. Белки плазмы крови фибриноген и тромбин участвуют в процессах свертывания крови, предотвращая кровопотери при ранениях.
Гормональная, или регуляторная. Высокоспецифические белки-гормоны регулируют обмен веществ.
Рецепторная. Многие белки являются рецепторами гормонов, нейро- медиаторов, других биологически активных веществ. Они осуществляют избирательное узнавание, связывание и передачу их регуляторного действия.
Передача наследственной информации. Белки входят в состав хромосом и участвуют в воспроизведении генетической информации, в регуляции процессов роста и размножения.
Опорная. Упругость и прочность костей скелета, кожи, сухожилий обеспечивают преимущественно белки коллаген и эластин.
Энергетическая. Около 10—15% энергопотребления организма обеспечивается белками. При окислении 1 г белков выделяется 17 кДж (4,1 ккал) энергии.
 Аминокислоты
Аминокислоты
При нагревании белков до высоких температур с крепкими кислотами, щелочами, а также под действием ферментов белковые молекулы расщепляются на более . простые соединения. На основании изучения конечных продуктов гидролиза белков было найдено, что в состав молекулы входит до 20 различных аминокислот. Аминокислотами называют соединения, содержащие одновременно аминные и карбоксильные группы. Молекулы большинства природных аминокислот имеют общую структуру, в которой аминогруппа находится в альфа-положении по отношению к карбоксильной:
Следовательно, аминогруппа присоединена к ближайшему от карбоксила углеродному атому. Некоторые аминокислоты имеют аминогруппу в бета- или -гамма-положении.
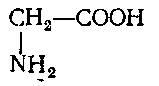
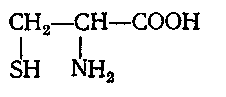
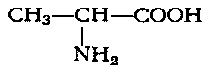
Глицин Аланин Цистеин
А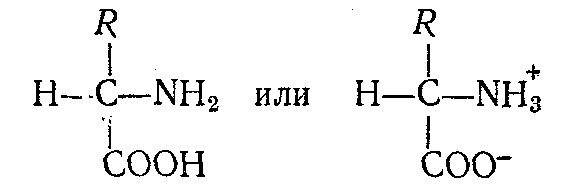 минокислоты
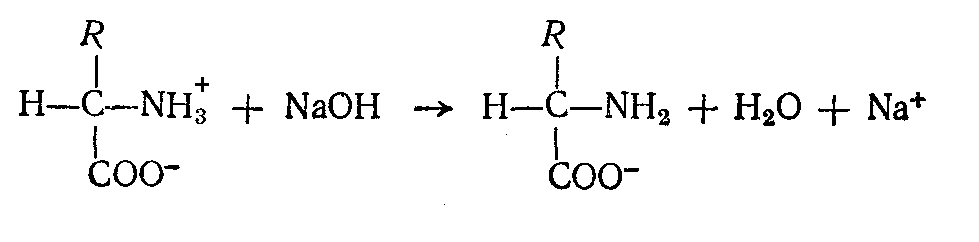
являются амфотерными электролитами,
т. е. обладают свойствами кислот и
оснований и могут реагировать как с
основаниями, так и кислотами:
минокислоты
являются амфотерными электролитами,
т. е. обладают свойствами кислот и
оснований и могут реагировать как с
основаниями, так и кислотами: