
- •2.Периодический закон менделеева.
- •3.Ядерная модель атома.
- •4. Виды химической связи.
- •7.Понятие о растворах
- •8.Растворы электролитов.
- •9.Комплексные соединения.
- •10.Грубодисперсные системы.
- •11.Водородный электрод.
- •12.Коррозия Ме.
- •13.Вяжущие вещества.
- •14.Керамика.
- •15.Дефекты облицовки зданий.
- •18. Гидрофобизация строительных материалов
- •Методы гидрофобизации строительных материалов и конструкций
- •18.Солевая коррозия кирпичной кладки.
7.Понятие о растворах
Раство́р — гомогенная (однородная) смесь, образованная не менее чем двумя компонентами, один из которых называется растворителем, а другой растворимым веществом, это также система переменного состава, находящаяся в состоянии химического равновесия.
Химический раствор - это смесь одной или нескольких кислот с водой.
Чаще под раствором подразумевается жидкое вещество, например раствор соли или спирта в воде (или даже раствор золота в ртути — амальгама).
Существуют также растворы газов в жидкостях, газов в газах и жидкостей в жидкостях, в последнем случае растворителем считается вода, или же компонент, которого больше.
В химической практике обычно под растворами понимают гомогенные системы, растворитель может быть жидким, твёрдым (твёрдый раствор), газообразным.
Зако́н Ге́нри — закон, по которому при постоянной температуре растворимость газа в данной жидкости прямо пропорциональна давлению этого газа над раствором. Закон пригоден лишь для идеальных растворов и невысоких давлений.
C=kp
где:
p — парциальное давление газа над раствором,
c— концентрация газа в растворе в долях моля,
k— коэффициент Генри.
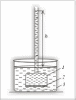
Явление самопроизвольного перехода растворителя через полупроницаемую перегородку в раствор называется осмосом. Через некоторое время объем раствора в сосуде 1 увеличится и его уровень поднимется выше уровня растворителя в сосуде 3 на высоту h.
В результате увеличения объема раствора в сосуде 1 возникает гидростатическое давление, называемое осмотическим давлением, которое количественно оценивается высотой h подъема жидкости в сосуде 1.
Процесс перехода растворителя в раствор самопроизволен, но обратный процесс самопроизвольно осуществляться не может, и для разделения раствора на растворитель и растворенное вещество следует затратить работу. Если в сосуде 1 с раствором увеличить давление, то растворитель будет переходить в обратном направлении через мембрану 2 в сосуд 3. Этот процесс называется обратным осмосом, его используют для опреснения морской воды.
Прибор для определения
осмотического давления:
1 – сосуд с раствором;
2 – полупроницаемая перегородка;
3 – сосуд с растворителем
Рассмотрим закон Вант-Гоффа: осмотическое давление раствора численно равно тому давлению, которое производило бы данное количество растворенного вещества, если бы оно в виде идеального газа занимало при данной температуре объем, равный объему раствора.
Все описанные законы относятся к бесконечно разбавленным растворам.
Давоение пара, давление, оказываемое паром, когда он испаряется с поверхности жидкости или твердого тела. В случае, если в замкнутом пространстве с поверхности испаряется столько же молекул, сколько возвращается и оседает, такое равновесие называется давлением насыщенного пара. Если твердое тело переходит в жидкое состояние, давление паров жидкости уменьшается пропорционально относительной молекулярной массе. Это имеет значение для химических анализов.
Первый закон Рауля связывает давление насыщенного пара над раствором с его составом; он формулируется следующим образом:
Парциальное давление насыщенного пара компонента раствора прямо пропорционально его мольной доле в растворе, причём коэффициент пропорциональности равен давлению насыщенного пара над чистым компонентом.

Растворы, для которых выполняется закон Рауля, называются идеальными. Идеальными при любых концентрациях являются растворы, компоненты которых очень близки по физическим и химическим свойствам, и образование которых не сопровождается изменением объёма и выделением либо поглощением теплоты.
Отклонения от закона Рауля
Растворы, компоненты которых существенно различаются по физическим и химическим свойствам, подчиняются закону Рауля лишь в области очень малых концентраций; при больших концентрациях наблюдаются отклонения от закона Рауля. Случай, когда истинные парциальные давления паров над смесью больше, чем вычисленные по закону Рауля, называют положительными отклонениями. Противоположный случай, когда парциальные давления паров компонентов оказываются меньше вычисленных — отрицательные отклонения.
Причиной отклонений от закона Рауля является то обстоятельство, что однородные частицы взаимодействуют друг с другом иначе, чем разнородные (сильнее в случае положительных и слабее в случае отрицательных отклонений).
Второй закон Рауля
Тот факт, что давление паров над раствором отличается от давления паров над чистым растворителем, существенно влияет на процессы кристаллизации и кипения. Из первого закона Рауля выводятся два следствия, касающиеся понижения температуры замерзания и повышения температуры кипения растворов, которые в объединённом виде известны как второй закон Рауля.
Понижение
температуры кристаллизации растворов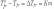
Условием кристаллизации является равенство давления насыщенного пара растворителя над раствором давлению пара над твёрдым растворителем. Поскольку давление пара растворителя над раствором всегда ниже, чем над чистым растворителем, это равенство всегда будет достигаться при температуре более низкой, чем температура замерзания растворителя. Так, океанская вода начинает замерзать при температуре около минус 2 °C.
Разность между температурой кристаллизации растворителя T°fr и температурой начала кристаллизации раствора Tfr есть понижение температуры кристаллизации.
Понижение температуры кристаллизации бесконечно разбавленных растворов не зависит от природы растворённого вещества и прямо пропорционально моляльной концентрации раствора.
