
- •4.Пути использования глицина и серина
- •8.Строение кетоновых тел
- •9.Синтез гема
- •11.Транспортные формы, выделение углекислого газа из организма
- •Окислительное фосфорилирование адф. Механизм сопряжения окисления и фосфорилирования. Коэффициент окислительного фосфорилирования (р/о).
- •15. Функции слюны
- •1. Образование ацетил-sКоА из глюкозы, других моносахаров или кетогенных аминокислот.
- •2. Перенос ацетил-sКоА из митохондрий в цитозоль:
- •3. Образование малонил-sКоА из ацетил-sКоА.
- •4. Синтез пальмитиновой кислоты.
- •18.Минерализация костной ткани и твердых тканей зуба
- •Окислительное декарбоксилирование пирувата
- •Структурные гликопротеины.
- •Протеогликаны
- •Этапы минерализации костной ткани
18.Минерализация костной ткани и твердых тканей зуба
В основе этого процесса — образование кристаллов апатита с участием фосфата кальция.
В организме внеклеточная жидкость перенасыщена фосфатом кальция и он начинает осаждаться.
Выделяют 2 стадии осаждения фосфата кальция:
▪нуклеация — образование плотного осадка (ядра);
▪рост кристаллов из ядра — эпитаксис.
Нуклеация бывает гомогенная (кристаллы образуются без участия другой фазы) и
гетерогенная (образование кристаллов инициирует другая фаза, играющая роль матрицы-затравки). Матрица может и направлять рост кристаллов. Роль матрицы выполняют
протеогликаны, гликозаминогликаны, Са-связывающие белки: фосфопротеины и белки,
содержащие γ-карбоксиглутаминовую кислоту (γ-КГК), для синтеза которой нужен витамин К.
Теории минерализации костной ткани и твердых тканей зуба:
1)физико-химическая, в основе которой лежат названные выше 2 стадии;
2)ферментная: щелочная фосфатаза костной ткани гидролизует фосфорорганические
эфиры, в результате этого освобождается фосфат-ион, что при наличии кальция и
матрицы вызывает рост кристаллов ГА;
3)смешанная: сначала синтезируется внеклеточный матрикс, а затем наступает этап
минерализации из-за перенасыщенного состояния раствора фосфата кальция и наличия
матрицы.
НЕКОЛЛАГЕНОВЫЕ БЕЛКИ КОСТНОЙ ТКАНИ И ИХ РОЛЬ
В ПРОЦЕССАХ МИНЕРАЛИЗАЦИИ
Остеокальцин: 1) содержит 3 остатка γ-КГК → связывает Са 2+ ; 2) прочно связан с
апатитом; 3) участвует в росте кристаллов.
Костный сиалопротеин: 1) содержит трипептид АРГ-ГЛИ-АСП (R-G-D) → способен
связываться с другими клетками, макромолекулами и рецепторами клеточных мембран; 2) через
специальный рецептор (10 остатков ГЛУ) связывается с Са 2+; 3) относится к фосфопротеинам,
тесно связан с клетками и апатитом; 4) присоединяет остеобласты к кости в период ее синтеза.
Остеопонтин: 1) содержит трипептид R-G-D; 2) связывается с Са 2+; 3) прочно связан с
апатитом.
Остеонектин: 1) имеет Са-связывающий домен, хотя в нем и нет γ-КГК; 2) связывается с
коллагеном и апатитом.
Тромбоспондин: 1) содержит трипептид R-G-D; 2) связывается с поверхностями клеток и
другими белками костной ткани.
Костный кислый гликопротеин: участвует в минерализации костной ткани.
I. Белки, нерастворимые в ЭДТА и НCl, проявляют сродство к коллагену и эластину и играют роль "скелета". Этот скелет, во-первых, придает устойчивость структуре эмали, во-вторых, на нем крепится. Этот белок и является функциональной единицей белковой матрицы
Са-связывающий белок образует нерастворимый комплекс с Са2+, одна его молекула способна связать 8-10 ионов Са. Часть этого кальция используется на создание белковой трехмерной матричной сетки, а другая – на взаимодействие сетки с минеральной фазой – гидроксиапатитом эмали.
Кроме того, в образовании агрегатов Са-связывающего белка большую роль играют фосфолипиды, которые локализованы в местах контакта Са-связывающего белка и минеральной фазы. (рис. в «Биохимии полости рта»
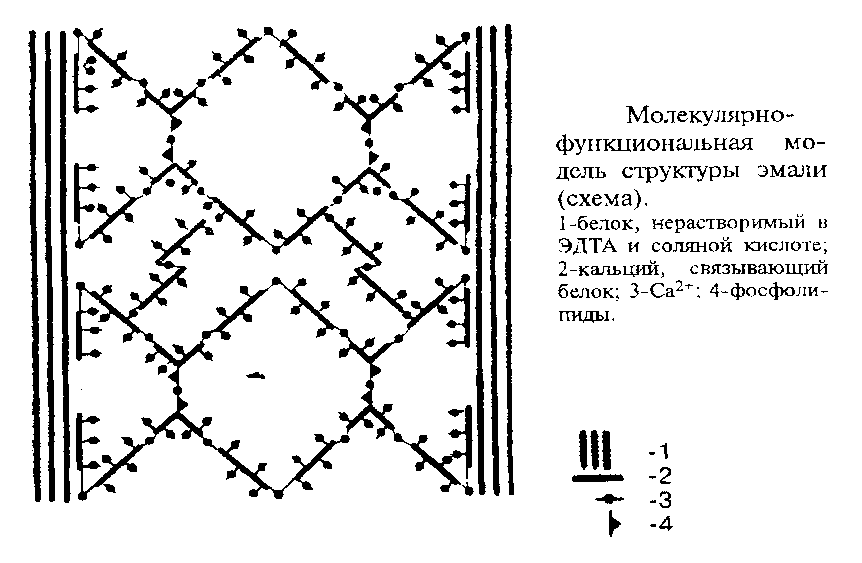
Субъединицы белка образуют особую трехмерную сетку из длинных перегородок, которые связаны между собой через одинаковые интервалы поперечными Са-мостиками. Центрами нуклеации являются именно эти перегородки благодаря наличию функциональных групп (фосфат фосфосерина и фосфолипидов, карбоксилы аспарагиновой и глутаминовой кислот и др.). Кристаллы формируются на перегородках с обеих сторон. Это обеспечивает их строго упорядоченное расположение, регулярность строения, прочность и другие свойства эмали. По мере завершения минерализации белковые перегородки все больше погружаются в кристаллы.
Таким образом, Са-связывающий белок и белок, нерастворимый в ЭДТА и НCl, ориентируют ход кристаллизации, обеспечивая упорядоченность эмали.
II. Белки эмали играют еще одну очень важную роль: белковая сеть, окружающая апатиты, предотвращает контакт апатитов с кислотами, смягчая их влияние и защищая кристаллы апатита от растворения.
В ранней стадии развития кариозного процесса (в стадии белого и пигментированного пятна) содержание белка в участке поражения возрастает в 3-4 раза. При этом пигментированное пятно в течение нескольких лет может не превращаться в кариозную полость, хотя в нём содержание Са и Р значительно снижено. Отсюда сделали вывод, что белок эмали действительно оказывает защитное действие, стабилизируя процесс деминерализации.
19




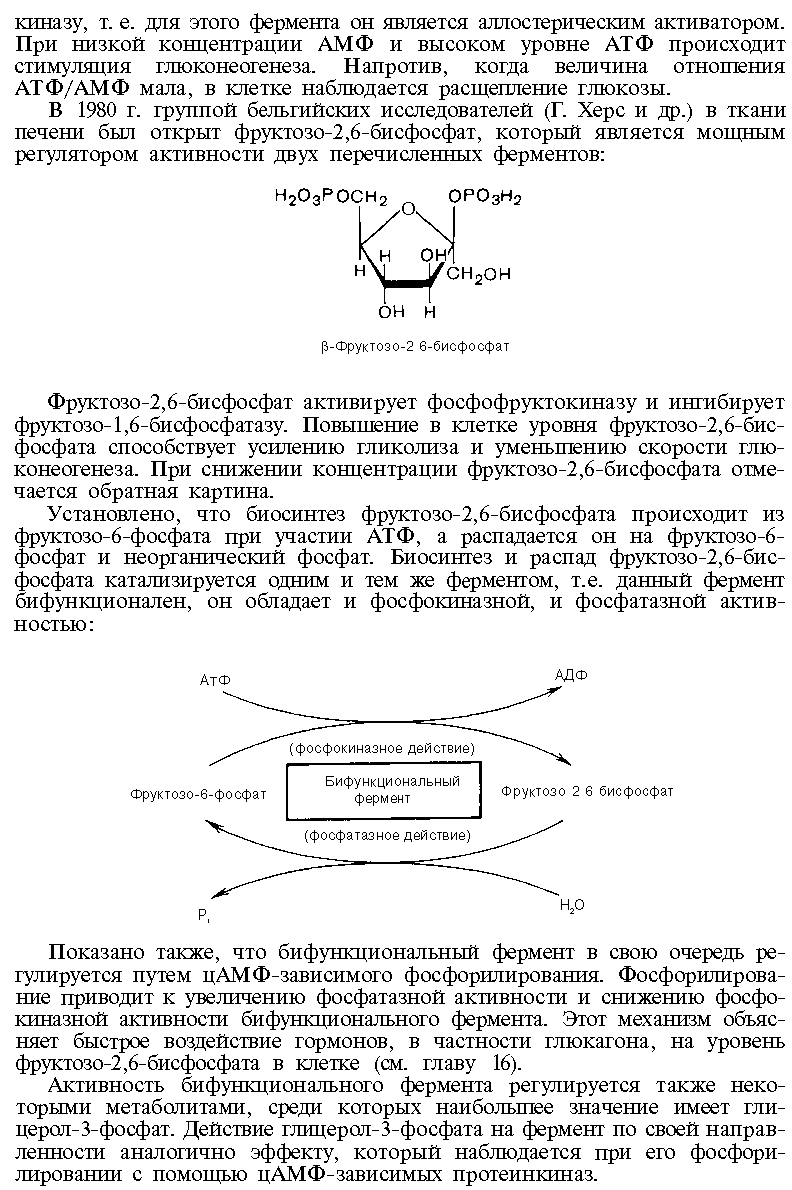
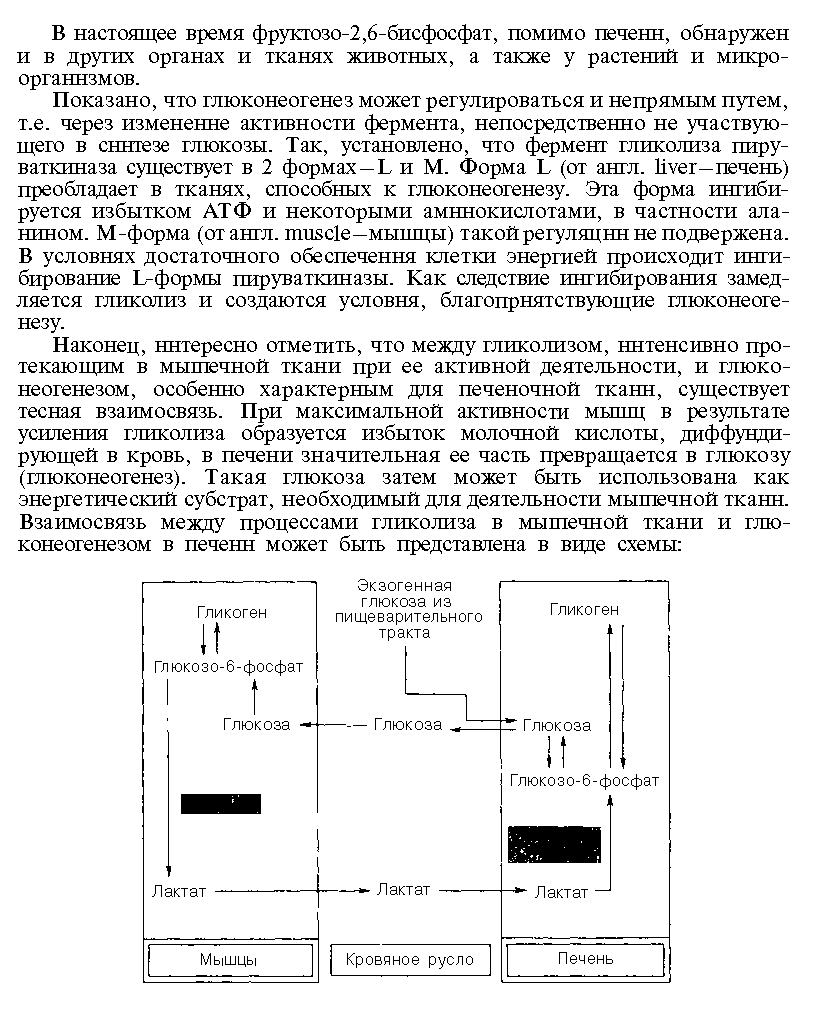
ЦИКЛ КОРИ
Метаболический груз работающей мышцы передается в печень, где соотношение НАДН/НАД+ ниже, чем в сокращающейся мышце
В мышцах нет Г-6-фосфатазы, поэтому гликоген, распада-ющийся в миоцитах, используют только они сами, т.к. фосфорилированная глюкоза не может выйти из клетки
Источники глюконеогенеза - только гликогенные аминокислоты
-
В пируват – ала, сер, цис, гли
Большинство аминокислот преобразуется в промежуточные продукты цикла Кребса:
-
В оксалоацетат или фумарат – асп, асн
-
В фумарат – 1) аминокислоты тир, фен, тре, вал, мет, иле, гли, про, арг, глу, глн, гис 2) жирные кислоты с чётным числом атомов С.
-
Анаплеротические – реакции для пополнения количества метаболитов ЦТК
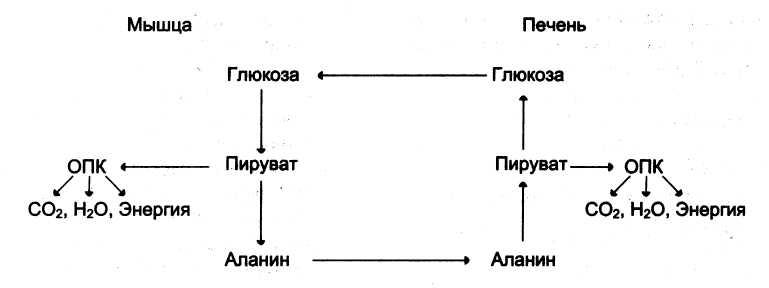
30% аминокислот, поступающих в печень – аланин. Биологический смысл глюкозо-аланинового цикла – транспорт аминного азота из мышц и предотвращение лактоацидоза
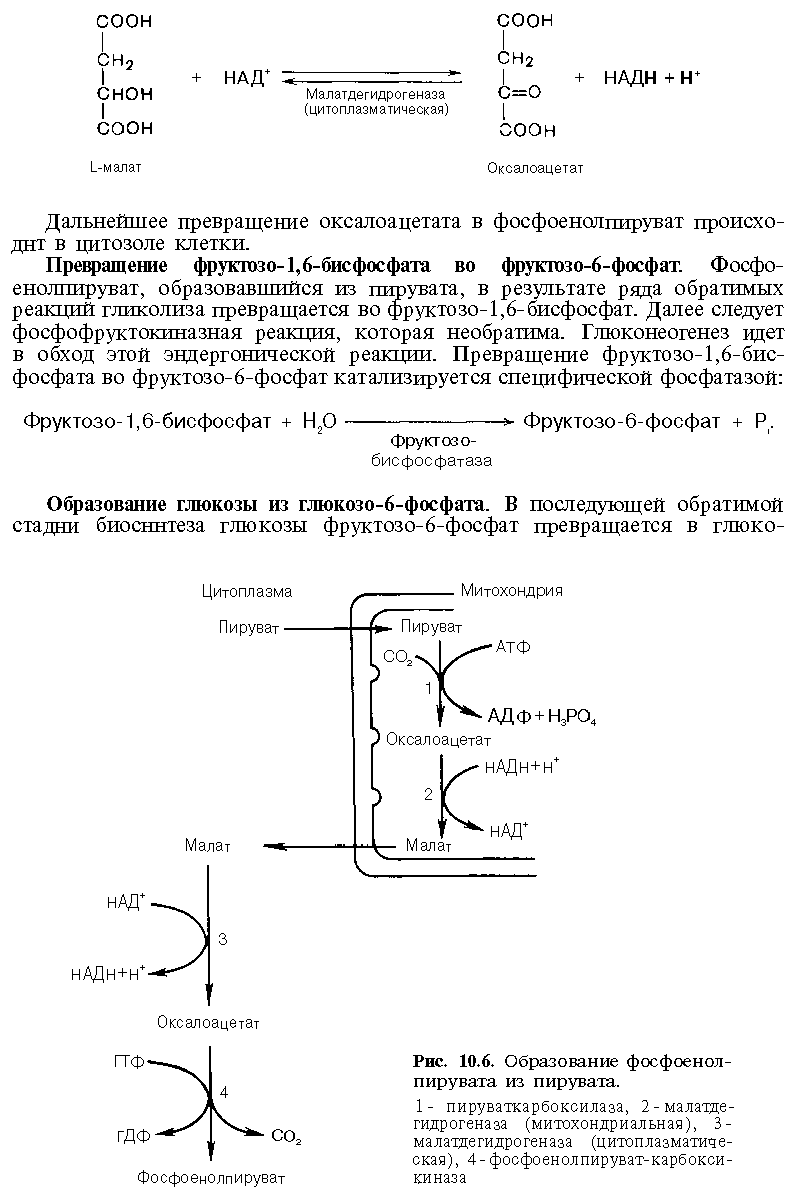
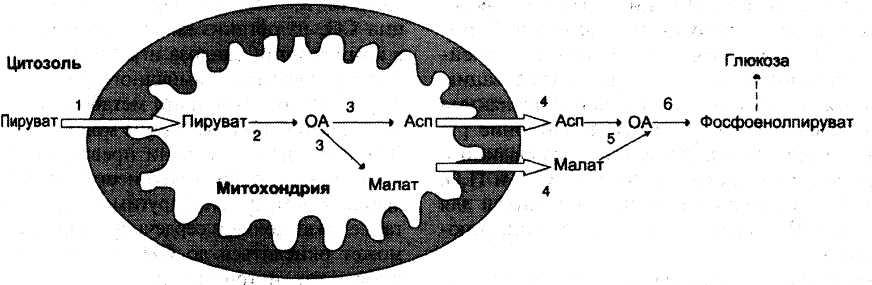
Стадии превращения пирувата в фосфоенолпируват
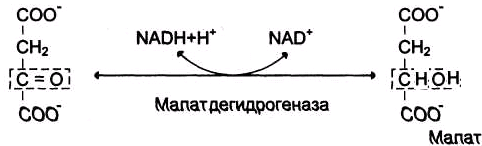
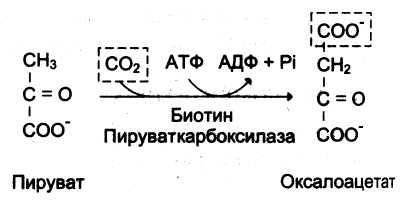 В
виде малататранспортируется
через мембрану митохондрии, а затем
снова преобразуется в оксалоацетат
В
виде малататранспортируется
через мембрану митохондрии, а затем
снова преобразуется в оксалоацетат
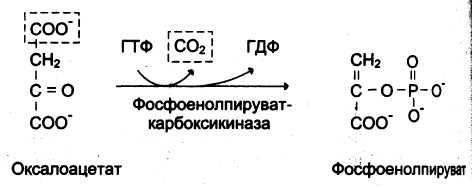
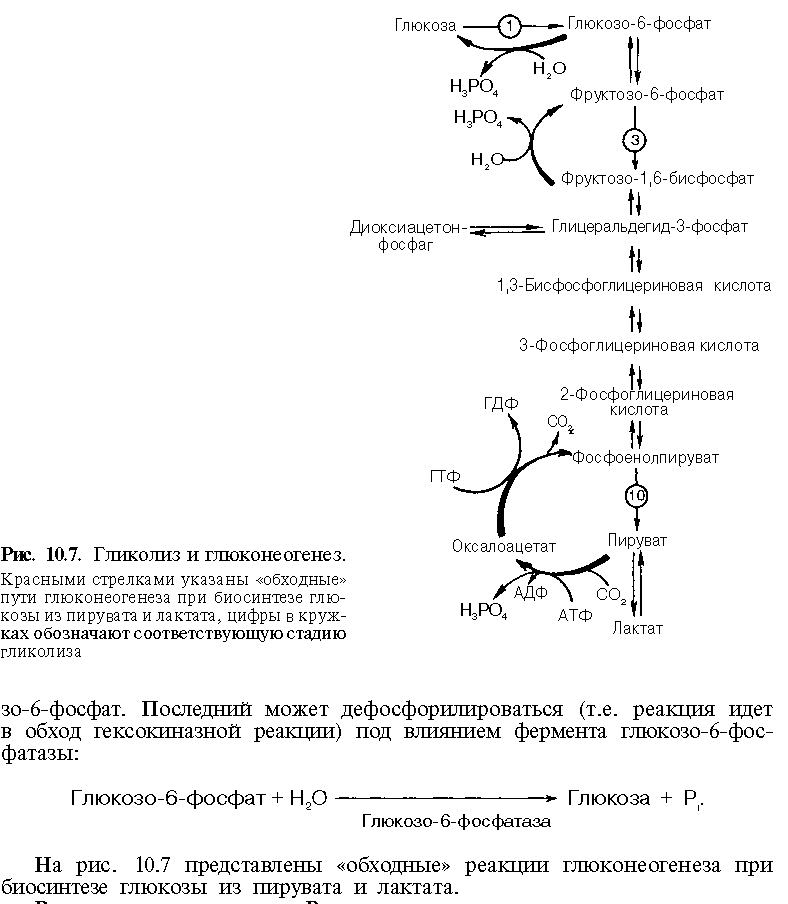
процесс ГНГ обратный гликолизу, но в местах 3-х необратимых реакций используются 4 обходных фермента:
Ферменты обходных реакций глюконеогенеза
4 Глюкозо-6-фосфатаза 3 Фруктозо-1,6-бифосфатаза
2 Фосфоэнолпируват- карбоксикиназа, ОА→ФЕП
1 Пируваткарбоксилаза, ПВК→ОА
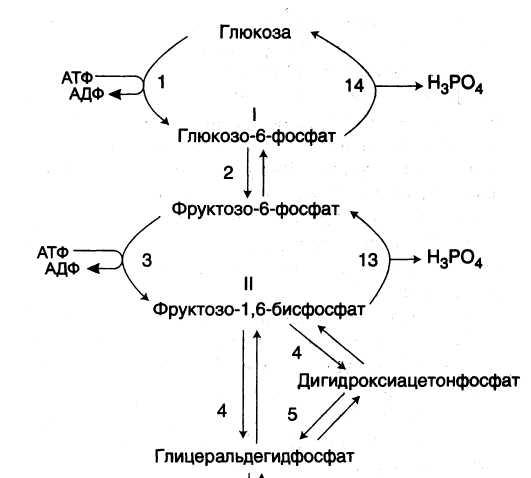
Синтез глюкозы в результате глюконеогенеза энергозависим При синтезе глюкозы из лактата расходуется энергия 4 АТФ и 2 ГТФ
лактат + лактат → 1 молекула глюкозы
• пируваткарбоксилаза – 2 АТФ,
• фосфоенолпируваткарбоксикиназа – 2 ГТФ
• на этапе обратимой киназной реакции гликолиза при глюконеогенезе идёт уже не образование, а расход АТФ – 2 АТФ
Таким образом – при низком содержании углеводов в пище, голодании, длительной физической работе – организм должен иметьвозможность получить глюкозу. Это достигается процессом глюконеогенеза.Кроме получения глюкозы, глюконеогенез обеспечивает и уборку "шлаков" – лактата, образованного при мышечной работе и в эритроцитах, и глицерола, являюще-
гося продуктом липолиза в жировой ткани
Глюконеогенез – синтез глюкозы de novo из неуглеводных компонентов. Протекает в печени и ≈10% в почках.
-
Предшественники для глюконеогенеза
-
лактат (главный),
-
глицерол (второй),
-
аминокислоты (третий) – в условиях длительного голодания.
-
Физиологическое значение.
Места поступления субстратов (предшественников) для глюконеогенеза
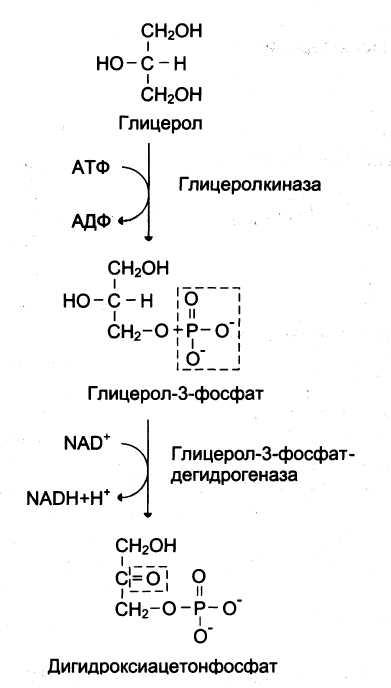
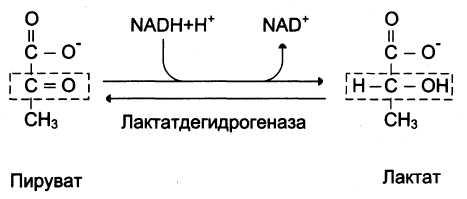
аланин Биологический смысл глюкозо-аланинового цикла – транспорт аминного азота из мышц и предотвращение лактоацидоза
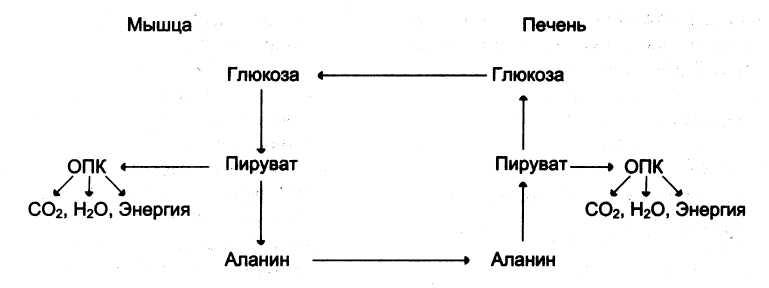
20. Пути образования и использования пировиноградной кислоты. Окислительное декарбоксилирование пирувата: последовательность реакций, связь с дыхатель¬ной цепью, регуляция, энергетический эффект. Метаболизм пирувата в реакциях трансаминирования и глюконеогенеза, биологическое значение этих процессов. Обмен пирувата и баланс витаминов. Характеристика тиамина и пантотеновой кислоты, их роль. Особенности метаболизма пирувата микрофлорой полости рта.
Пируват — важное химическое соединение в биохимии. Он является конечным продуктомметаболизма глюкозы в процессе гликолиза. Одна молекула глюкозы превращается при этом в две молекулы пировиноградной кислоты. Дальнейший метаболизм пировиноградной кислоты возможен двумя путями — аэробным и анаэробным. В условиях достаточного поступления кислорода, пировиноградная кислота превращается в ацетил-кофермент А, являющийся основным субстратом для серии реакций, известных как цикл Кребса, или дыхательный цикл, цикл трикарбоновых кислот. Пируват также может быть превращён в анаплеротической реакции в оксалоацетат. Если кислорода недостаточно, пировиноградная кислота подвергается анаэробному расщеплению с образованием молочной кислоты у животных и этанол[1] у растений.
