
- •Введение
- •Глава 1. Электрохимические устройства.
- •1.1. Классификация электрохимических устройств
- •1.2.Электроды
- •1.2.1. Монополярные электроды.
- •1.2.2. Катоды.
- •1.2.3. Биполярные электроды
- •1.3. Электродные контакты
- •1.4. Электролиты
- •1.5. Корпус электрохимической ячейки
- •1.6. Разделение электродных пространств
- •1.7.Электрическое подключение электродов, ячеек и электролизеров
- •1.8. Гидравлическое подключение электролизеров
- •1.9. Перемешивание электролита
1.8. Гидравлическое подключение электролизеров
Электролизеры и ячейки в них могут подключаться гидравлически последовательно (рис.1.13), или параллельно рис 1.14.
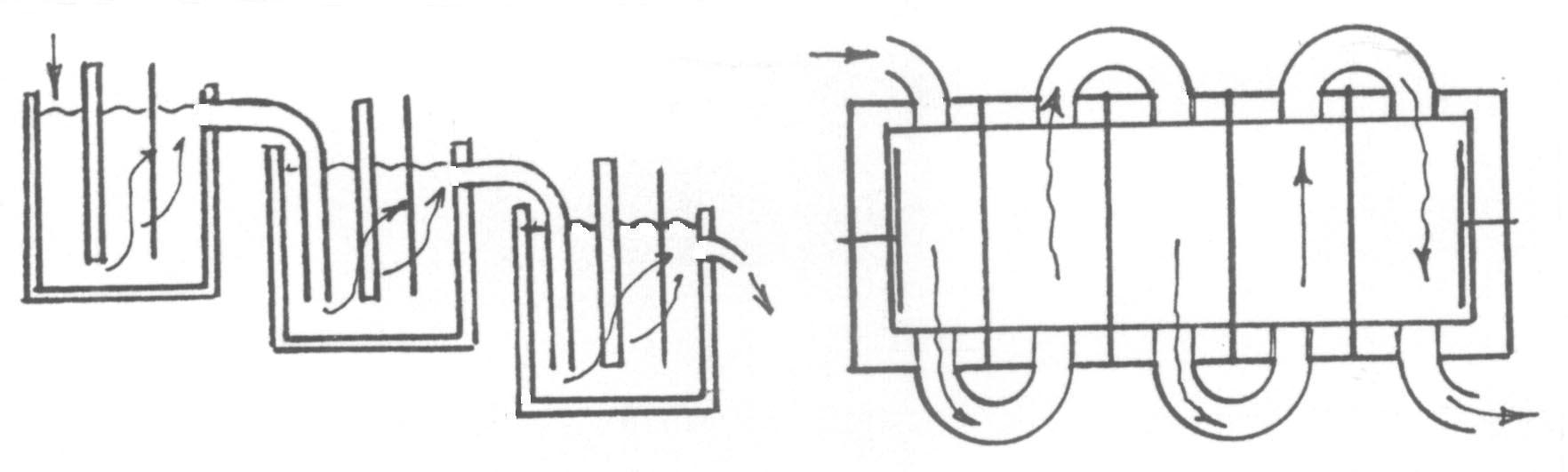
Рис.1.13. Схема последовательного питания электролитом электролизера с моно- и биполярными электродами.
При последовательном питании электролизеров проток стремятся организовать так, чтобы электролит подавался в нижнюю часть ванны, а отводился из ее верхней части, или наоборот. Такая схема циркуляции обеспечивает максимально равномерное распределение концентрации в ванне. Размещение электролизеров, обеспечивающих самопроизвольный последовательный проток электролита называется каскадом. Параллельное питание монополярных электродов чаще всего применяется при разделении электродных пространств диафрагмами и в электролизерах фильтр-прессной конструкции.
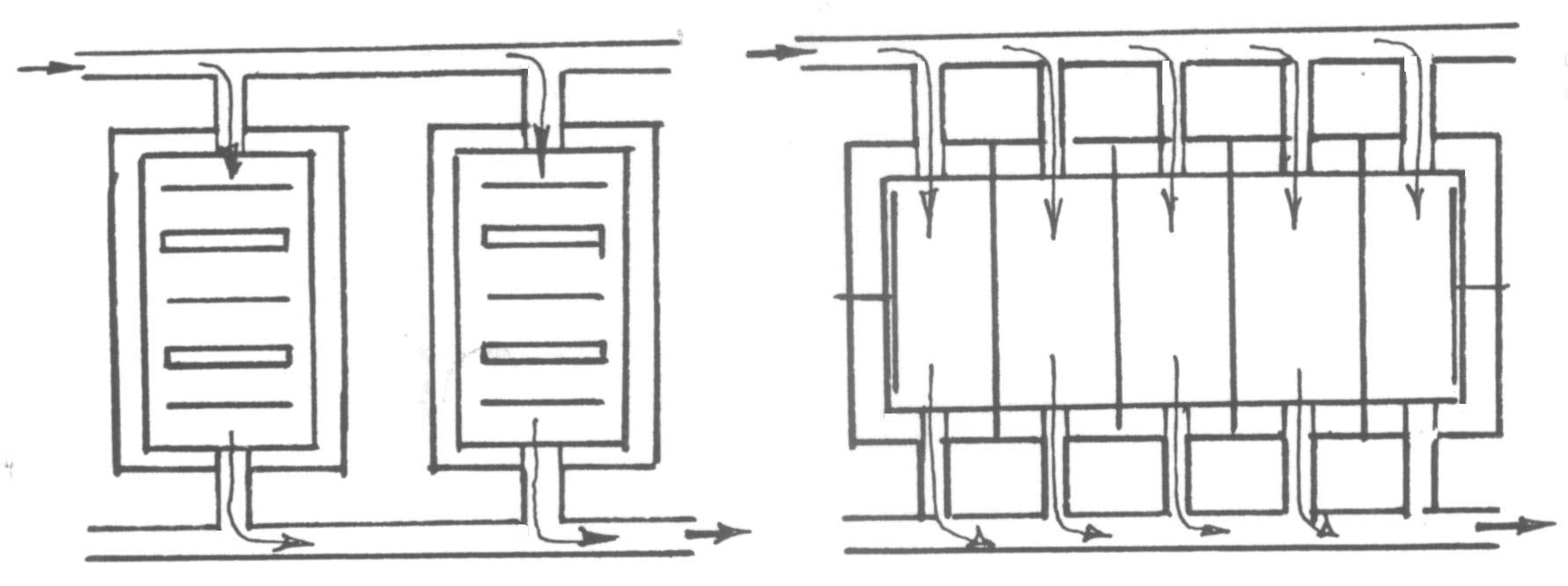
Рис.1.14. Схема параллельного питания электролитом электролизера с моно- и биполярными электродами.
Использование последовательного электрического подключения электродов и параллельного подключения ячеек по электролиту приводит к появлению токов утечки. Током утечки называется та часть тока, которая ответвляется от торцевых электродов в коллектор для подачи и отвода электролита, минует последовательно установленные электроды и не совершает полезной работы.
Величина токов утечки зависит от конструкции электролизера и может быть определена по закону Ома для параллельных проводников. В роли первого проводника выступает непосредственно электролизер. Ток в электролизере переносится от первого монополярного электрода через все последовательно расположенные биполярные электроды и слои электролита до концевого монополярного электрода. Сопротивление электролиза прохождению тока в данном случае равно сумме всех поляризационных и омических сопротивлений (рис.1.15).
Rэл-за = Rпол + Rом
Вторым проводником являются каналы для подвода электролита и отвода продуктов реакции. Их сопротивление зависит от длины пути тока l по питающим каналам и их поперечного сечения S:
Rканал = l/(S)
где - электропроводность электролита.
Соотношение тока электролиза и тока утечки можно оценить из закона Ома для параллельных цепей:
Uэл-ра = Iэл-за (Rпол + R ом) = Iут Rканал
![]()
Из полученного соотношения видно, что токи утечки возрастают с увеличением напряжения на электролизере (при увеличении числа последовательно соединенных электродов), и снижаются при уменьшении поперечного сечения каналов и увеличении из длины.

Рис.1.15. Эквивалентная электрическая схема электролизера с биполярными электродами и параллельным питанием электролитом.
R1 - поляризационные сопротивления, R2 - омические сопротивления электролита в электролизере, R3 - омические сопротивления электролита в перетоке, R4 - омические сопротивления электролита в питающем канале.
Основными задачами технолога-проектировщика является создание таких схем, при которых потери электроэнергии на производстве минимальны. То есть необходимо в максимальной степени уменьшить токи утечки, напряжение на ванне и обеспечить проведение процесса с максимальным выходом по току. Кроме того, необходимо рациональное размещение ванн в сериях и цехе в целом, сведение к минимуму длины ошиновки при объединении электролизеров в группы и серии. Это уменьшает не только потери электроэнергии, но и расход дорогостоящих цветных металлов, из которых изготовлены шины.
Уменьшение напряжения на каждом проектируемом электролизере возможно при увеличении электропроводности раствора, уменьшении поляризационных сопротивлений и падения напряжения в контактах и ошиновке.
Простых решений для удовлетворения выше перечисленных требований не существует, необходимо искать компромиссные решения по каждому пункту. Например:
-
увеличение электропроводности электролита возможно при увеличении его концентрации. Но увеличение концентрации электролита может привести к ускоренному разложению продуктов реакции, уменьшению выхода по току и увеличению, а не уменьшению энергозатрат (получение H2S2O8);
-
увеличение электропроводности возможно при использовании веществ с большей подвижностью ионов. Но эти альтернативные электролиты могут быть более дороги сами по себе (КОН более электропроводен, но и более дорог, чем NaOH);
-
существенно повысить электропроводность электролита можно введением электропроводных добавок (кислоты, щелочи или соли). Однако подкисление электролита увеличивает возможность выделения на катоде водорода, а подщелачивание - гидролиза солей с образованием нерастворимых гидроксидов (гидроэлектрометаллургия).
-
уменьшению межэлектродного расстояния и снижению омического падения напряжения в электролите могут препятствовать увеличение газонаполнения электролита, необходимость размещения диафрагм или экранов между электродами, периодического извлечения электродов (рафинирование меди и никеля) и т.п.
-
уменьшение поляризационных сопротивлений достигается оптимальным составом электролита и использованием катализаторов - специальных электродных покрытий. Однако, чем больше активность катализатора, тем меньше срок его службы. В ряде случаев применение электродов с активным слоем вообще невозможно (гидрометаллургия). Уменьшению поляризационных сопротивлений способствует также увеличение температуры. Но с ростом температуры увеличивается испарение, энергозатраты на нагрев и требуется определение температурного оптимума расчетом каждого варианта;
-
уменьшению падения напряжения в шинах способствует увеличение их поперечного сечения. Но это же вызывает большой расход на ошиновку цветных металлов, стоимость которых ложится на себестоимость производимой продукции.
