
- •Введение
- •Глава 1. Электрохимические устройства.
- •1.1. Классификация электрохимических устройств
- •1.2.Электроды
- •1.2.1. Монополярные электроды.
- •1.2.2. Катоды.
- •1.2.3. Биполярные электроды
- •1.3. Электродные контакты
- •1.4. Электролиты
- •1.5. Корпус электрохимической ячейки
- •1.6. Разделение электродных пространств
- •1.7.Электрическое подключение электродов, ячеек и электролизеров
- •1.8. Гидравлическое подключение электролизеров
- •1.9. Перемешивание электролита
Глава 1. Электрохимические устройства.
НАЗНАЧЕНИЕ И ОБЩИЕ ЭЛЕМЕНТЫ КОНСТРУКЦИИ [9-12 ]
1.1. Классификация электрохимических устройств
Все электрохимические устройства предназначены для превращения химической энергии в электрическую или наоборот, электрической в химическую. В зависимости от направления превращения они делятся на химические источники тока и электролизеры.
По назначению электрохимические устройства можно условно разделить на несколько классов:
-химические источники тока (ХИТ);
-электрохимические реакторы (электролизеры);
-электрохимические преобразователи информации;
-электрохимические станки;
-гальванические ванны.
В химических источниках тока протекают окислительно-восстановительные реакции, в результате которых из исходных веществ с большим запасом энергии (G) образуются продукты, запас энергии которых значительно меньше. Разница запаса энергий выделяется в виде электрической энергии (целевой продукт) и тепла (потери полезной энергии).
Электролизеры - это электрохимические устройства, предназначенные для превращения электрической энергии в химическую. Подведенная к электролизеру электрическая энергия преобразуется и накапливается в нем за счет образования продуктов реакции, у которых запас энергии (G) больше, чем у исходных веществ. Можно сказать, что электролизеры используются для получения товарной продукции путем электрохимического синтеза неорганических и органических твердых, жидких или газообразных веществ.
Электрохимические преобразователи информации предназначены для контроля за величиной отдельных параметров (состав, концентрация, скорость движения и др.) газовой или жидкой среды, в которую помещен преобразователь. Скорость протекающей в преобразователе электрохимической реакции (плотность и сила тока) или величина потенциала электрода зависит от величины выбранного для контроля параметра. Изменение указанного параметра приводит к пропорциональному изменению величины выходного сигнала (ток, напряжение), регистрируемых вторичным прибором. То есть, продукцией преобразователей является научная информация.
Электрохимические станки используются для локального анодного растворения металла с целью придания детали необходимой конфигурации и размера. Использование этого метода целесообразно при обработке очень твердых сплавов и формировании в деталях отверстий сложного профиля. Таким образом, задачей электрохимической размерной обработки материала является высокоскоростной контролируемый съём металла.
Гальванические ванны применяются для обработки деталей с целью нанесения на их поверхность тонкой пленки (от нескольких микрон до нескольких десятков микрон) металла или неметалла с целью придания обрабатываемому изделию декоративного вида, повышенной коррозионной стойкости и других свойств.
По способу превращения энергии и направлению протекающих реакций многие электрохимические устройства отвечают признакам как ХИТ, так и электролизеров. Так, в электрохимических станках реакции протекают в сторону образования веществ с меньшим запасом энергии, как в ХИТ:
Feo - 2e = Fe2+
Однако задачей этих устройств не является получение электроэнергии. Напротив, электроэнергия к ним подводится (как в электролизерах) для ускорения процесса растворения металла (формообразования).
В гальванических ваннах большинство процессов протекает при подводе электрического тока, в сторону увеличения запаса энергии продуктов реакции:
Zn2+ + 2e = Zno
Однако имеются процессы, например, оксидирование и эматалирование алюминия, в которых эти реакции протекают в сторону уменьшения запаса энергии, как в химических источниках тока. Электроэнергия к системе подводится (как в электролизере) для получения оксидной пленки с заданными характеристиками.
Несмотря на большое разнообразие электрохимических устройств, все они имеют ряд общих признаков. Общими признаками всех электрохимических систем является обязательное наличие двух электродов - проводников первого рода и электролита между ними - проводника второго рода, помещенных в общий корпус. Система из двух электродов, электролита и общего корпуса называется электрохимической ячейкой, рис. 1.1, А.
Если для предотвращения взаимодействия продуктов реакции электродные пространства разделяются одной или несколькими перегородками с ионной проводимостью, то такая ячейка становится двухкамерной (рис. 1.1, Б) или многокамерной (рис. 1.1, В). Двухкамерные ячейки являются основой электролизеров для электролиза воды, многокамерные - электродиализаторов для очистки или опреснения воды.
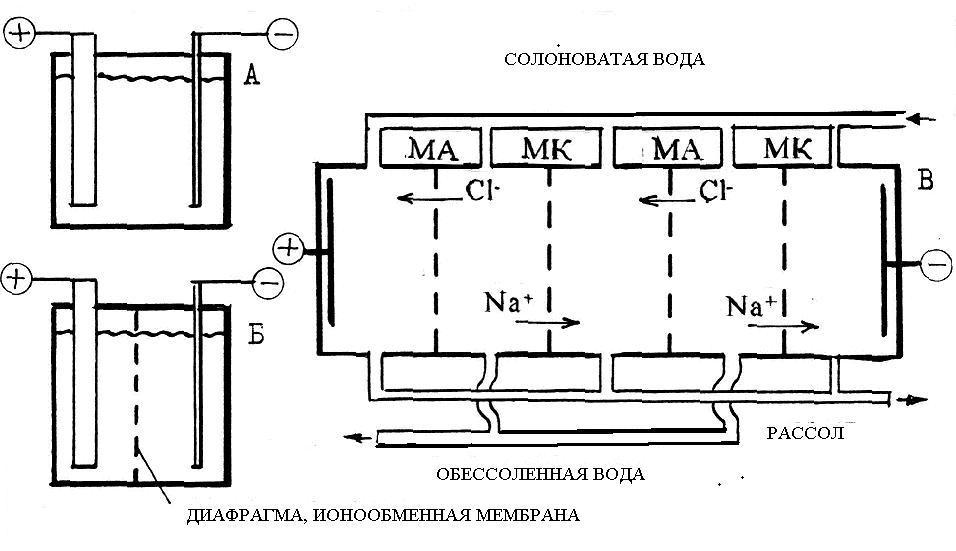
Рис.1.1. Типы электрохимических ячеек .
А - однокамерная, Б - двухкамерная, В - многокамерная.
Рассмотрим более подробно эти составляющие электрохимической ячейки.
