- •Федеральное агентство по образованию
- •Содержание
- •Тема 2: Алканы. Циклоалканы
- •Тема 3: Непредельные углеводороды: алкены, алкадиены, алкины
- •Тема 4: Ароматические углеводороды
- •Тема 5: Галогенпроизводные. Спирты. Фенолы. Простые эфиры
- •Тема 6: Азот- и карбонилсодержащие
- •Тема 7: Карбоновые кислоты и их производные
- •Тема 8: Углеводы. Аминокислоты и белки. Гетероциклы
Федеральное агентство по образованию
ГОУ ВПО «Алтайский государственный университет»
Химический факультет
Кафедра органической химии
Задачи и упражнения по органической химии
учебно-методическое пособие
|
|
|
|
Барнаул 2008
УДК 547(076.5)
ББК 24.2я 73-5
З 691
Задачи и упражнения по органической химии : учебно-методическое пособие / И. Б. Катраков. – Барнаул : Изд-во Алт. ун-та, 2008. – 28 с.
Составитель: кандидат химических наук, доцент И. Б. Катраков
Учебное пособие содержат вопросы и задачи для решения на семинарских занятиях по курсу «Органическая химия» для студентов, обучающихся по специальности 280101 – Безопасность жизнедеятельности в техносфере.
ISBN5-7904-0498-7
Рекомендовано к изданию химическим факультетом АлтГУ.
Пособие размещено в Интернете на сайте химического факультета АлтГУ: http://www.chem.asu.ru/
ISBN5-7904-0498-7Катраков И.Б., 2008
Издательство Алтайского государственного университета, 2008
Содержание
Тема 1: Теоретические основы органической химии 4
Тема 2: Алканы. Циклоалканы 8
Тема 3: Непредельные углеводороды: алкены, алкадиены, алкины 11
Тема 4: Ароматические углеводороды 14
Тема 5: Галогенпроизводные. Спирты. Фенолы. Простые эфиры 17
Тема 6: Азот- и карбонилсодержащие 20
Тема 7: Карбоновые кислоты и их производные 24
Тема 8: Углеводы. Аминокислоты и белки. Гетероциклы 27
Тема 1: Теоретические основы органической химии
Термины и понятия
Акцептор
Валентность
Валентный угол
Водородная связь
Геометрия молекулы
Гибридизация
Гомологи
Гомологический ряд
Длина связи
Донор
Заместитель
Изомер
Изомерия
Индуктивный эффект
Карбанион
Крбокатион
Ковалентная связь
Мезомерный эффект
Механизм реакции
Молекула
Номенклатура
Нуклеофил
Орбиталь
Органическая химия
Полярность связи
Поляризуемость
Реагент
Реакция замещения
Реакция присоединения
Реакция элиминирования
Свободный радикал
σ-Связь
π-Связь
Структурная формула
Субстрат
Функциональная группа
Химическая связь
Химическое строение
Электроотрицательность
Электрофил
Энергия активации
Энергия связи
Упражнения
1. Определите валентные углы и гибридизацию каждого атома углерода в молекулах:
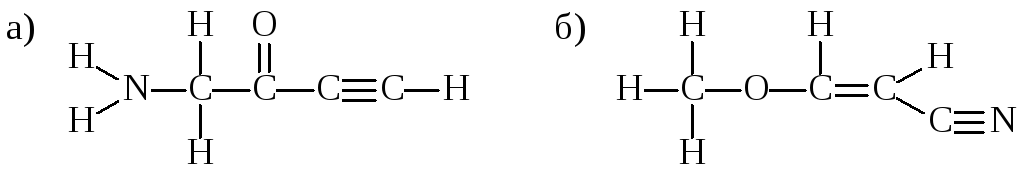
2. Напишите сокращенные структурные формулы и схематичные изображения следующих веществ:

3. Напишите структурную формулу веществ, схематически изображенных ниже:

4. Какие из структур изображены с ошибками? Какие именно ошибки допущены?
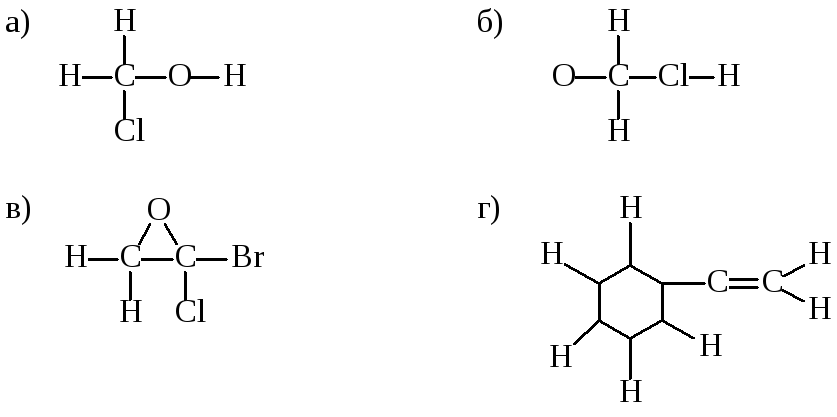
5. Определите, полярны или неполярны, и почему, следующие связи:
а) C–O; б)C–C; в)N–H; г)C–Cl.
6. Какие функциональные группы имеют полярные связи? В каких группах нет таких связей?
7. Изобразите все изомеры состава C6H14.
8. Изобразите все изомеры состава C3H8О.
9. Определите функциональные группы и классы, к которым принадлежат следующие соединения:
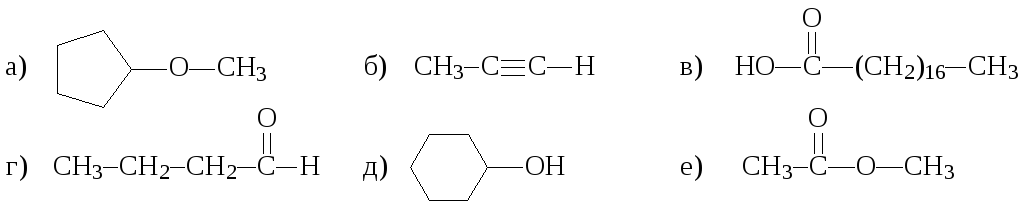
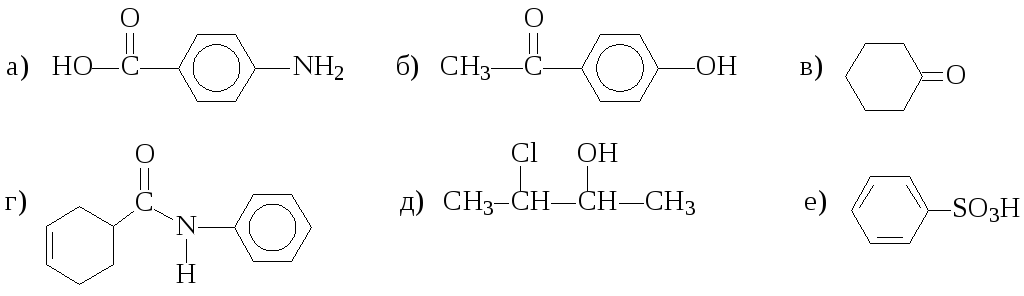
10. Какие функциональные группы имеются в молекулах соединений:
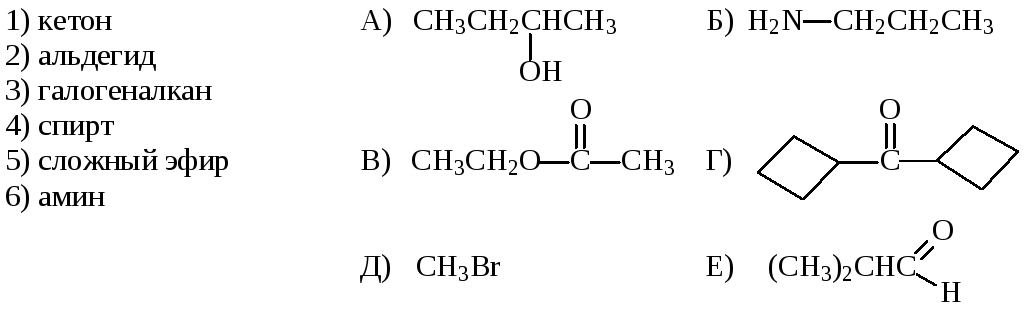
11. Укажите соответствие между классом соединения и структурной формулой:
12. Перечислите классы органических веществ, в которых входят:
б) азот; б) кислород.
13. Какие из перечисленных характеристик будут одинаковыми для двух изомеров?
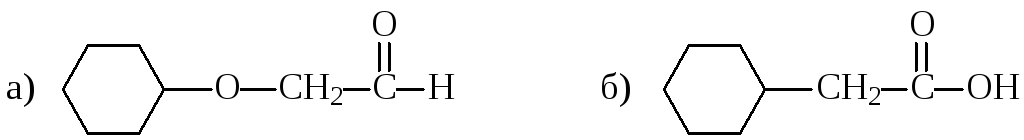
а) молекулярная масса; б) реакционная способность по отношению к гидроксиду натрия; в) молекулярная масса; г) растворимость в воде; д) токсичность для человека; е) температура плавления.
Основывайте свой ответ на Ваших знаниях об общих свойствах изомеров.
14. Составьте структурные формулы веществ (в некоторых случаях может быть несколько правильных ответов):
а) алкан C4H10; б) алкинC4H6; в) альдегидC4H8O;
г) простой эфир C4H10O; д) амидC3H7NO; е) сложный эфирC3H6O2.
15. Какие из пар соединений являются изомерами?
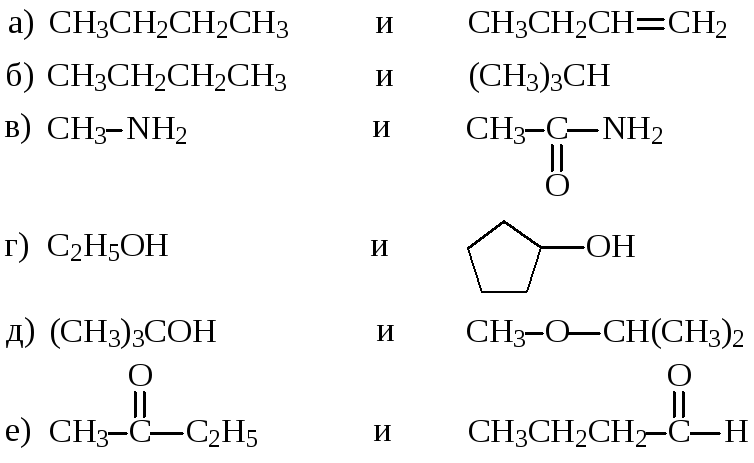
В каких случаях оба соединения принадлежат одному классу?
16. Приведите примеры гомолитического и гетеролитического разрыва связей в соединениях:
а) CH4; б)CH3Cl; в)CH3Li.
17. Расположите приведенные связи в ряд по возрастанию их способности к гетеролитическому разрыву:
а) C–I; б)C–Cl; в)C–Br; г)C–F.
18. Классифицируйте нижеприведенные реагенты по группам – радикалы, нуклеофилы, электрофилы: :NH3,CN–,NO2+,OH–,RCOO–,Br–,Br2(hν),AlCl3,Cl–, (CH3)3C·,H2O,H2O2.
19. Укажите графически распределение электронной плотности в нижеприведенных соединениях. Назовите все присутствующие эффекты.
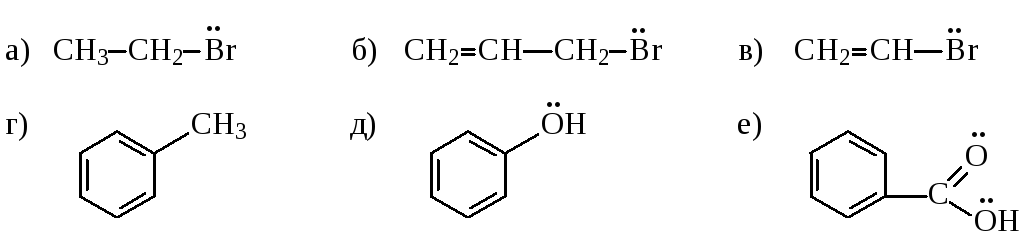
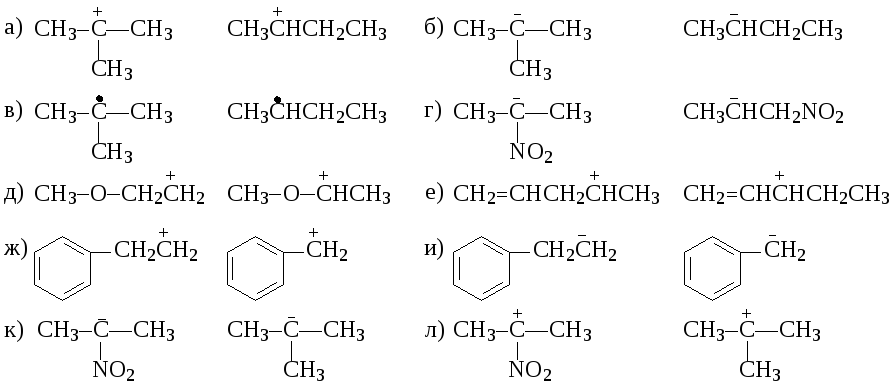
20. Знаками больше / меньше (< / >), укажите относительную устойчивость частиц в нижеприведенных парах.
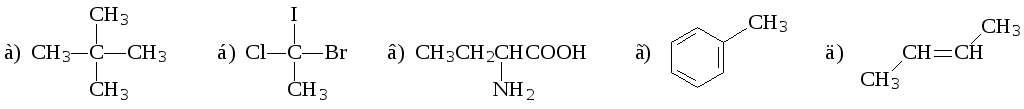
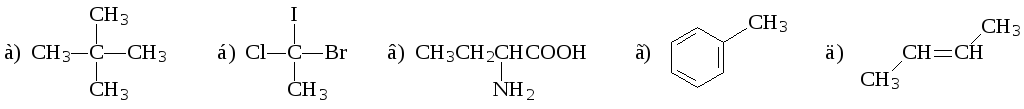
21. В нижеприведенных соединениях отметьте (*) хиральный атом углерода (если он есть!):
22. Расположите следующие группы в порядке уменьшения их старшинства в системе Канна–Ингольда–Прелога:
а) –OH, –Cl, –CHO;
б) –F, –Cl, –Br, –I;
в) –CH3, –CH2–CH3, –C(CH3)3.
23. Определите абсолютную конфигурацию хирального атома углерода в нижеприведенных соединениях: