
Text_lektsiy_z_TTD_chastina_1__3-y_sem_ukr_2015
.pdf
Лекция №10 |
61 |
Лекція №10 |
Дата: |
|
2.4 ЗАСТОСУВАННЯ ПЕРШОГО ЗАКОНУ ДЛЯ СТАЦІОНАРНИХ ПОТОКОВИХ ПРОЦЕ-
СІВ ДО КРУГОВИХ ПРОЦЕСІВ ( ЦИКЛІВ)
Цикл - це сукупність розімкнених процесів. Для кожного і -го процесу (і = 1, 2, . n - число розімкнених процесів в циклі) можна записати:
& |
= |
& |
+ |
& |
+ N тех i |
Qi |
H i |
K i |
т.ч. можна записати подібне рівняння для кожного розімкненого процесу, тобто n рівнянь. Підсумовуємо, ліві і праві частини цих рівнянь, тоді для циклу отримаємо:
|
|
|
|
|
|
|
|
0 |
|
|
0 |
|
|
|
|
|
||
|
|
|
|
|
|
& |
|
& |
|
|
|
|
& |
∑ N тех i |
||||
|
|
|
|
|
∑ Qi = ∑ |
H i + ∑ |
|
|
K i + |
|||||||||
|
|
|
|
|
|
властивості параметрів стану |
||||||||||||
|
|
|
|
|
& |
= ∑ N тех i |
– Перший закон для циклів |
|||||||||||
|
|
|
|
∑ Qi |
||||||||||||||
|
|
|
|
|
|
& |
& |
|
|
|
|
|
& |
|
|
|||
|
|
|
|
|
|
|
|
& |
|
|
|
|
||||||
|
|
|
|
|
|
∑Qi = Qп − |
Qв |
|
|
= Qц |
||||||||
|
|
|
|
|
|
∑ N тех ,i |
= N техв |
|
|
|
= N ц |
|||||||
|
|
|
|
|
|
− |
N техп |
|
||||||||||
& |
|
– сумарна кількість теплоти, в одиницю часу що підводиться до РТ |
||||||||||||||||
Qп |
||||||||||||||||||
|
від зовнішнього джерела; |
|
|
|
|
|
|
|
|
|
|
|
||||||
& |
|
– сумарна кількість теплоти в одиницю часу що відводиться від РТ |
||||||||||||||||
Qв |
||||||||||||||||||
|
до зовнішнього джерела |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
& |
– алгебраїчна сума теплот (+,-,0); в одиницю часу за цикл (теплових |
||||||||||||||||
∑ Qi |
||||||||||||||||||
|
потоків); |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
& |
|
– теплова потужність циклу (теплота циклу в одиницю часу). |
||||||||||||||||
Qц |
||||||||||||||||||
∑N тех, i |
- алгебраїчна сума технічних потужностей (робіт в одиницю часу) |
|||||||||||||||||
|
за цикл. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
N |
в |
- сумарна технічна потужність (сумарна робота), що відводиться в |
||||||||||||||||
|
тех |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
циклі від робочого тіла (РТ); |
|
|
|
|
|
|
|
|
|||||||||
N |
п |
- сумарна технічна потужність, що підводиться в циклі до РТ; |
||||||||||||||||
|
тех |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N ц |
- сумарна потужність циклу. |
|
|
|
|
|
|
|
|
|||||||||
Тоді: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
& |
|
& |
в |
|
|
п |
= |
N ц |
|
|
(4а) |
||||
|
|
|
Qп − |
Qв |
= N тех − |
|
N тех |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Перший закон термодинаміки для циклів через технічну потужність (техн. роботу) (4а) показує, як РТ здійснюючий цикл обмінюється енергією із зовні-
шнім середовищем.
ТТД (3-й семестр) |
2015 р. |

Лекция №10 |
62 |
У рівняння входять лише величини, що характеризують енергообмін РТ із зовнішнім середовищем!!!
|
|
|
У складних циклах може бути внутрішній теплообмін між |
|
|
||
|
Q/ |
|
потоками РТ: у одному з процесів теплота відводиться, в |
|
|
іншому підводиться усередині циклу ( Q / = −Q / / з урахуван- |
|
|
|
||
Q// |
|
ням правила знаків). |
|
|
При підсумовуванні (для циклу) теплоти внутрішнього теп- |
||
|
|
|
|
|
|
|
лообміну скорочуються. |
& |
|
Якщо (4а) розділити на m [кг/с] – витрата РТ в циклі, то: |
|
qп − qв = lтехв − lтехп = lц |
(4б) |
Перший закон термодинаміки для циклів через технічну роботу в пито-
мих величинах
Рівняння (4) можна отримати, використовуючи узагальнену форму енергобалансу (3б), при цьому треба врахувати, що зміна енергії потоку речовини за цикл дорівнює 0 ( Епр = 0 ) (властивість параметрів стану)
Qподв |
|
|
Q |
|
|
|
|
|
|
|
|
& |
|
п |
& |
|
в |
||||
|
|
|
|
отв |
|
|
||||
|
|
|
|
|
Qп |
+ N |
тех |
= Qв |
+ N |
тех |
|
|
|
|
|
||||||
N техподв |
Цикл |
|
N техотв |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
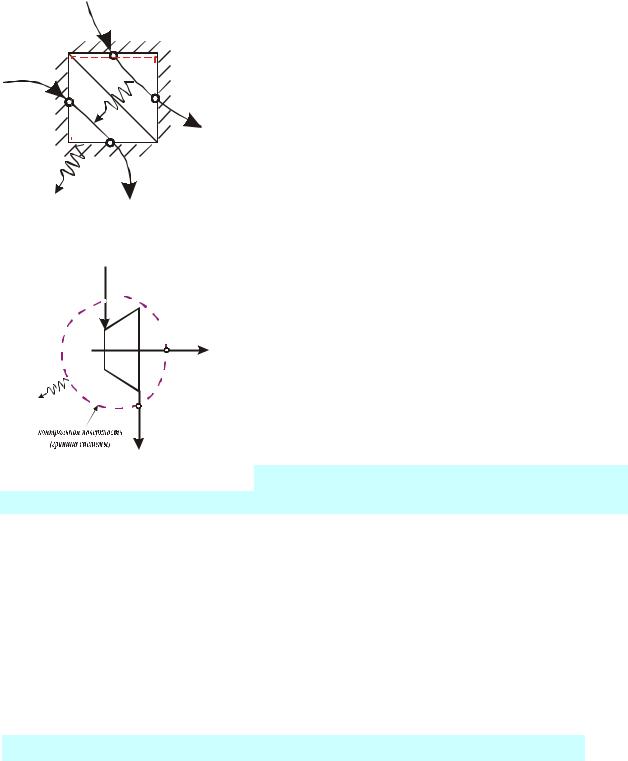
а) Прямі цикли - по ним працюють теплові двигуни
|
Qподв |
Схема Е/Б |
|
|
|
|
|
|
N подв |
N отв |
Схема показує як РТ, що здійснює прямий цикл |
тех |
тех |
|
|
|
обмінюється енергією із зовнішнім середовищем. |
|
Qотв |
|
|
|
|
|
|
Призначення прямих циклів - перетворення теплоти, що отримана за рахунок використання енергоресурсів (нафта, газ, вугілля), в корисну роботу циклу.
Особливості прямого циклу:
N техв − N техп = N ц > 0 - тоді з (4а)
ТТД (3-й семестр) |
2015 р. |

Лекция №10 |
63 |
& |
> |
|
& |
|
|
|
|||
Qп |
|
Qв |
|
|
|
|
|
|
|
N ц - корисна потужність (робота циклу) передається споживачеві. Є
продукцією циклу (тобто «користь»). «Користь» визначається призначенням, а «витрата» - це те що ми витрачаємо для здобуття даної «користі».
& - витрата на реалізацію циклу (використовуються енергоресурси).
Qп
|
|
|
|
|
|
|
|
.Т.ч. ще раз!!! |
& |
− |
& |
= N |
в |
− |
N |
п |
= N ц > 0 І -й закон для прямих циклів |
Qп |
Qв |
тех |
тех |
|||||
затрата |
|
|
|
|
|
польза |
||
|
|
|
|
|
|
|
|
|
Користь N ц визначається двома способами:
а) як алгебраїчна сумма технічних потужностей (робіт)
N техв − N техп = N ц > 0
б) як алгебраїчна сумма теплових потоків за цикл (теплот)
& |
− |
& |
= N ц > 0 |
Qп |
Qв |
І-й закон для прямих циклів широко використовується при аналізі циклу.
Рівнянню відповідає схема Е/Б:
Qподв |
|
|
|
|
|
|
& |
в ко- |
|
Nц |
Для оцінки ефективності перетворення теплоти Qп |
|||
рисну роботу |
N ц > 0 вводять тепломеханічний коефіці- |
|||
|
||||
єнт (ТМК).
 Qотв
Qотв
Використовуючи перший закон:
(етта) η = |
користь |
= |
N |
ц |
= |
lц |
< 1 |
- |
завжди |
|
|
|
|
|
|||||||
витрата |
Qп |
qп |
||||||||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
(тільки для прямих циклів)
Те що η < 1 завжди - буде доведено при вивченні 2-го Закону. Оскільки η < 1,
& |
перетворюється на корисну роботу (техніч- |
то η показує, яка частина від Qподв |
ну потужність). З цього місця матеріал наданий для студентів як СРС до Лекції
б) Зворотні цикли - по ним працюють ХУ, ТНУ.
Для них справедливе рівняння (4а), а схеми Е/Б представлена у вигляді:
|
|
|
Qотв |
|
|
|
Qотв |
|
|
|
|
|
|
||
|
|
|
|
|
|
||
N техотв |
|
|
N техподв |
|
|
|
NЦ |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
або |
|||
|
|
|
Qподв |
|
|
|
Qподв |
|
|
|
|
|
|
||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ТТД (3-й семестр) |
2015 р. |

|
|
|
|
|
|
|
Лекция №10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
64 |
|
|
Схема відображає особливості зворотних циклів. З схеми можна отримати рів- |
|||||||||||||||||||
|
|
няння (4а) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
У зворотних циклах Nц |
< 0, тобто | N техп |
| > N техв |
(це означає, що Nц по- |
||||||||||||||||
|
|
винне підводитися із зовнішнього середовища з метою реалізації циклу, тобто |
|||||||||||||||||||
|
|
витрачається |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Оскільки Nц < 0, то |Qв| > |Qп| |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
На практиці зручно розглядати | Nц | (т.е >0) |
тоді (4а) записується у вигляді: |
||||||||||||||||||
|
|
|
|
|Q | - Q = | N п |
| - N в |
= | N | |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
в |
п |
тех |
тех |
|
ц |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Часто 1-й закон використовується для зворотних циклів у вигляді: |
|
|
|||||||||||||||||
|
|
|Qв| - Qп |
= | Nц | |
- цьому рівнянню відповідає схема: |
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
Qотв |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Nц |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Qподв |
ХУ и ТНУ (зворотні цикли) |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
Схема Е/Б |
|
Призначення |
|
|
|
Ефективність |
|
|
|
|
|
||||||||
|
|
|
|
|
- вироблення теплоти |
QГ - опалювальна потужність (тепло- |
|||||||||||||||
|
|
|
|
|
для цілей теплопоста- |
продуктивність) |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
чання |
|
|
|
|
Ефективність циклу теплонасосної |
|||||||||||
|
|
|
|
|
|
|
|
|
установки на базі 1-го закону ТТД оці- |
||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
нюється: |
|
|
|
|
|
|
|
|
|
|
|
TГ |
>T0 |
QГ- “польза” |
|
|
|
|
|
|
Опалювальним коефіцієнтом: |
||||||||||||
|
|
|
|
|
|
|
|
користь |
|
& |
|
|
|
q |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
Q |
Г |
|
г |
|
|||||||
|
|
N - “затрата” |
|
|
|
|
|
ϕ = |
|
= |
|
= |
|
|
|
> 1 |
|||||
ТНУ |
|
|
|
|
|
|
|
|
|
|
lц |
||||||||||
|
|
|
|
|
|
|
|
витрата |
N |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
ц |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
QХ=Q0 |
|
|
|
|
|
|
|
|
завжди |
|
|
|
|
|
|
|
|
|
|
|
|
TХ =T0 |
T0-тем-ра окруж. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
TГ=T0 |
|
природной среды– |
- знизити температуру |
Qx - холодильна потужність (холодо- |
|||||||||||||||||
QГ=Q0 |
|
|
|||||||||||||||||||
|
|
|
|
системи (об'єкту) до |
продуктивність) |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
N - “затрата” |
Ефективність циклу холодильної уста- |
||||||||||||||||||
|
|
заданого рівня (нижче |
|||||||||||||||||||
ХУ |
|
|
|
||||||||||||||||||
|
|
|
|
|
за температуру до- |
|
новки на базі 1-го закону ТТД оціню- |
||||||||||||||
|
|
|
|
|
|
ється: |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
вкілля) і надалі підт- |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
QХ - “польза” |
|
|
холодильним коефіцієнтом ε |
||||||||||||||||
|
|
TХ <T0 |
|
римувати на заданому |
користь |
& |
|
|
|
|
q |
|
|
|
|||||||
|
|
|
|
|
рівні. |
|
|
|
|
Q |
х |
|
= |
х |
|
||||||
|
|
|
|
|
|
|
|
|
ε = |
= |
N |
|
l |
|
> або < |
||||||
|
|
|
|
|
|
|
|
|
|
витрата |
ц |
|
|
|
ц |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
1 (далі переконаємося) |
|
|
|
|
|
|
|
|
|||
|
|
ε ,ϕ |
- показують скільки користі можна отримати на одиницю витрат ро- |
||||||||||||||||||
боти.
ТТД (3-й семестр) |
2015 р. |

Лекция №10 |
65 |
§ 2.5. ЗАСТОСУВАННЯ 1-ГО ЗАКОНУ ДЛЯ СТАЦІОНАРНИХ ПОТОКОВИХ ПРОЦЕСІВ ДО ТЕПЛОТЕХНІЧНИХ ПРИСТРОЇВ.
Схема дій при складанні енергобалансу:
1). Формулювання завдання. Зображення схеми установки або її елементу (системи) і виділення обмежень по умові завдання. У нашому курсі зазвичай g z = 0 . Приклади:
А). ТО (ТЕПЛООБМІННИКИ) ПОВЕРХНЕВОГО ТИПА - ПРИЗНАЧЕНІ ДЛЯ ПЕРЕДАЧІ ТЕПЛОТИ ВІД ГРІЮЧОГО ПОТОКУ ДО ТОГО, ЩО НАГРІВАЄТЬСЯ.
Для потокових процесів масову витрату водяної пари часто позначають як D[кг с]. (замість m& [кг
с]. (замість m& [кг с])
с])
Обмеження:
1) & = 0
lтех ( N тех )
2) , & для кожного k ( K ) = 0
Греющий поток 
потоку зміною кінетичної енергії можна нехтувати.
Нагреваемый
поток
У нашому курсі вважатимемо, що теплообмінник добре теплоізольований і відведення теплоти в довкілля відсутнє (Qо с=0)
Б) АДІАБАТНІ (Q = 0) МАШИНИ —
(Турбіни, нагнітачі: компресори, димососи, насоси, вентилятори)
а ) Адіабатна турбіна:
|
|
w1 ,m , |
|
|
H 1 = h1 m , |
w2=w1 |
|
|
|
K 1 = k1 m |
|
K=0 |
1 |
|
Q=0 |
|
|
|
|
|
|
|
|
 N тех = m& lтех
N тех = m& lтех
Обмеження:
1). За визначенням q = 0, (Q = 0)
2). Зміною k , ( K ) нехтуємо з причини малос-
|
|
|
|
|
ті |
|
|
|
Q |
|
2 |
w2 ,m , |
У турбіні РТ взаємодіє з лопатками, |
які |
|||
|
||||||||
|
|
|
|
жорстко пов'язані з валом і РТ передає лопаткам |
||||
|
|
|
H 2 = h2 m , |
|||||
|
|
|
K 2 = k2 m |
енергію у формі технічної роботи ( l |
тех |
> 0 ) |
усе- |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
редині турбіни. По відношенню до РТ лопатки є зовнішнім середовищем. Робота виконується за рахунок зменшення ентальпії (потенційній енергії потоку робочого тіла).
Таким чином, енергія потоку речовини |
& |
(в основному H перетворю- |
& |
& |
≈ |
& |
ється на технічну роботу. (з врахуванням , що К = 0 |
Eпр |
H ) |
ТТД (3-й семестр) |
2015 р. |

Лекция №10 |
66 |
б ) Адіабатні нагнітачі -
призначені для підвищення тиску газоподібних робочих тіл (повітря, інші гази, пари) до заданого тиску. У них робота передається від лопаток до РТ
( l тех < 0 ).По відношенню до РТ лопатки є зовнішнім середовищем.
|
|
|
w , m , h |
2 |
|
|
|
|
|
||
|
|
|
2 |
|
|
|
2 |
|
|
|
|
w2 w1 |
|
|
|
|
|
|
|
|
|
|
|
K=0 |
|
|
|
|
|
Q=0 |
|
|
|
|
& |
|
|
||||
|
|
|
|
N тех |
= m lтех |
|
|
|
|
Обмеження ті ж, що і для турбіни:
1. |
- За визначенням q = 0, (Q = 0) |
2. |
- Зміною k , ( K ) нехтуємо з причини |
малості
Q
1
w1, m , h1
2). Часто доцільно представити схему установки або її елемент у вигляді зручному для складання енергобалансу з нанесенням тих енергопотоків, які задані в завданні.
Наприклад:
теплообмінник (два варіанти рис.):
H1
1
|
H1 |
|
|
|
H2 |
||
H3 3 |
1 |
2 |
|
|
|||
|
|
|
|
|
|
|
|
|
Q |
|
Q |
|
|
||
|
|
|
|
|
|
||
|
2 H2 |
|
|
|
|
|
|
|
H3 |
4 |
|
H4 |
|||
|
3 |
|
|
||||
|
|
|
|
|
|
||
Qос=0 |
4 |
|
Qос=0 |
|
|
|
|
|
H4 |
|
|
|
|
|
|
3). Складання енергетичного балансу і вирішення завдань.
Особливість складання енергобалансу визначається особливостями виводів рівнянь (3а) і (3б)
А) Часткова форма (3а)
1. Виділимо в термодинамічній системі, потоки з однаковою витратою речовини на вході і виході (( m& 1 = m& 2 = m& [кг/с]) ). Для кожного потоку записати
рівняння в частковій формі і нанести обмеження за умовами завдання.
2. Пам’ятати, що в рівнянні (3а) всі алгебраїчні (підставляти зі своїм знаком).
Б) Узагальнена форма (3б)
1)За допомогою контрольної поверхні виділити дану систему і нанести лише ті енергетичні потоки, які для неї характерні.
2)В узагальнене рівняння енергобалансу підставляємо модулі числових значень величин, і результат розрахунку теж завжди модуль. Напрям енергетичного потоку оцінюється по стрілці на малюнку і по індексах «підв» і
«відв.»
ТТД (3-й семестр) |
2015 р. |

Лекция №11-12 |
67 |
Лекція №11-12 |
Дата: |
Зауваження по рівняннях 1-го закону ТТД
1.Рівняння (1) і (2) - для закритих систем. Уміти виводити і знати.
2.Рівняння (3) і (4) - для потокових процесів. Уміти виводити, знати особливості виводу цих рівнянь та особливості складання балансу.
3.Для вивчення використовувати лекції, зошит для практичних за- нять, «Методичні вказівки до самостійної роботи по курсу ТТД» і «Роздавальний матеріал по курсу ТТД» .
§ 2.6. ДРУГИЙ ЗАКОН ТД І ЙОГО ФОРМУЛЮВАННЯ
Немного истории:
В 1850 г. Клаузиус на основе идей Карно, Майера и Джоуля сформулировал оба основных закона ТД. Он впервые дал количественную формулировку Первого закона ТД в виде уравнения, связывающего величины тепла и работы с внутренней энергией. При формулировке Второго закона ТД он ввел новую величину, которую вначале назвал «эквивалентом превраще- ния», а затем (1865 г.) энтропией. Утверждение Второго закона ТД о направлении всех естественных процессов нашло выразительное проявление в
принципе возрастания энтропии.
Тепломеханічні процеси підкоряються двом законам. Виконання 1-го закону є необхідним, але недостатньою умовою протікання цих процесів. Якщо дотримується 1-й, а 2-й ні, то такі процеси протікати не можуть. Таким чином, 2-й закон накладає обмеження на протікання реальних процесів. 2-й закон вказує, які процеси при дотриманні 1-го можливі, а які ні. Обидва закону носять дослідний характер і підтверджуються всім досвідом, накопиченим людством.
1-й закон - головбух
2-й закон - директор
Другий закон складається з 2-х тверджень.
1) Принцип існування ентропії (Поняття ентропії введене Клаузіусом)
|
|
dS = |
δQ +δ Q r |
|
|
(1) |
|
|
T |
|
|
||
|
|
|
|
|
||
δQ >< 0 |
- зовнішній теплообмін |
|
||||
δQr ≥ 0 |
- теплота тертя |
|
|
|
|
|
T > 0 |
- абсолютна температура К. |
|
||||
Рівняння (1) використовується для обчислення ентропії тіла і її зміни в процесі. Міркування по структурно-логічному обґрунтуванню рівняння (1)
приведені в Розділі 1 (СРС до Лекції №4).
2) Принцип не зменшення ентропії ізольованої системи (принцип зростан-
ня ентропії ізольованої системи, в якій протікають реальні процеси).
ТТД (3-й семестр) |
2015 р |

|
Лекция №11-12 |
68 |
|
|
|
|
|
|
n |
|
|
|
SІС = ∑ Si ≥ 0 |
|
(2) |
|
i =1 |
|
|
i - кількість тіл ізольованої системи |
|
||
Si зміна ентропії окремого тіла системи |
|
||
Ентропія ізольованої системи не може зменшуватися.
Нагадаємо: ІС - це сукупність тіл, які обмінюються енергією лише між собою за відсутності енергообміну із зовнішнім середовищем.
n
Рівняння (2) вимагає, аби алгебраїчна сума ∑ Si ≥ 0 , при цьому зміна
i =1
ентропії окремого тіла може бути і менше 0.
З (2) можна виділити 3 ознаки протікання тепломеханічних процесів.
а) SІС > 0 - ознака протікання реальних (необоротних) процесів в ізольо-
ваних системах (ІС).
Ентропія ІС, в якій протікають реальні процеси завжди збільшується (народжується, виробляється, створюється).
SІС = ( SІС 2 − SІС1 ) > 0 , тобто
SІС 2 > SІС1 , для реальних процесів.
Уцьому і полягає однобічна спрямованість реальних процесів.
Твердження 2-го закону про однобічну спрямованість реальних (необоротних) процесів в ізольованій системі, тобто твердження про їх необоротність, є головним в 2-м законі.
Причини необоротності можна узагальнити, якщо ввести поняття узагальненого тертя (механічне, гідравлічне, магнітне, теплове тертя) і відповідно пов'язаних з тертям узагальнених опорів. В результаті узагальненого тертя всі форми руху переходять в теплову (хаотичну) форму руху, що приводить до зростання ентропії ІС. Таке явище отримало назву - дисипація енер- гії (розсіювання). Дисипацію енергії можна розглядати як виділення теплоти тертя . Дисипація енергії породжується необоротностями та призводить до зниження якості енергії, до зниження енергетичної ефективності протікання процесу, а значить до перевитрати палива.

 Боротьба з необоротностями - головне завдання теплотехніки
Боротьба з необоротностями - головне завдання теплотехніки
 .
.
В курсі ТТД зручно виділити дві причини необоротності:
ТТД (3-й семестр) |
2015 р |
Лекция №11-12 |
69 |
1.Тертя в РТ (механічне, гідравлічне і відповідно пов'язані з тертям механічний, гідравлічний опори).
2.Теплообмін при кінцевій різниці температур між РТ і джерелом тепло-
ти (термічне тертя породжує термічний опір T - курс ТМО).
ПРИКЛАДИ НЕОБОРОТНОСТІ
Теплообмінники (ТО) поверхневого типа.
H1
1Якщо хороша теплова ізоляція (адіабатна) то
основними необоротностями будуть:
H3 |
|
|
Q |
|
|
|
|
|
|
|
|
|
|
2 H2 |
1) |
тертя по ходу РТ |
|||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
2) |
теплообмін при кінцевій різниці температур |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
між потоками |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Qос=0 |
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
H4 |
|
|
|||||
Адіабатні машини:
W1, m , h1, k1
1
 N тех = m& lтех
N тех = m& lтех
W2=W1
K=0
Q=0
2 W2, m , h2, k2
1)тертя в РТ
2)друга необоротність виключається, оскільки процес протікає без ТО.
б) SІС = 0 - ознака протікання оборотних
процесів в ізольованих системах (ІС).
SІС = ( SІС 2 − SІС1 ) = 0 SІС 2 = SІС1 .
Ентропія ІС при протіканні в ній оборотних процесів не змінюється (немає узагальненого тертя, немає узагальненого опору, немає переходу різних форм впорядкованого руху в хаотичну теплову форму) .Реально здійснити оборотні процеси не можливо. Вони досяжні лише в принципі. Це поняття є абстракцією.
Оборотні процеси у зв'язку з відсутністю в них узагальненого тертя мають найвищу енергетичну ефективність. Тому в курсі вони розглядатимуться як еталон для реальних процесів
в) SІС < 0 - ознака неможливих процесів в ізольованих системах (ІС).
Хаотичний рух у впорядкований рух сам по собі переходити не може.
ТТД (3-й семестр) |
2015 р |

Лекция №11-12 |
70 |
§ 2.7. ОСОБЛИВОСТІ ТЕПЛООБМІНУ В ІС
а) Передача теплоти від гарячого тіла (Г) до холодного (Х):
Г
Х
TГ = const
Горяче тіло (Г): TГ = const
QrГ = 0 (рівноважний процес)
Холодне тіло (Х) TХ = const
QrХ = 0 (рівноважний процес)
 TХ = const
TХ = const
1)Застосуємо 1-й закон: Q Г = Q Х = Q
2)Застосуємо 2-й закон:
|
|
|
|
|
|
Q |
Г |
|
|
QХ |
|
|
Q |
|
Q |
|
|
SІС = |
SГ + |
S Х |
= − |
|
|
|
|
+ |
= |
− |
+ |
|
> 0 |
||||
|
|
|
|||||||||||||||
|
|
TГ |
|
|
TГ |
|
|||||||||||
|
|
|
|
|
|
|
|
TХ |
|
|
TХ |
|
|||||
оскільки TГ > TХ , процес можливий, але необоротний (оскільки супроводиться зростанням ентропії).
|
|
|
Звідки взялися формули |
? |
|
Якщо δQr = 0 |
|
|
||||||||||||||||
T |
|
|
|
|
TГ |
dS = |
δQ +δ Q r |
|
|
|
|
|||||||||||||
|
|
|
|
T |
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
T |
|
|
|
|
2 |
|
|
|
|
Q |
|
|
|
|
|
|
|
|
|
|
|
TХ |
|
|
Q |
= ∫TdS = {T = const}= T S |
|
S = |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(при T = const ) |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
SГ < 0 |
|
|
|
S ИС > 0 s |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S Х > 0
(Необоротний теплообмін)
Якщо температури відрізняються на нескінченно малу величину
T |
|
TГ |
TГ |
− TХ |
= dT то TГ |
≈ TХ , |
то |
S ИС = 0 - оборотне |
|
|
|||||||
|
|
TХ |
||||||
|
|
протікання процесу |
|
|
|
|||
|
|
|
|
|
|
|||
|
TГ = TХ |
|
|
|
|
|
|
|
Sис = 0
(Оборотний теплообмін)
s
SГ < 0
S Х > 0
ТТД (3-й семестр) |
2015 р |
