
- •Міністерство освіти і науки, молоді та спорту україни
- •Міністерство освіти і науки, молоді та спорту україни
- •Самостійна робота № 6
- •Спільні та відмінні ознаки неорганічних і органічних сполук
- •Номенклатура
- •Завдання для самостійної роботи.
- •Самостійна робота № 7
- •Природні джерела вуглеводнів Нафта, вугілля, природний газ
- •Природний газ
- •Гази, супутні нафті
- •Нафта Склад і властивості нафти
- •Перегонка нафти
- •Вуглеводневі фракції, які добувають при перегонці нафти
- •Крекінг нафтопродуктів.
- •Кам'яне вугілля
- •Вуглеводнева сировина та охорона довкілля
- •Завдання для самостійної роботи.
- •Самостійна робота № 8
- •Будова фенолу
- •Фізичні властивості
- •Добування
- •Самостійна робота № 9
- •Фізичні властивості
- •Поширення в природі
- •Хімічні властивості
- •Застосування
- •Добування штучних волокон
- •Завдання для самостійної роботи.
- •Самостійна робота № 10
- •Добування
- •Застосування
- •Завдання для самостійної роботи.
- •Самостійна робота № 11
- •Значення хімії у створенні нових матеріалів і. Металічні матеріали
- •Іі. Неметалічні матеріали
- •Нові методи добування матеріалів
- •Значення хімії у розв'язанні сировинної проблеми
- •Завдання хімії у розв'язанні сировинної проблеми
- •Хімія у повсякденному житті
- •Хімія та екологія Основні джерела забруднення довкілля
- •Хімія – головна сила у боротьбі за чистоту природи
- •Роль хімії в житті суспільства
- •Озонові дірки в атмосфері
- •Парниковий ефект
- •Ядерна зима
- •Екологічний моніторинг
- •Завдання для самостійної роботи.
Завдання для самостійної роботи.
Скласти реферат, кросворд або доповідь на теми: «Природні джерела вуглеводнів», «Основні види палива, та їх значення в енергетиці»,
«Вуглеводнева сировина та охорона довкілля»
Самостійна робота № 8
Тема: Феноли, їх характеристика, фізичні та хімічні властивості, добування та застосування.
Феноли
Феноли - ароматичні сполуки, до складу молекул яких входять гідроксильні групи, зв'язані з ароматичним ядром.
ОН
ОН
СН3

Фенол о-крезол
(одноатомні феноли)
ОН
ОН
НО
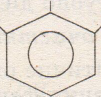
Пірогалол (трьохатомний фенол)
ê
ОН
Гідрохінон (двоатомні феноли)
Будова фенолу
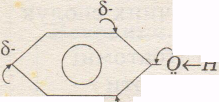
ОН – група, зв’язана з ароматичними радикалом (феніл). p - система бензольного кільця втягує неподілені електрони Оксигену. Це приводить до збільшення полярності зв’язку О¬Н, за рахунок чого фенол набуває властивості слабкої кислоти (карболової). Також у бензольному ядрі підвищується електронна густина у положеннях 2,4,6, де і відбувається зміщення атомів гідрогену.
Фізичні властивості
Тверда, кристалічна речовина (tпл 42°С). Червоніє на повітрі через окиснення. За кімнатної температури погано розчинний у воді, при 60°С у будь-яких співвідношеннях, отруйний.
Хімічні властивості фенолу
Обумовлені гідроксильною групою – ОН
Зростає кислотність групи ОН. Фенол – слабкіша кислота, ніж Н2СО3 і Н2S, але сильніша, ніж алканоли.
Взаємодія з активними металами з утворенням фенолятів
2С6Н5ОН + 2Na → 2C6H5ONa + H2
Взаємодія з лугами (відмінність від одноатомних спиртів)
2С6Н5ОН + 2NaОН → 2C6H5ONa + H2О
Феноляти розкладаються слабкими кислотами
C6H5ONa + СО2 + Н2О ® C6H5OН + NaНСО3
Якісна реакція на фенол
3C6H5OH + FeCI3 ® [C6H5O]3Fe + 3HCI
фіолетовий розчин
ферум (ІІІ) феноляту
Обумовлені бензольним ядром
Внаслідок зростання густини у кільці полегшується атака кільця частинками, що мають дефіцит електронів (електрофіли). Реакції електрофільного заміщення.
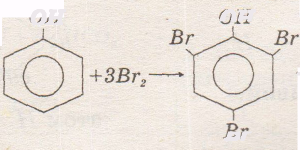
ОН
+ЗНВг
Взаємодія з бромною водою
Взаємодія з нітратною кислотою (нітрування)
С6Н5ОН + НNO3 C6H5NO2 + H2O
Добування
Із кам’яновугільної смоли
С6Н6
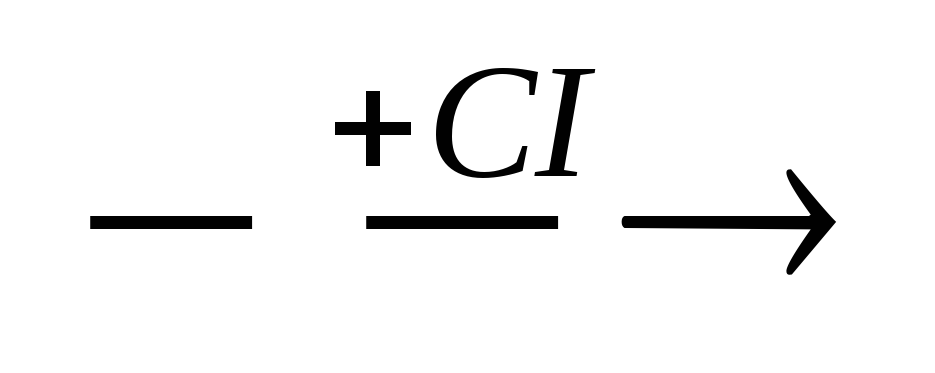 С6Н5СІ
С6Н5СІ
 С6Н5ОН
С6Н5ОН
Застосування
1. У медицині як антисептик (карболка).
2. Виробництво фенолформальдегідних пластмас
3. Виробництво барвників, лікарських речовин вибухових речовин.
Охорона довкілля
Від промислових відходів, що містять фенол (промислові відходи коксохімічного виробництва). Фенол згубно діє на флору і фауну; у людини викликає опіки і отруєння.
Методи очистки відходів від фенолу
1. Каталітичне окислення газів, що містять фенол.
2. Виділення фенолу розчинниками.
3. Обробка озоном.
4. Біохімічний метод.
Завдання для самостійної роботи.
1. Назвати речовини, що мають такі формули:
СН3СІ, С6Н5СІ, С6Н5ОН, С2Н5ОН, С6Н5СН3.
2. Здійснити перетворення:
СН4 → С2Н2 → С6Н6 → С6Н5СІ → С6Н5ОН → С6Н5СН3
3. Який об’єм водню виділиться в результаті взаємодії 2,3 г натрію з надлишком фенолу (н.у)?
4. Скільки фенолу можна добути з 156 кг бензолу, якщо виробничі втрати становлять 10%?
5. Зобразити структурні формули ізомерних ароматичних сполук складу:
а) С6Н6О2; б) С7Н8О. Назвати їх. Які з них належать до фенолів? Чому?
6. На основі теорії будови органічних речовин передбачити хімічні властивості сполуки, формула якої С6Н5 – СН2 – ОН. Написати відповідні рівняння реакцій.
7. На нейтралізацію суміші фенолу з етанолом витратили розчин об’ємом 50 мл з масовою часткою натрій гідроксиду 18 % і густиною 1,2 г/мл. Така маса суміші прореагувала з металічним натрієм масою 9,2 г. Визначити масові частки фенолу та етанолу у суміші.
8. Дописати рівняння реакцій, назвати речовини: С6Н5ОН + NaОН →
9. Пояснити екологічні проблеми, що виникають при виробництві фенолу.
10. Написати рівняння реакцій бромування фенолу і бензолу. Пояснити відмінність на основі електронної теорії.
11. З якими з цих речовин: їдкий натр, сода, бромна вода, нітратна кислота – реагуватиме фенол? Скласти рівняння реакції, назвати продукти.
12. У фенолу чи етанолу більше появляються кислотні властивості? Відповідь обґрунтувати рівнянням реакцій.
13. Як проявляється взаємний вплив гідроксогрупи і бензольного циклу в молекулі фенолу? Відповідь підтвердити рівняннями реакцій.
14. Який об’єм водню виділиться при взаємодії фенолу з 5,75 г натрію?
15. Що відбудеться, якщо крізь розчин натрій феноляту пропустити сірчистий газ? Скласти рівняння реакції.
16. Дати порівняльну характеристику фенолу і бензолу. Що спільного і відмінного:
а) в їх будові; б) властивостях? Відповідь підтвердити рівняннями реакцій.
17. Як у лабораторних умовах добути фенол, якщо вихідною речовиною є ацетилен та інші необхідні речовини?
18. Під час взаємодії розчину фенолу у бензолі (масова частка фенолу 20%) з металічним натрієм добули водень , який повністю прореагував з бутадієном масою 5,4 г. Визначити масу розчину фенолу у бензолі.
