
- •Введение
- •Глава I. Химическая термодинамика
- •2. Теплоемкость идеального газа.
- •3. Теплоемкость твердых тел.
- •4. Правило Неймана - Коппа.
- •5. Температурная зависимость теплоемкости.
- •6. Квантовая теория теплоемкости
- •Глава III. Применение первого начала к химическим процессам
- •Термохимия – раздел термодинамики
- •2. Связь тепловых эффектов химических реакций при постоянном объеме (qv) и давлении (qp).
- •3. Закон Гесса.
- •4. Следствия из закона Гесса.
- •5. Зависимость теплового эффекта химической реакции от температуры (уравнение Кирхгофа).
- •Глава IV. Второе начало термодинамики.
- •Содержание второго начала термодинамики.
- •2. Обратимые и необратимые процессы.
- •3. Коэффициент полезного действия тепловой машины. Цикл Карно.
- •4. Работа холодильника (теплового насоса).
- •5. Измерение рассеивания энергии. Энтропия.
- •6. Термодинамический взгляд на энтропию.
- •7. Вычисление энтропии.
- •8. Направление протекания процессов в изолированных системах и термодинамические условия равновесия.
- •9. Энергия Гиббса. Энергия Гельмгольца.
- •10. Направление протекания процессов в неизолированных системах и термодинамические условия равновесия.
- •11. Уравнение Гиббса - Гельмгольца.
- •12. Применение второго закона термодинамики к фазовым переходам. Уравнение Клаузиуса - Клапейрона.
- •13. Химическое равновесие. Закон действующих масс и константа равновесия.
- •14. Различные формы констант равновесия и связь между ними.
- •15. Уравнение изотермы химической реакции. Химическое сродство.
- •16. Направление реакций и условие равновесия.
- •17. Зависимость константы равновесия от температуры и давления.
- •18. Равновесие в гетерогенных системах.
- •19. Термическая диссоциация.
- •Глава V. Третий закон термодинамики.
- •Недостаточность I и II законов термодинамики для расчета химического сродства.
- •2. Тепловая теорема Нернста.
- •3. Следствия из тепловой теоремы Нернста.
- •4. Расчет абсолютных значений энтропии.
- •5. Применение таблиц термодинамических функций для расчетов равновесий.
- •Глава VI. Правило фаз.
- •1. Основные понятия и определения.
- •2. Уравнение правила фаз.
- •3. Геометрический образ уравнения состояния.
- •4. Однокомпонентные системы.
- •5. Двухкомпонентные системы.
- •5.1. Системы с неограниченной растворимостью
- •5.2. Системы с неограниченной растворимостью компонентов в жидком состоянии и ограниченной в твердом.
- •6. Трехкомпонентные системы.
5. Зависимость теплового эффекта химической реакции от температуры (уравнение Кирхгофа).
Большинство экспериментальных определений теплот реакций относится к комнатной температуре, хотя практически важно знать его значение при любой температуре. Первое начало термодинамики позволяет определить зависимость теплового эффекта от температуры и осуществлять соответствующие термохимические расчеты.
Для реакции вида:
![]() ,
(3.21)
,
(3.21)
где
![]() - коэффициенты;
- коэффициенты;
М1, М2,
...,N1,N2,
... – продукты химической реакции,
тепловой эффект
![]() .
.
![]() .
(3.22)
.
(3.22)
Тогда:
![]() .
(3.23)
.
(3.23)
После дифференцирования по температуре:
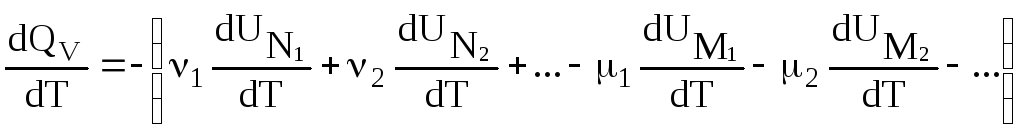 ,
(3.24)
,
(3.24)
где
![]() - температурный коэффициент теплового
эффекта химической реакции;
- температурный коэффициент теплового
эффекта химической реакции;
Учитывая, что
![]() = СV:
= СV:
![]() (3.25)
(3.25)
или
![]() .
(3.26)
.
(3.26)
Уравнение (3.26) – уравнение Кирхгофа в дифференциальной форме записи, которое читается:
“Температурный коэффициент теплового эффекта химической реакции равен изменению теплоемкости системы за счет этой реакции.”
Если
![]() ,
то
,
то
![]() ,
т. е. с повышением температуры тепловой
эффект химической реакции уменьшается.
,
т. е. с повышением температуры тепловой
эффект химической реакции уменьшается.
Если
![]() ,
то
,
то
![]() и с повышением температуры тепловой
эффект химической реакции возрастает.
и с повышением температуры тепловой
эффект химической реакции возрастает.
При
![]() ,
то
,
то
![]() и температура не влияет на величину
теплового эффекта химической реакции.
и температура не влияет на величину
теплового эффекта химической реакции.
После разделения переменных и интегрирования:
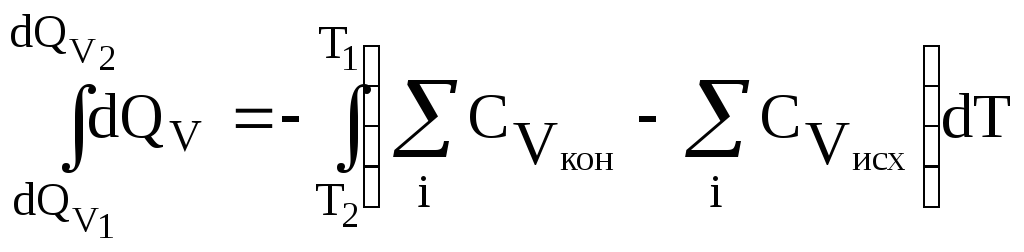 .
(3.27)
.
(3.27)
где
![]() .
.
Тогда
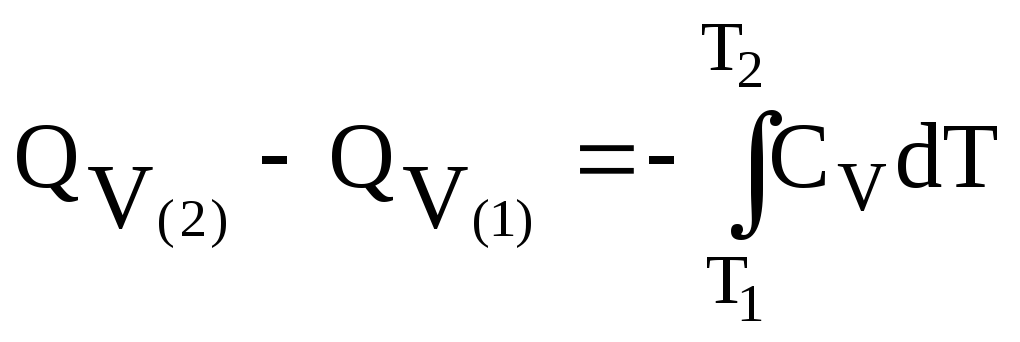 (3.28)
(3.28)
и по аналогии:
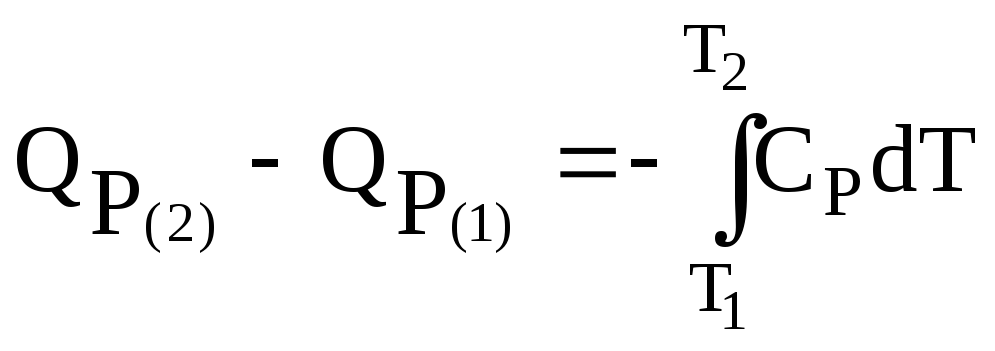 .
(3.29)
.
(3.29)
Уравнения (3.28) и (3.29) – уравнения Кирхгофа в интегральной форме записи.
В обобщенной форме записи:
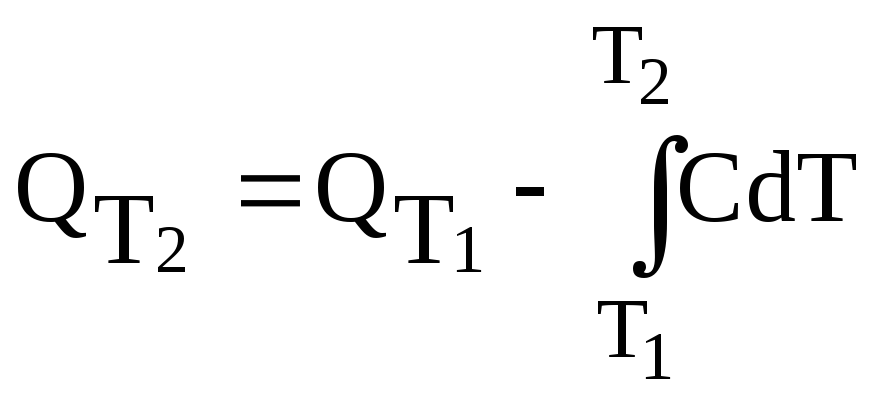 .
(3.30)
.
(3.30)
Кроме того:
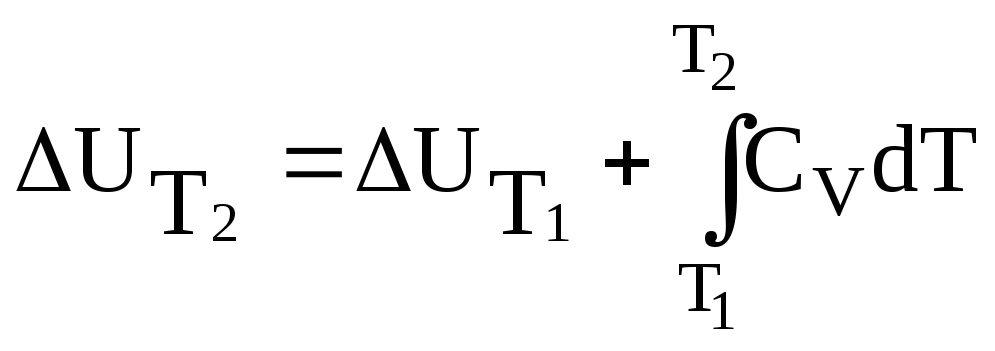 ,
(3.31)
,
(3.31)
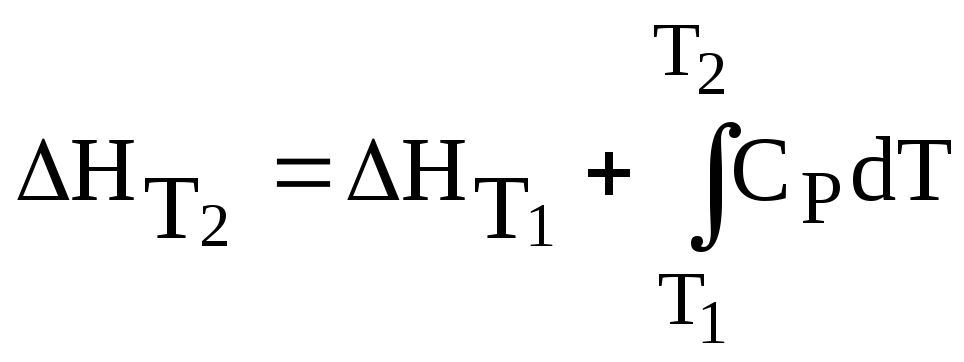 .
(3.32)
.
(3.32)
Таким образом, для нахождения величины теплового эффекта химической реакции при заданной температуре необходимо знать его величину при любой другой температуре и располагать уравнениями Сi=f(T).
Глава IV. Второе начало термодинамики.
Содержание второго начала термодинамики.
Первого начала термодинамики недостаточно для полной характеристики термодинамических процессов. В рамках первого начала можно установить энергетический баланс процессов, но получить сведения о возможности, направлении и пределах их протекания не представляется возможным.
Итак, второе начало позволяет:
находить направление и устанавливать возможность самопроизвольного (естественного, спонтанного) течения термодинамических процессов и пределы их протекания;
определять условия, при которых превращение какого-либо запаса энергии в полезную работу происходит наиболее полно.
Предлагаются следующие формулировки второго начала термодинамики:
“... холодное тело В, погруженное в теплое тело А, не может воспринять большую степень теплоты, чем какую имеет А.”
(М. В. Ломоносов)
“... невозможен процесс, единственный результат которого состоял бы в переходе энергии от более холодного тела к более горячему.”
(Рудольф Клаузиус)
“... невозможен процесс, единственный результат которого состоял бы в поглощении теплоты от нагревателя и полного преобразования этой теплоты в работу.”
(У. Томсон (лорд Кельвин))
