
- •Глава 1 Элементы кинематики
- •§ 1. Модели в механика. Система отсчета. Траектория, длина пути, вектор перемещения
- •§ 2. Скорость
- •§ 3. Ускорение и его составляющие
- •2) Прямолинейное равнопеременное движение. При таком виде движения
- •4)Прискорость по модулю не изменяется, а изменяется по направлению. Из формулыследует, что радиус кривизны должен быть постоянным. Следовательно, движение по окружности является равномерным;
- •§ 4. Угловая скорость и угловое ускорение
- •Глава 2
- •§ 5. Первый закон Ньютона. Масса. Сила
- •§ 7. Третий закон Ньютона
- •§ 8. Силы трения
- •§ 9. Зеком сохранения импульса. Центр масс
- •§ 10. Уравнение движения тала переменной массы
- •Глава 3 Работа и энергия
- •§ 11. Энергия, работа, мощность
- •§ 12. Кинетическая и потенциальная энергии
- •§ 13. Закон сохранения энергии
- •§ 14. Графическое представление энергии
- •§ 15. Удар абсолютно упругих и неупругих тал
- •Глава 4Механика твердого тела
- •§ 16. Момент инерции
- •§ 17. Кинетическая энергия вращения
- •§ 18. Момент силы. Уравнение динамики вращательного движения твердого тела
- •§ 19. Момент импульса и закон его сохранения
- •§ 20. Свободные оси. Гироскоп
- •§ 21. Деформации твердого тела
- •Глава 5 Тяготение. Элементы теории поля
- •§ 22. Законы Кеплера. Закон всемирного тяготения
- •§ 23. Сила тяжести и вес. Невесомость
- •§ 24. Поле тяготения и его напряженность
- •§ 25. Работа в поле тяготения. Потенциал поля тяготения
- •§ 26. Космические скорости
- •§ 27. Неинерционные системы отсчета. Силы инерции
- •1. Силы инерции при ускоренном поступательном движении системы отсчет». Пусть на тележке к штативу на нити подвешен шарик массой т (рис. 40). Пока тележка покоится или движется
- •2. Силы вверим, действующие на тело, покоящееся во вращающейся системе отсчета. Пусть диск равномерно вращается с угловой скоростьювокруг вертикальной оси, проходящей через
- •Глава 6 Элементы механики жидкостей
- •§ 28. Давление в жидкости и газа
- •§ 29. Уравнение неразрывности
- •§ 30. Уравнение Бернулли и следствия из него
- •§ 31. Вязкость (внутреннее трение). Ламинарный и турбулентный режимы течения жидкостей
- •§ 32. Методы определения вязкости
- •§ 33. Движение тел в жидкостях и газах
- •5.3. Сопло фонтана, дающего вертикальную струю высотой имеет форму усеченного
- •5.5. В широком сосуде, наполненном глицерином (плотность падает с устано-
- •Глава 7
- •§ 34. Преобразования Галилея. Механический принцип относительности
- •§ 35. Постулаты специальной (частной) теории относительности
- •§ 38. Преобразования Лоренца
- •§ 37. Следствия из преобразований Лоренца
- •1. Одновременность событий в разных системах отсчета. Пусть в системе к в точках с координатамив моменты временипроисходят два события. В системе
- •§ 38. Интервал между событиями
- •§ 39. Основной закон релятивистской динамики материальной точки
- •§ 40. Закон взаимосвязи массы и энергии
- •Глава 8
- •§ 41. Статистический и термодинамический методы. Опытные законы идеального газа
- •2) Давление данной массы газа при постоянном объеме изменяется линейно с температурой:
- •§ 42. Уравнение Клапейрона — Менделеева
- •§ 43. Основное уравнение молекулярно-кинетической теории идеальных газов
- •§ 44. Закон Максвелла о распределении молекул идеального газа по скоростям и энергиям теплового движения
- •2) Средняя3) средняя квадратичная
- •§ 45. Барометрическая формула. Распределение Больцмана
- •§ 46. Среднее число столкновений и средняя длина свободного пробега молекул
- •§ 47. Опытное обоснование молокулярно-кинггичоской теории
- •§ 48. Явления переноса в термодинамически неравновесных системах
- •§ 48. Вакуум и методы его получения. Свойства ультраразреженных газов
- •Глава 9 Основы термодинамики
- •§ 51. Первое начало термодинамики
- •§ 52. Работа газа при изменении его объема
- •§ 53. Теплоемкость
- •§ 54. Применение первого начала термодинамики к изопроцессам
- •§ 55. Адиабатический процесс. Политропный процесс
- •§ 56. Круговой процес (цикл). Обратимый и необратимый процессы
- •§ 57. Энтропия, её статистическое толкование и связь с термодинамической вероятностью
- •§ 58. Второе начало термодинамики
- •2)ПоКлаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
- •§ 59. Тепловые двигатели и холодильные машины. Цикл Карно и его к. П. Д. Для идеального газа
- •Глава 10 Реальные газы, жидкости и твердые тела
- •§ 60. Силы и потенциальная энергия межмолекулярного взаимодействия
- •§ 61. Уравнение Ван-дер-Ваальса
- •§ 62. Изотермы Ван-дер-Ваальса и их анализ
- •§ 63. Внутренняя энергия реального газа
- •§ 64. Эффект Джоуля — Томсона
- •§ 65. Сжижение газов
- •§ 66. Свойства жидкостей. Поверхностное натяжение
- •§ 67. Смачивание
- •§ 68. Давление под искривленной поверхностью жидкости
- •§69. Капиллярные явления
- •§ 70. Твердыt тала. Моно- и поликристаллы
- •§ 71. Типы кристаллических твердых тел
- •§ 72. Дефекты в кристаллах
- •§ 73. Теплоемкость твердых тел
- •1800 К! Однако для большинства твердых тел комнатная температура является уже достаточно высокой.
- •§ 74. Испарение, сублимация, плавление и кристаллизация. Аморфные тела
- •§75. Фазовые переходы I и п рода
- •§ 76. Диаграмма состояния. Тройная точка
§ 43. Основное уравнение молекулярно-кинетической теории идеальных газов
Для
вывода основного уравнения
молекулярно-кинетической теории
рассмотрим одно-атомный идеальный газ.
Предположим, что молекулы газа движутся
хаотически, число взаимных
столкновений между молекулами газа
пренебрежимо мало по сравнению с
числом ударов о стенки сосуда, а
соударения молекул со стенками сосуда
абсолютно упругие.
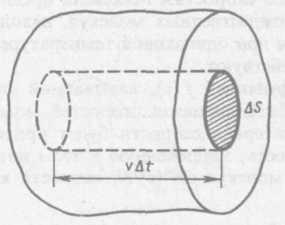
Выделим на стенке сосуда некоторую
элементарную площадку![]() (рис.
64)и
вычислим давление, оказываемое на эту
площадку. При каждом соударении
молекула,
движущаяся перпендикулярно площадке,
передает ей импульс
(рис.
64)и
вычислим давление, оказываемое на эту
площадку. При каждом соударении
молекула,
движущаяся перпендикулярно площадке,
передает ей импульс![]()
где
то
—
масса молекулы,![]() —
ее скорость. За время
—
ее скорость. За время![]() площадки
площадки![]() достигнут
только
достигнут
только
те
молекулы, которые заключены в объеме
цилиндра с основанием![]() и
высотой
и
высотой![]() (рис. 64). Число этих молекул равно
(рис. 64). Число этих молекул равно![]() (n
— концентрация молекул).
(n
— концентрация молекул).
Необходимо,
однако, учитывать, что реально молекулы
движутся к площадке![]() под
разными углами и имеют различные
скорости, причем скорость молекул при
каждом
соударении меняется. Для упрощения
расчетов хаотическое движение молекул
заменяют
движением вдоль трех взаимно
перпендикулярных направлений, так что
в
любой момент времени вдоль каждого из
них движется
под
разными углами и имеют различные
скорости, причем скорость молекул при
каждом
соударении меняется. Для упрощения
расчетов хаотическое движение молекул
заменяют
движением вдоль трех взаимно
перпендикулярных направлений, так что
в
любой момент времени вдоль каждого из
них движется![]() молекул,
причем половина
молекул,
причем половина
молекул
![]() движется
вдоль данного направления в одну
сторону, половина — в
движется
вдоль данного направления в одну
сторону, половина — в
противоположную.
Тогда число ударов молекул, движущихся
в заданном направлении, о
площадку
![]() будет
будет
![]() При
столкновении с площадкой эти молекулы
При
столкновении с площадкой эти молекулы
передадут ей импульс
• И.
Лошмидт (1821—1895) — австрийский химик и
физик.
И.
Лошмидт (1821—1895) — австрийский химик и
физик.
![]()
Тогда давление газа, оказываемое им на стенку сосуда,
![]() (43.1)
(43.1)
Если
газ в объеме V
содержит
N
молекул,
движущихся со скоростями![]() то
то
целесообразно рассматривать среднюю квадратичную скорость
![]() (43,2)
(43,2)
характеризующую всю совокупность молекул газа. Уравнение (43.1) с учетом (43.2) примет вид
![]() (43.3)
(43.3)
Выражение (43.3) называется основным уравнением молекулярно-кмнетнческой теории идеальных газов. Точный расчет с учетом движения молекул по всевозможным направлениям дает ту же формулу.
Учитывая, что n—N/V, получим
![]() (43.4)
или
(43.4)
или
![]() (43.5)
(43.5)
где Е — суммарная кинетическая энергия поступательного движения всех молекул газа.
Так как масса газа m = Nm0, то уравнение (43.4) можно переписать в виде
![]()
Для одного моля газа т=М(М — молярная масса), поэтому
![]()
где Vm — молярный объем. С другой стороны, по уравнению Клапейрона — Менделеева, pVm = RT. Таким образом,
![]()


откуда
![]() (43.6)
(43.6)
Так
как M=m0NА
где
mо
— масса одной молекулы, а![]() —
постоянная Авогадро, тоиз
уравнения (43.6) следует, что
—
постоянная Авогадро, тоиз
уравнения (43.6) следует, что
![]() (43.7)
(43.7)
где k=R/NA — постоянная Больцмана. Отсюда найдем, что при комнатной температуре молекулы кислорода имеют среднюю квадратичную скорость 480 м/с, водорода — 1900 м/с. При температуре жидкого гелия те же скорости будут соответственно 40 и 160 м/с.
Средняя кинетическая энергия поступательного движения одной молекулы идеального газа
![]() (43.8)
(43.8)
(использовали
формулы (43.5) и (43.7)) пропорциональна
термодинамической температуре
и зависит только от нее. Из этого
уравнения следует, что при![]()
т. е.
при 0 К прекращается поступательное
движение молекул газа, а следовательно,
его
давление равно нулю. Таким образом,
термодинамическая температура является
мерой
средней кинетической
энергии поступательного движения
молекул идеального газа,
и формула (43.8) раскрывает
молекулярно-кинетическое толкование
температуры.
