
- •Вопросы по дисциплине котельные установки и парогенераторы (2 семестр).
- •1. Предисловие.
- •2. Общие сведения из теории химических реакций.
- •3. Теория стационарного теплового воспламенения.
- •4. Сжигание газа.
- •4.1. Пламя в неподвижной среде.
- •4.2. Распространение фронта пламени в движущейся среде.
- •4.3. Процессы в плоском фронте пламени.
- •4.4 Стабилизация ламинарного фронта пламени.
- •4.5. Диффузионное пламя.
- •4.6. Конструкции газовых горелок.
- •5. Сжигание жидкого топлива.
- •5.1. Общие сведения.
- •5.2. Форсунки для сжигания мазута.
- •6. Сжигание твердого топлива.
- •6.1. Общие сведения горения твердого топлива.
- •6.2. Слоевой способ сжигания твердого топлива.
- •6.3. Факельный способ сжигания топлива.
- •6.4. Системы пылеприготовления.
- •6.5. Шлакоудаление.
- •7. Тяговые устройства котельного агрегата
Вопросы по дисциплине котельные установки и парогенераторы (2 семестр).
1. Предисловие.
Июнь – время сессии для студентов, тяжелейший период в нашей жизни. А экзамены главное, чем мы с вами занимаемся, чего непременно ждем, а этому предшествует утомительная подготовка, переживания… В период сессии все концентрируются на учебе (что неоднократно опровергалось в 5 общежитии).
Одним из экзаменов на 3курсе летней сессии специальности ТЭН является дисциплина «котельные установки и парогенераторы», сложность сдачи которой обусловлена необычными тестами, составленными одним из преподавателей нашей кафедры. Поэтому коллектив авторов в очередной раз разработал пособие в помощь сокурсникам в подготовке к экзамену. В данном пособии отражен основной материал, читаемый на лекциях: общие сведения по горению, горение газообразного, твердого и жидкого топлив, вспомогательное оборудование котельных.
Авторы надеются, что их труд будет оценен положительно, и желает успехов всем кто столкнется с экзаменационными тестами. Все замечания и пожелания по пособию авторы просят направлять по эл. адресу AK13-N@yandex.ru или обсуждать лично.
Успехов на экзаменах!
Казанцев А.Е.
2. Общие сведения из теории химических реакций.
Д ля
раскрытия теории горения топлив
необходимо предварительно познакомится
с механизмами протекания этих процессов.
В простейшем математическом описании
это будут химические реакции, отражающие
состав и концентрацию реагирующих
веществ и продуктов, получающихся в
ходе реакции. При этом скорость данной
реакции можно выразить соотношением
ля
раскрытия теории горения топлив
необходимо предварительно познакомится
с механизмами протекания этих процессов.
В простейшем математическом описании
это будут химические реакции, отражающие
состав и концентрацию реагирующих
веществ и продуктов, получающихся в
ходе реакции. При этом скорость данной
реакции можно выразить соотношением![]() ,
гдеAиB– реагирующие вещества,CиD– продукты реакции,a, b,
c,d– стехиометрические коэффициенты, аw1 иw2– скорость
соответственно прямой и обратной
реакции. Скорость прямой химической
реакции определяется из соотношения
,
гдеAиB– реагирующие вещества,CиD– продукты реакции,a, b,
c,d– стехиометрические коэффициенты, аw1 иw2– скорость
соответственно прямой и обратной
реакции. Скорость прямой химической
реакции определяется из соотношения![]() ,
а скорость обратной
,
а скорость обратной![]() ,
при этом следует обратить внимание на
то, что в степени стоят стехиометрические
коэффициенты (т.е.маленькиебуквыa, b,
c,d
). В случае еслиреакция равновесная,то скорости равны между собой
,
при этом следует обратить внимание на
то, что в степени стоят стехиометрические
коэффициенты (т.е.маленькиебуквыa, b,
c,d
). В случае еслиреакция равновесная,то скорости равны между собой
![]() ,
но это возможно только приравновеснойреакции. Она определяется по константе
равновесия
,
но это возможно только приравновеснойреакции. Она определяется по константе
равновесия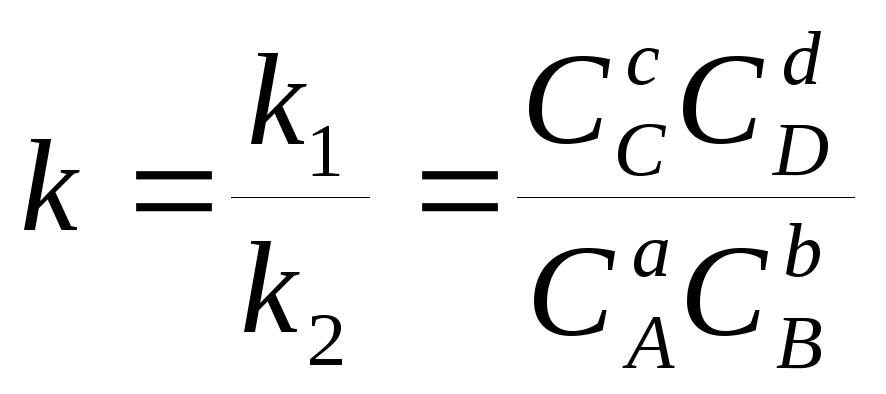 ,
которая в свою очередь определяется
законом Аррениуса
,
которая в свою очередь определяется
законом Аррениуса![]() ,
чем выше температура тем соответственно
выше скорость химической реакции.Порядок реакцииопределяется как
сумма коэффициентов. Например,
,
чем выше температура тем соответственно
выше скорость химической реакции.Порядок реакцииопределяется как
сумма коэффициентов. Например,![]() ,
,
![]() порядок реакции 1+0.5=1.5,
порядок реакции 1+0.5=1.5,![]() 1.5+1.5=3
1.5+1.5=3
Тепловой эффект реакции можно определить
как разность между энергиями активации
обратной и прямой реакции. Т.е в
математическом виде это выглядит так
![]()
![]() ,
отсюда можно сделать вывод если энергия
активации прямой реакции больше чем
обратной, то тепловой эффект реакции
будет отрицательным, то реакция называется
эндотермической, в обратном случае
экзотермической. При этомEII
– энергия активации обратной реакции,
аEI
– прямой реакции.
,
отсюда можно сделать вывод если энергия
активации прямой реакции больше чем
обратной, то тепловой эффект реакции
будет отрицательным, то реакция называется
эндотермической, в обратном случае
экзотермической. При этомEII
– энергия активации обратной реакции,
аEI
– прямой реакции.
Если вам придется столкнутся с принципом ЛеШателье-Брауна то главное в нем, что любое внешнее воздействие смещает равновесие в сторону обратную внешнему воздействию. Например при экзотермической реакции, и с отводом теплоты равновесие сместится в сторону продуктов реакции (тепло в результате выделяется, и мы его в добавок еще отводим, т.е. создаем условия для дополнительного выделения тепла). Или при понижении температуры равновесие смещается в сторону увеличения концентрации продуктов реакции.
