- •Лекция №29. Элементы квантовой механики.
- •I.Волны де Бройля.
- •II.Статистическая инитериретация волны де Бройля.
- •III.Соотношение неопределённостей Гейзенберга.
- •IV.Принцип дополнительности.
- •V.Волновая функция.Уравнение Шредингера.
- •VI.Микрочастица в потенциальной яме.
- •VII.Уравнение Шредингера для водородоподобного атома.Квантовые числа.
VI.Микрочастица в потенциальной яме.
|
|
Если поместить микрочастицу в бесконечно глубокую потенциальную яму (ограниченная область пространства, в которой потенциальная энергия рассматриваемой частицы меньше, чем вне этого пространства), то волновая функция , описывающая стационарные состояния частицы, будет иметь вид: |
![]() (13)
(13)
где ℓ – ширина ямы (ящика);
n– номер энергетического уровня;
x– место положения частицы.
Выражение для собственных значений энергии частицы в глубоком одномерном прямоугольном потенциальном ящике имеет вид:
![]() , (14)
, (14)
где а = L– ширина ямы,
n= 1, 2, 3…∞ – уровни.
Схема уровней энергии микрочастицы в таком потенциальном ящике и вид функции *показаны на рисунке 3. Минимальное значение энергии микрочастицы в потенциальной яме не равно нулю, то есть она находится в постоянном движении.
Обращает на себя внимание и зависимость плотности вероятности обнаружения микрочастицы на различных расстояниях от стенок ямы от числа n. В дальнейшемn, характеризующее энергетическое (в целом пространственное) положение микрочастицы в потенциальной яме получило названиеглавного квантового числа.
Расстояние между соседними энергетическими уровнями для частиц различной массы mв ящике шириной а составляет:
![]() (15)
(15)
|
|
Если а или mустремить в бесконечность (а,m), то расстояние между энергетическими уровнями становится бесконечно малым, то есть приходим к свободной микрочастице. Для лёгких частиц, при малых областях локализации, увеличивается минимальное значение энергии, и резко растёт расстояние между соседними уровнями (этим объясняется отсутствие электронов внутри или в непосредственной близости от атомного ядра). |
VII.Уравнение Шредингера для водородоподобного атома.Квантовые числа.
Уравнение Шредингера прекрасно описывает поведение электронов в атоме (для простоты обычно рассматривают водородоподобный атом, в котором анализируют взаимодействие ядра с одним конкретным электроном). Его решение в сферической системе координат показывает, что в общем случае плотность вероятности обнаружить электрон около ядра зависит от трёх квантовых чисел n, ℓ иm.
Первое (n), как и следовало ожидать для частицы, находящейся в потенциальной яме, характеризует энергию электрона в атоме:
![]() (16)
(16)
|
|
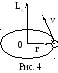
и равно 1, 2, 3,…, при этом данное выражение полностью соответствует теории Бора. Второе ℓ определяет величину орбитального момента импульса электрона в атоме (рис. 4):
и принимает значения
ℓ = 0, 1, 2, 3,…, n– 1. Третьеmзадаёт величину проекции
этого момента на заданное направление |
Lон=m·ħ,
где m= –ℓ, +ℓ,…, –1, 0, 1,…, ℓ – 1, ℓ (всего 2ℓ + 1 значений), то есть определяет направление вектора ℓ0в пространстве.
Квантовое число ℓ получило название орбитального, аm–магнитного.
С квантово-механической точки зрения радиус боровской орбиты имеет смысл расстояния от ядра, на котором плотность вероятности найти электрон имеет наибольшее значение. В зависимости от набора квантовых чисел электронное облако вокруг ядра может иметь сферическую симметрию (ℓ = 0) или приобрести вид своеобразных гантелей.
Затем, согласно теории Дирака, учитывающей релятивистский эффект, микрочастица обладает собственным моментом импульса ℓS(спином). При этом выполняется соотношение:
![]() ,
,
где S– спиновое квантовое число (для электронаS= 1/2).
Спин электрона, как и орбитальный момент импульса, не может принимать любое направление в пространстве:
Lsн = ħ·Sm,
где Sm =1/2.