
- •Лекция №29. Элементы квантовой механики.
- •I.Волны де Бройля.
- •II.Статистическая инитериретация волны де Бройля.
- •III.Соотношение неопределённостей Гейзенберга.
- •IV.Принцип дополнительности.
- •V.Волновая функция.Уравнение Шредингера.
- •VI.Микрочастица в потенциальной яме.
- •VII.Уравнение Шредингера для водородоподобного атома.Квантовые числа.
Лекция №29. Элементы квантовой механики.
I.Волны де Бройля.
При рассмотрении различных моделей атома, установлено (Резерфорд), что он имеет “ажурное” строение. Атом, как система разноимённо электрически заряжённых частиц, может быть устойчив только при условии, что заряды движутся друг относительно друга. Однако заряд, движущийся по замкнутой криволинейной траектории, имеет нормальное ускорение, а следовательно должен терять свою энергию, испуская электромагнитные волны, а это приводит к тому, что атом будет неустойчив.
Это противоречие приводит к выводу, что электроны в атомах движутся по законам, отличным от законов классической механики и электродинамики для макроскопических тел.
Ранее мы представляли электрон как частицу, т.е. материальное образование корпускулярного характера, которому присуща масса, энергия, импульс, момент импульса, размер и т.д. Однако целый ряд экспериментальных фактов заставляет признать, что электрон (а также и другие частицы) обладают не только свойствами корпускул, но и свойствами волн, подобно фотонам света. Существенным отличием является, однако, то, что фотоны не обладают массой покоя, в то время какэлектроныи большинство других элементарных частицимеют массу покоя.
Правильное решение этой проблемы было сделано в 1924 году французским физиком-теоретиком Луи де Бройлем, одним из создателей квантовой теории. Он предположил; что все частицы должны обладать волновыми свойствами, подобными волновым свойствам света, т.е. между корпускулярными и волновыми характеристиками электрона существует связь (в 1927 году это получило блестящее подтверждение в экспериментах по дифракции электронов в кристаллах) – за что в 1929 году он получил Нобелевскую премию.
Для фотона известно:
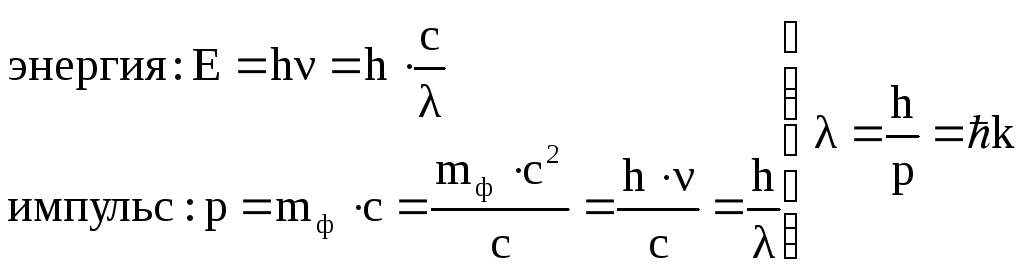 (1)
(1)
где ![]() – волновое число;
– волновое число;
![]() .
.
Де Бройль постулировал, что это соотношение (1) справедливо и для электронов (а в последствии и для любых микрочастиц и систем из них). Для электрона соотношение де Бройля:
![]() (2)
(2)
где 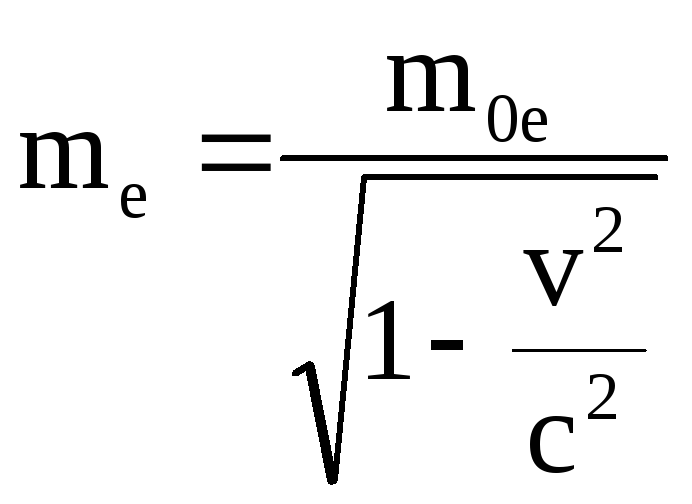
Если скорость электрона (или частицы) v<<c, тоme≈m0e.
Пример: при ускорении электрона
в поле ~ 104Вme≈mm0e,
скорость![]()
Тогда можно получить соответствующие длины волн летящих электронов из уравнения (2):
![]()
Расчёт даёт: ![]() (Uв вольтах).
(Uв вольтах).
Если U= 1 ÷ 104В= 100,1 Å (диапазон рентгеновских лучей).
Если взять дифракционную решётку, сравнимую с для электронов, то можно наблюдать дифракцию электронов. Это впервые осуществили американские физики в 1927 году – Девиссон и Джермер на кристаллах металла. Метод исследования строения вещества, основанный на дифракции электронов называетсяэлектронофографией.
Результат представляет собой прекрасное доказательство идеи де Бройля. Но возник ещё вопрос – “не присущи ли волновые свойства только потоку большой совокупности электронов? Такая задача была решена в 1948 году В. Фабрикантом, который с сотрудниками осуществил опыт по дифракции электронов со столь малой силой тока в приборе, что каждый электрон проходил через прибор независимо от других, т.е. опыт показал, что волновые свойства присущи каждому электрону в отдельности.
Выводы:
Электрон является сложным материальным образованием. Его нельзя представить в виде материальной точки, он является сложной структурой, обладающей волновыми свойствами. Эта структура, очевидно меняется в зависимости от условий, в которых находится электрон, т.е. в зависимости от характера его взаимодействия с окружающей материей.
Коргускулярность электрона проявляется в том, что электрон не делим на части.
Нет единой точки зрения в понимании природы соотношения корпускулярного и волнового аспектов.
Волна де Бройля описывает движение материальной частицы, но не даёт сведений о её структуре.
