
metodicheskoe_posobie_po_psikhiatrii
.pdf(F98.3) Pica of infancy and childhood
(F98.4) Stereotyped movement disorders
(F98.5) Stuttering (stammering)
(F98.6) Cluttering
(F98.8) Other specified behavioural and emotional disorders with onset usually occurring in childhood and adolescence: Attention deficit disorder without hyperactivity, Excessive masturbation, Nail-biting, Nosepicking, Thumb-sucking).
РАЗДЕЛ 4.
СОВРЕМЕННАЯ ПСИХОФАРМАКОТЕРАПИЯ
Открытие психотропных средств позволило назвать вторую половину XX века в истории психиатрии эрой психофармакологии. Психофармакотерапия (ПФТ) в настоящее время является основным, наиболее эффективным способом лечения психических расстройств. По данным ВОЗ, около 1/3 взрослого населения развитых стран принимают психофармакологические препараты. Это связано с их достаточно высокой эффективностью, умеренной частотой побочных явлений и простотой применения. Открытие нейролептиков и антидепрессантов между 1950 и 1960 гг., введение транквилизаторов и современных снотворных в последующие годы существенно изменило основы организации как стационарной, так и амбулаторной психиатрической помощи, повысило качество жизни пациентов с психическими расстройствами.
Современное фармакологическое воздействие позволяет довольно точно воздействовать на отдельные области головного мозга и нейрохимические системы, нормализуя протекание информационных и эмоциональных процессов в ЦНС.
Таким образом, ПФТ является неотъемлемым компонентом комплексной стратегии оказания медицинской помощи, наряду с психотерапевтическими и социальными мероприятиями.
Взаимодействие психофармакологических препаратов и организма человека описывается в отдельных разделах психофармакологии – фармакодинамики, фармакокинетики и фармакогенетики.
Фармакодинамика психотропных препаратов (совокупность эффектов и механизмы их действия).
Основные эффекты психотропных препаратов осуществляются через рецепторные механизмы посредством нейротрансмиттеров в области нейрональных синапсов.
Рецепторы – макромолекулярные структуры клетки, избирательно чувствительные к определенным химическим соединениям. Взаимодействие химических веществ с рецептором приводит к возникновению биохимических и физиологических изменений в организме, которые выражаются в том или ином клиническом эффекте. Передача нервного импульса опосредуется нейромедиаторами (нейротрансмиттерами).
Медиатор (нейротрансмиттер, нейропередатчик) – вещество, с
помощью которого нервный сигнал передается через синапс. Медиатор образуется либо в теле нейрона (и попадает в синаптическую бляшку, пройдя через весь аксон), либо непосредственно в синаптической бляшке. В синаптической бляшке молекулы медиатора упаковываются в синаптические пузырьки, в которых они хранятся до момента высвобождения.
Известно несколько медиаторных веществ, для большинства из них описаны системы синтеза, хранения, высвобождения, взаимодействия с постсинаптическими рецепторами (из которых наиболее хорошо изучен ацетилхолиновый рецептор), инактивации, возврата продуктов их расщепления в пресинаптические окончания. Согласно принципу Дейла, во всех пресинаптических окончаниях зрелого нейрона высвобождается один и тот же медиатор. Однако в процессе своего развития некоторые нейроны временно синтезируют и высвобождают более одного медиаторного вещества. Предполагают, что каждый нейрон можно отнести к категории либо возбуждающих, либо тормозных («концепция функциональной специфичности»). Возбуждающий или тормозной характер действия медиатора определяется свойствами постсинаптической мембраны. Одна постсинаптическая мембрана может иметь более одного типа рецепторов для данного медиатора и каждый из этих рецепторов способен контролировать разный механизм ионной проницаемости («принцип множественности медиаторного сигнала»). С другой стороны, разнообразие медиаторных веществ заставляет предполагать, что они выполняют и другие функции, возможно, служат трофическими факторами. В настоящее время известно более 30 веществ, выполняющих медиаторные функции.
Среди большого количества обнаруженных нейротрансмиттеров, наиболее важными являются следующие:
1.Аминокислоты: глутаминовая кислота, аспарагиновая кислота, глицин, гамма-аминомасляная кислота (ГАМК).
2.Моноаминовые нейротрансмиттеры: серотонин, ацетилхолин, катехоламины (адреналин, норадреналин, дофамин).
3.Летучие неорганические нейротрансмиттеры исследуемые в последние годы, особенно окись азота (NO).
4.Пептиды (например, вещество Р). Многие из пептидов, впрочем, чаще играют не непосредственно нейротрансмиттерную, а нейромодуляторную роль – повышают или понижают эффективность переноса информации через синапс, обслуживаемый другим нейротрансмиттером.
Нейромодуляторная роль характерна для эндорфинов и энкефалинов, число которых ограничено, но синаптические рецепторы, которые реагируют на взаимодействие с медиаторами особым, электрофизиологическим феноменом, различаются и их очень много. Различные типы нейротрансмиттеров, их рецепторов и расщепляющих ферментов группируются по-разному в разных отделах головного мозга. Уровень нейротрансмиттеров в значительной мере определяет поведенческие возможности человека - тонус, настроение и др.
ДОФАМИН (DA)
Локализуется преимущественно в среднем мозге (черная субстанция, вентральная покрышка), обонятельной луковице, гипоталамусе и перивентрикулярной области продолговатого мозга.
Производится DA в дофаминэргических нейронах из предшественника тирозина, который перемещается в нейрон активным транспортным насосом, а затем преобразуется в DA двумя из трех энзимов, которые также синтезируют норадреналин.
Разрушение DA также осуществляется теми же самыми ферментами, которые разрушают норадреналин, а именно монаминоксидазой (МАО) и катехолметилтрансферазой (COMT). DA нейрон имеет пресинаптический транспортер, который является уникальным для DA, но работает аналогично нораденалиновому и серотониновому.
Рецепторы для DA регулируют дофаминэргичекую нейропередачу. Существует множество дофаминовых рецепторов, известно, по крайней мере, пять фармакологических подтипов и несколько их молекулярных изоформ (Dn, n - цифровые обозначения подтипа). D1– находятся преимущественно в зоне черного вещества и полосатого тела, в префронтальной области; D2 – в нигростриальной, мезолимбической областях и передней доле гипофиза (секреция пролактина); D3 (пресинаптические) - в различных структурах мозга, контролируют дофаминэргическую активность по закону отрицательной обратной связи; D4 (пресинаптические) - преимущественно в нигростриарной и мезолимбической областях. Наиболее изучен D2-рецептор, по-
тому что он стимулируется дофаминэргическими агонистами и блокируется дофаминовыми антагонистами при лечении шизофрении.
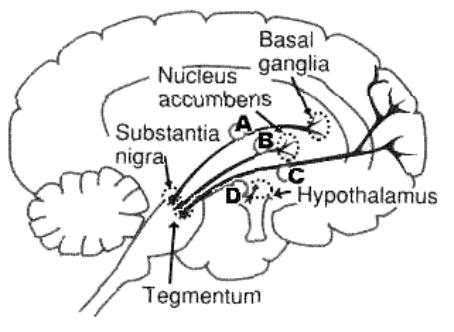
Рис. 1. Дофаминэргические проводящие пути в ЦНС.
Можно выделить несколько главных дофаминергических систем в ЦНС:
A.Нигростриальный дофаминовый путь проектируется от substantia nigra к basal ganglia и, как полагают, управляет движениями (Рис.
1).
B.Мезолимбический дофаминовый путь проектируется от средне-
го мозга (ventral tegmental area) к nucleus accumbens лимбической системы,
отвечающей за многие виды эмоционального поведения типа эффектов радости, эйфории при употреблении наркотиков, а также возникновения галлюцинаций и бреда при психозах. Антипсихотическое действие классических нейролептиков обычно связано с их дофаминблокирующей активностью в мезолимбической системе.
C.Мезокортикальный дофаминовый путь, тесно связан с мезо-
лимбическим дофаминовым путем (В). Он также проектируется от среднего мозга (ventral tegmental area), аксоны достигают дорзолатеральной и вентромедиальной префронтальной коры. Полагают, что эта система опосредует когнитивные, негативные и аффективные психопатологические симптомы при шизофрении, а также когнитивные побочные эффекты нейролептической терапии. С мезокортикальной системой связывают действие атипичных нейролептиков.
D.Тубероинфундибулярный дофаминовый путь управляет секре-
цией пролактина и проектируется от гипоталамуса до гипофиза.
СЕРОТОНИН (5-hydroxytryptamine, 5HT)
Физиологические функции серотонина чрезвычайно многообразны. Серотонин «руководит» очень многими функциями в организме, выполняет роль как нейротрансмиттера, так и гормона. 5-НТ играет важную роль в регуляции эмоционального поведения, двигательной активности, пищевого поведения, сна, терморегуляции, участвует в контроле нейроэндокринных систем, сосудистого тонуса, в процессах свёртывания крови, аллергии и воспаления, болевой чувствительности.
Локализация. Серотонинергические нейроны группируются в стволе мозга: в варолиевом мосту и ядрах шва. От моста идут нисходящие проекции в спинной мозг, нейроны ядер шва дают восходящие проекции к мозжечку, лимбической системе, базальным ганглиям, коре. При этом нейроны дорсального и медиального ядер шва дают аксоны, различающиеся морфологически, электрофизиологически, мишенями иннервации и чувствительностью к некоторым нейротоксичным агентам, например, метамфетамину.
Синтезируется серотонин из триптофана, после того как эта аминокислота транспортируется в серотониновый нейрон. Триптофановый насос сходен с серотониновым. Ферменты триптофангидроксилаза и декакорбаксилаза трансформируют триптофан в конечный продукт – серотонин, который скапливается в синаптических пузырьках до тех пор, пока не поступит нейронный импульс для его выброса.
Разрушается 5HT ферментом моноаминооксидазой (МАО), превращаясь в неактивный метаболит. Серотониновый нейрон имеет пресинаптический транспортный насос аналогичный дофаминовому (DA). Эффекты антидепрессантов в основном обусловлены блокадой обратного захвата и разрушения серотонина.
Рецепторы серотонина представлены как метаботропными, так и ионотропными. Всего насчитывается семь типов таких рецепторов (5HTn, где n – буквено-цифровые обозначения подтипа). 5-HT1-7, причем 5-НТ3 – ионотропные, остальные – метаботропные, семидоменные, связанные с G-белками.
5-HT1 тип, насчитывающий несколько подтипов: 1А-E, которые могут быть как претак и постсинаптическими, подавляет аденилатциклазу; 5-НТ4 и 7 – стимулируют; 5-HT2, насчитывающий несколько подтипов: 2А-C, которые могут быть только постсинаптическими, активирует инозитолтрифосфат. 5-HT5A подтип также подавляет аденилатциклазу.
Существует определенное сходство в строении клеточных рецепторов к серотонину и норадреналину, подобие их транспортных клеточных систем. Известно также, что норадреналин ингибирует выброс серотонина. На их связи основано действие антидепрессанта
миртазапина, который, блокируя альфа-2 рецепторы норадреналина, по принципу отрицательной обратной связи повышает содержание в синаптической щели и норадреналина, и серотонина (так как его ингибирование также тормозится) до нормы. Есть еще другие серотониновые центры в мозговом стволе, которые влияют на регуляцию цикла сна.
Серотониновые нейроны из серединного шва среднего мозга и дофаминовые нейроны из черной субстанции проецируются на базальные ганглии, где могут взаимодействовать, причем серотонин тормозит выброс дофамина.
АЦЕТИЛХОЛИН (АСh)
Основная локализация: медиальное ядро перегородки, диагональная связка, базальное гигантоклеточное ядро. Аксоны этих нейронов проецируются на гиппокамп, проходя через кору больших полушарий. Холинергические системы участвуют в таких функциях как память, регуляция движения (на уровне стриатума), уровень бодрствования (ретикулярная формация ствола мозга, базальные ганглии). В спинном мозге ацетилхолин является нейромедиатором в синапсах, образуемых a-мотонейронами на клетках Реншоу. В вегетативной нервной системе АСh – медиатор во всем парасимпатическом отделе и в преганглионарных нервных окончаниях симпатического отдела.
Синтезируется ACh в холинергических нейронах от двух предшественников: холина и ацетилкоэнзима (Ac-CoA). Холин поступает с пищей и внутринейронных источников, а Ac-CoA образуется из глюкозы в митохондриях нейрона. Эти два субстрата взаимодействуют с ферментом ацетилтрансферазой в процессе образования ацетилхолина.
Разрушается ACh ферментом ацетилхолинэстеразой (AchE), которая преобразовывает ACh в неактивные продукты. Один из них – холин, который может быть закачан назад (80%) в нейрон пресинаптическим транспортером холина, подобным транспортерам для других нейромедиаторов.
Рецепторы для ACh многочисленны. Главное их подразделение
– никотиновые (N) и мускариновые (M) холиноэргические рецепторы. Имеются также многочисленные их подтипы, лучше всего описанные для мускриновых подтипов рецептора (M1,М2, Mx). Возможно M1 постсинаптический рецептор ключевой к опосредованию функций памяти и к периферийным побочными эффектами антихолинэргических препаратов в виде сухости во рту, нечеткости зрения и др.
НОРАДРЕНАЛИН (NA)
Наряду с адреналином и дофамином относится к катехоламинам. Локализация в мосте (голубое пятно, латеральная ретикулярная формация моста), в продолговатом мозге и ядре одиночного тракта. Немногочисленные (несколько сотен) нейроны голубого пятна образуют диффузные проекции большой протяженности, достигая практически всех отделов ЦНС – коры больших полушарий, лимбической системы, таламуса, гипоталамуса, спинного мозга. В ЦНС, как правило, – тормозной медиатор (кора), реже – возбуждающий (гипоталамус). Является медиатором во всех постганглионарных симпатиче-
ских окончаниях, за исключением потовых желез.
Синтез норадреналина. Предшественником норадреналина является дофамин (он синтезируется из тирозина, который, в свою очередь – производное фенилаланина), который с помощью фермента дофамин-бета-гидроксилазы гидроксилируется (присоединяет OHгруппу) до норадреналина в везикулах синаптических окончаний. При этом норадреналин тормозит фермент, превращающий тирозин в предшественник дофамина, благодаря чему осуществляется саморегуляция его синтеза.
Разрушение норадреналина - несколько путей деградации, обеспечивающихся двумя ферментами: моноаминооксидазой-А (МАО-А) и катехол-О-метил-трансферазой (COMT). В конечном итоге норадреналин превращается либо в 4-гидрокси-3-метоксифенилгликоль (англ.) русск., либо в ванилилминдальную кислоту.
Рецепторы норадреналина. Выделяют альфа-1, альфа-2 и бетарецепторы к норадреналину. Каждая группа делится на подгруппы, различающиеся сродством к разным агонистам, антагонистам и, частично, функциями. Альфа-1 и бета -рецепторы могут быть только постсинаптическими и стимулируют аденилатциклазу, альфа-2 могут быть и пост-, и пре-синаптическими, и тормозят аденилатциклазу. Бе- та-рецепторы стимулируют липолиз.
Действие его как можно рассматривать как нейромедиатора и как гормона. Считается одним из важнейших «медиаторов бодрствования». Норадренергические проекции участвуют в восходящей ретикулярной активирующей системе. Недостаток норадреналина в мозговых структурах приводит к депрессивным состояниям, характеризующимся тоской. Норадренергические пути участвуют в модуляции активности серотонинергической системы. Как оказалось, норадренергические пути ствола от голубого пятна к серотонинергическим нейронам шва (аксонодендритическое взаимодействие) активируют высвобождение серотонина, а норадренергические пути к коре голов-
ного мозга, взаимодействуя с терминалями серотонинергических аксонов (аксоаксональное взаимодействие), напротив, тормозят высвобождение серотонина. Норадреналин принимает участие в реализации реакций типа «бей или беги», но в меньшей степени, чем адреналин. Уровень норадреналина в крови повышается при стрессовых состояниях, шоке, травмах, кровопотерях, ожогах, при тревоге, страхе, нервном напряжении. Отмечается роль норадреналина в патогенезе тревожно-фобического и обсессивно-компульсивного расстройства.
АДРЕНАЛИН
У млекопитающих мало адреналиновых путей. Адреналин секретируется диффузно (в мозговом слое надпочечников) и выполняет, в первую очередь, роль гормона.
ГИСТАМИН (H)
Представляет собой моноамин, выступающий в качестве трансмиттера. Особенно важную роль он играет как модулятор в мозге грудных детей. Гистаминергические нейроны находятся в заднем гипоталамусе и связаны со многими участками мозга, где оказывают влияние на состояние бодрствования, мышечную активность, прием пищи, сексуальные отношения и обменные процессы в мозге. Из-за участия этих нейронов в регуляции процессов сна и бодрствования многие антигистаминные препараты вызывают состояние сонливости.
Образуется путем декарбоксилирования аминокислоты гистидина. В организме существуют специфические рецепторы, для которых гистамин является естественным лигандом. В настоящее время различают три подгруппы гистаминовых (Н) рецепторов: Н1-, Н2- и Н3рецепторы.
ГЛУТАМИНОВАЯ КИСЛОТА (L-глутамат, Glu)
Является главным возбуждающим медиатором, локализуется во всех отделах ЦНС. В организме является в основном аминокислотой белкового синтеза.
Глутамат как нейромедиатор синтезируется при наличии глюкозы в митохондриях нервных окончаний, происходит дезаминирование глутамина до глутамата при помощи фермента глутаминазы. Также при аэробном окислении глюкозы глутамат обратимо синтезируется из альфа-кетоглутарата (образуется в цикле Кребса) при помощи аминотрансферазы. Синтезированный нейроном глутамат закачивается в везикулы. Глутамат выводится в синаптическую щель, откуда удаляется двумя транспортными насосами. Первый из этих насосов – пре-
синаптический глютамат-транспортер, который работает подобно всем другим транспортерам нейромедиаторов. Второй транспортный насос расположен на близлежащих астроцитах, там он трансаминируется до глутамина. Глутамин выводится снова в синаптическую щель и только тогда захватывается нейроном.
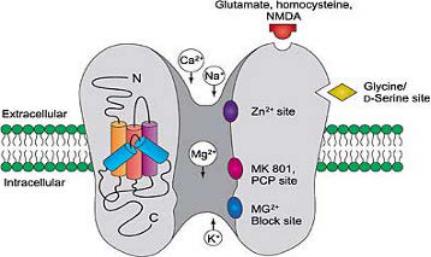
Глутаматные рецепторы. Cуществуют ионотропные (NMDAрецепторы - N-methyl-D-aspartate, AMPA-рецепторы и каинатные рецепторы) и метаботропные (mGLuR 1-8) глутаматные рецепторы. Эндогенные лиганды глутаматных рецепторов – глутаминовая кислота и аспарагиновая кислота. Для активации NMDA рецепторов также необходим глицин. Блокаторами NMDA-рецепторов являются PCP, кетамин, амантадин. Каинова кислота является активатором каинатных рецепторов (аминокислота из морских водорослей с нейротоксическим действием, разрушает тела нейронов с глутаматными рецепторами).
Глутамат, взаимодействуя с глутаматными рецепторами, увеличивает проницаемость мембраны для ионов натрия и кальция, вызывает деполяризацию и возбуждающий эффект. Из них наибольшее внимание уделяется NMDA-рецепторам (см. рис. 2), которые связаны с кальциевыми каналами. В эксперименте было показано, что блокада этих рецепторов предупреждает дегенерацию нейронов при ишемии мозга, при атрофических заболеваниях головного мозга - болезнь Альцгеймера.
Рис. 2. NMDA-рецептор.
АСПАРАГИНОВАЯ КИСЛОТА (L-аспартат)
Возбуждающий медиатор, который обнаружен преимущественно в среднем мозге, а также в переднем и заднем столбе спинного мозга. Полагают, что его действие имеет много общего с глутаматом. Глутамат и аспартат (ВАК) являются основными медиаторами возбуждения в ЦНС. С гиперактивностью соответствующих систем связывают развитие многих положительных реакций: усиление когнитивных способностей, памяти, обучения, контроля пищевого поведения и др. Снижение функциональной активности этих систем сопровождается развитием психотических реакций, что хорошо известно на примере использования препаратов, обладающих антиВАКергическим действием на уровне блокады NMDA-рецепторов (кетамин, фенциклидин, дизоцилпин и др.). При слабости ВАКергической передачи, наряду с симптомами психоза, будет присутствовать и негативная симптоматика. Этот механизм положен в основу антиглутамат/антиаспартатергической концепцией патогенеза шизофрении предложенной J.S. Kim и H.H.Kornhuber (1982).
γ-АМИНОМАСЛЯНАЯ КИСЛОТА (ГАМК, GABA)
Важнейший ингибирующий (тормозный) медиатор центральной нервной системы. ГАМК вырабатывается исключительно в головном
испинном мозгу. Не менее трети (до 50%) синапсов головного мозга используют в качестве медиатора ГАМК. Под влиянием ГАМК активируются также энергетические процессы мозга, повышается дыхательная активность тканей, улучшается утилизация мозгом глюкозы, улучшается кровоснабжение.
Синтез. Гамма-аминомасляная кислота в организме образуется из другой аминокислоты - глутаминовой с помощью фермента глутаматдекарбоксилазы.
Удаляется ГАМК из синаптической щели путем захвата пресинаптическим окончанием (около 50 %), а также клетками глии. Глия играет важную роль, как в захвате, так и в метаболизме ГАМК.
Действие ГАМК в ЦНС осуществляется путём её взаимодействия со специфическими ГАМКергическими рецепторами.
Различают три класса ГАМК-рецепторов: ионотропные ГАМК-A
иГАМК-C, и метаботропные ГАМК-B. ГАМКА-рецептор помимо сайта, связывающего ГАМК, рецепторный комплекс содержит аллостерические сайты, способные связывать бензодиазепины, барбитураты, этанол, фуросемид, нейростероиды и пикротоксин. ГАМК активирует хлорные каналы (которые отличны от хлорных каналов, активируемых глицином, тем, что не блокируются стрихнином), а бензо-
