
- •Министерство Образования и науки Российской Федерации
- •Основы теории обработки результатов.
- •Погрешности измерения.
- •Модуль 1. Механика Лабораторная работа №2 «Определение ускорения свободного падения»
- •Краткая теория
- •2. Описание установки. Порядок выполнения работы.
- •Протокол лабораторной работы №2.
- •Список рекомендуемой литературы
- •Описание установки
- •3. Порядок выполнения работы а. Проверка правильности соотношения
- •Б. Проверка правильности соотношения
- •Вопросы для самопроверки к работе №3
- •2. Порядок выполнения работы.
- •Протокол лабораторной работы №4.
- •2.Описание установки
- •3. Порядок выполнения работы
- •Протокол лабораторной работы №5
- •Понятие температуры
- •Уравнение Клапейрона–Менделеева и изопроцессы
- •2. Описание прибора
- •3. Порядок выполнения работы
- •Протокол лабораторной работы №6.
- •Вопросы для самопроверки к работе №6
- •Список рекомендуемой литературы
- •1. Описание установки.
- •1. Порядок выполнения работы
- •Протокол лабораторной работы №7
- •Вопросы для самопроверки к работе №7
- •2. Порядок выполнения работы.
- •Протокол лабораторной работы №8
- •Вопросы для самопроверки к работе №8
- •Порядок выполнения работы.
- •Данные установки
- •Протокол лабораторной работы №9
- •Обработка результатов измерений
- •Прилагается к данной работе:
- •Порядок выполнения работы
- •Данные установки
- •Протокол лабораторной работы №10
- •Обработка результатов измерений
- •Вопросы для самопроверки к работе №10
- •Описание аппаратуры и порядок выполнения работы
- •Вопросы для самопроверки к работе №11
- •Порядок выполнения работы.
- •Описание метода измерения и установки.
- •Порядок выполнения работы.
- •Протокол лабораторной работы №15
- •Вопросы для самопроверки к работе №15
- •Принцип Гюйгенса
- •Принцип Гюйгенса – Френеля
- •Метод зон Френеля
- •Дифракция от щели в параллельных лучах
- •Дифракционная решетка
- •Лабораторная установка и порядок проведения работы
- •Часть I
- •Часть II
- •Протокол лабораторной работы №24
- •Вопросы для самопроверки к работе №24
- •Поляризация при отражении и преломлении
- •Поляризация при двойном лучепреломлением
- •Поляризационная призма Николя
- •Закон Малюса
- •Порядок выполнения работы
- •Протокол лабораторной работы №25
- •Внешний фотоэффект, законы Столетова.
- •Внешний фотоэффект и волновая теория света
- •Уравнение Эйнштейна для внешнего фотоэффекта
- •Внутренний фотоэффект
- •Типы фотоэлементов
- •Порядок выполнения работы
- •Протокол лабораторной работы №28
- •Вопросы для самопроверки к работе №28
- •Дисперсия света
- •Сериальные формулы
- •Ядерная модель строения атома по Резерфорду
- •Затруднения теории Резерфорда
- •Понятие о квантах и постоянная Планка
- •Постулаты Бора
- •Волны де Бройля
- •Линейчатые спектры по теории Бора
- •Энергетические уровни в атоме
- •Вывод расчетной формулы
- •Описание установки и порядок выполнения работы
- •Порядок выполнения работы
- •Протокол лабораторной работы №26
- •Протокол лабораторной работы №30 Вопросы для самопроверки к работе №30 Список рекомендуемой литературы
- •Правила оформления результатов выполнения заданий по каждой работе Лабораторного практикума
Уравнение Клапейрона–Менделеева и изопроцессы
Пусть
некоторый газ переходит из состояния,
определяемого параметрами
![]() ,
в состоянии с
,
в состоянии с![]() .
Указанные параметры связаны равенством
.
Указанные параметры связаны равенством
![]() (6)
(6)
Это равенство называют уравнением состояния. Оно принимает простой вид, если массу газа выразить в молях.
Молем
называют количество вещества, содержащее
столько же структурных элементов,
сколько содержится атомов в углероде
![]() массой 0,012кг.
массой 0,012кг.
Моль
любого вещества при нормальных условиях
(давление 760 мм. рт. ст. и температура
![]() )
занимает одинаковый для всех газов
объём – 22,4 литра. Следовательно, для
одного моля полученное уравнение (6)
имеет вид:
)
занимает одинаковый для всех газов
объём – 22,4 литра. Следовательно, для
одного моля полученное уравнение (6)
имеет вид:
![]()
Полученную постоянную величину обозначают буквой R
![]()
и называют молярной газовой постоянной.
Очевидно,
что для
![]() молей газа получим
молей газа получим
![]() или
или
![]() ,
(7)
,
(7)
где т – масса газа;
М – молярная масса данного газа;
![]() –число
молей газа.
–число
молей газа.
Это уравнение называют уравнением Клапейрона–Менделеева.
Процессы в газах, протекающие при неизменности какого–либо параметра, называют изопроцессами.
Процесс, протекающий при неизменной температуре, называется изотермическим. Уравнение изотермического процесса (закон Бойля–Мариотта) записывается так:
![]() ,
(8)
,
(8)
где
![]()
![]() – давление объём данной массы газа в
начальной и конечном состояниях.
– давление объём данной массы газа в
начальной и конечном состояниях.
Процесс, протекающий при неизменном давлении, называется изобарическим. Уравнение изобарического процесса (закон Гей–Люссака) может быть представлен в виде:
![]() или
или
![]() ,
(9)
,
(9)
где
![]() – объём газа при
– объём газа при![]() ;
;
![]() –объём
того же газа при температуре Т;
–объём
того же газа при температуре Т;
![]() –термический
коэффициент объёмного расширения газа,
одинаковый для всех газов:
–термический
коэффициент объёмного расширения газа,
одинаковый для всех газов:
![]() .
.
Величину
![]() называют биномом объёмного расширения.
называют биномом объёмного расширения.
Процесс, протекающий при неизменном объёме, называется изохорическим. Уравнение изохорического процесса называют уравнением Шарля
![]() или
или
![]() (10)
(10)
где
![]() – термический коэффициент давления.
– термический коэффициент давления.
Для идеальных газов, т.е. газов, точно подчиняющихся законам Бойля–Мариотта и Гей–Люссака,
![]() (11)
(11)
На
рис. 1 показаны графики изопроцессов в
координатах
![]() .
.

2. Описание прибора
Одним из приборов для измерения температуры является газовый термометр.
Стеклянный баллон А (рис. 2), опущенный в сосуд С с водой, соединён капиллярной трубкой В с манометром М1М2. Трубка имеет кран К. Оба колена манометра соединены резиновой трубкой Е. В трубке М1 имеется указатель У (стеклянное острие или метка). Для сохранения постоянного объёма газа в баллоне А каждый раз перед отсчётом давления надо подводить уровень жидкости до соприкосновения с остриём У или меткой.
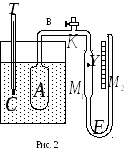
Изменение уровня жидкости в левом колене производится перемещение правого колена М2. Температура жидкости измеряется термометром Т.
3. Порядок выполнения работы
1. Наполняют сосуд С водой и опускают в него баллон А.
2.
Открывают кран К,
поднимая или опуская правое колено М2
манометра,
подводят уровень жидкости в левом колене
под остриё У или метку. При открытом
кране К
давления воздуха в баллоне равно
атмосферному. Обозначают его Р
и определяют по барометру. Температуру
![]() воздуха в баллоне принимают равной
температуре воды и записывают в таблицу.
воздуха в баллоне принимают равной
температуре воды и записывают в таблицу.
3.
Закрывают кран К
и включают нагреватель. Нагрев воду
примерно на
![]() ,
выключают нагреватель. Перемешивая
воду, ожидают пока температура воды
перестанет повышаться.
,
выключают нагреватель. Перемешивая
воду, ожидают пока температура воды
перестанет повышаться.
4.
Приведя уровень жидкости в левом колене
опять в соприкосновение с острием или
меткой, измеряют температуру воды
(воздуха в баллоне)
![]() и разность уровней жидкости в коленах
манометра
и разность уровней жидкости в коленах
манометра![]() .
Результаты измерений записывают в
таблицу.
.
Результаты измерений записывают в
таблицу.
5.
Нагревают воду ещё на
![]() и повторяют те же операции, которые
указаны в пунктах 3 и 4. Опыт повторяют
не менее 5 раз примерно через равные
интервалы температур. Полученные
значения
и повторяют те же операции, которые
указаны в пунктах 3 и 4. Опыт повторяют
не менее 5 раз примерно через равные
интервалы температур. Полученные
значения![]() и
и![]() откладывают (рис. 3) на графике и по
полученным точкам строят прямую,
проходящую через начало координат. Взяв
какую–либо точку на этой прямой, легко
найти отношение
откладывают (рис. 3) на графике и по
полученным точкам строят прямую,
проходящую через начало координат. Взяв
какую–либо точку на этой прямой, легко
найти отношение![]() ,
а зная отношение
,
а зная отношение![]() можно вычислить величину
можно вычислить величину![]() .
Если жидкость в манометре заменить
другой жидкостью плотностью
.
Если жидкость в манометре заменить
другой жидкостью плотностью![]() ,
то коэффициентс
нужно заменить на
,
то коэффициентс
нужно заменить на
![]() .
.

