
Краткий_курс_лекций_Таганович_Кухта
.pdfствуют в поддержании нормальной функции дыхательного центра, оказывают инотропный и хронотропный эффекты на сердце, увеличивают количество β-адренергических рецепторов в сердечной и скелетной мыщцах, жировой ткани и лимфоцитах, увеличивают образование эритропоэтина и повышают эритропоэз, стимулируют моторику желудочно-кишечного тракта, стимулируют синтез многих структурных белков в организме. Суммарный эффект T4 и T3 оценивается по изменению скорости потребленияO2 тканями, отражающей интенсивность метаболических процессов в них. Повышение потребления О2 под действием тиреоидных гормонов связано с усилением окисления жирных кислот. Гормоны ЩЖ увеличивают активность мембраносвязанной Na+-K+-ATФазы клеток, влияя тем самым на механизмы активного транспорта веществ. Давно известен разобщающий эффект T4 на процесс тканевого дыхания в митохондриях.
Зоб. Увеличение ЩЖ — это «попытка» организма компенсировать сниженное образование тиреоидных гормонов. Гипотиреоз — это состояние, развивающееся при нарушении синтеза или транспорта гормонов ЩЖ (особенно характерно снижение основного обмена). Гипотиреоз у плода и новорожденного приводит к нарушению роста, тяжелой необратимой задержке умственного развития (кретинизму). Гипотиреоз у детей старшего возраста проявляется отставанием в росте без задержки умственного развития. Гипертиреоз (тиреотоксикоз) возникает при гиперпродукции гормонов ЩЖ. Наиболее известная патология — базедова болезнь.
ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
Инсулин (I) — анаболический гормон, способствующий сохранению глюкозы, жирных кислот и аминокислот. Глюкагон, наоборот, — катаболический: он мобилизует глюкозу, жирные кислоты и аминокислоты из тканевых запасов в кровоток. Эти два гормона функционально взаимосвязаны.
I — полипептид, состоящий из двух цепей: А-цепь содержит 21 аминокислоту, B-цепь
— 30. Обе цепи связаны двумяS-S-мостиками. I человека отличается от инсулина свиньи только одной аминокислотой. Синтез I проходит по законам синтеза секретируемых белков.
Эффекты I многообразны, имеют временную зависимость: 1) быстрый (секунды) — ускорение транспорта глюкозы, аминокислот и калия в инсулинзависимые ткани; 2) промежуточный (минуты) — стимуляция синтеза белков и торможение их распада, активирование ферментов гликолиза и гликогенсинтазы, угнетение ферментов глюконеогенеза и фосфорилазы; 3) длительный (часы) — увеличение синтеза иРНК, ферментов липогенеза и др. Результирующий эффект влияния I — накопление углеводов, белков и жиров. Эффекты I тканеспецифичны.
Комплекс нарушений, вызванных недостаточностью функцийI, называется сахарным диабетом. Диабет характеризуется полиурией, полидипсией, потерей веса (при увеличенном аппетите), гипергликемией, глюкозурией, кетозом, ацидозом, которые нередко заканчиваются комой. Избыток внеклеточной глюкозы сопровождается её внутриклеточным дефицитом — «голодание среди изобилия», уменьшением поступления аминокислот в мышцы и увеличением скорости липолиза. Характерный признак диабета — гипергликемия, которая заметно проявляется после еды, поэтому после глюкозной нагрузки концентрация глюкозы в плазме у больного диабетом значительно выше, чем у здорового, а возвращение к начальному уровню проходит медленнее. Гипергликемия >10 ммоль/л превышает реабсорбционные возможности почек и становится причиной глюкозурии. Выделение oсмотически активных молекул глюкозы влечет за собой потерю больших количеств воды(осмотический диурез). Длительная гипергликемия способствует неферментативному гликозилированию белков. Определение уровня гликозилированной формы гемоглобина HbA1С используется для оценки эффективности лечения инсулином. Основные нарушения обмена липидов при диабете: усиление катаболизма липидов, увеличение образования кетоновых тел, снижение синтеза жирных кислот и триацилглицеролов. В силу недостаточости I нарушается гликолиз
94
и стимулируется образование глюкозы из белков (глюконеогенез). Потребности в энергии удовлетворяются катаболизмом белков и жиров. Развивается белковая недостаточность. Больной теряет вес. В кровотоке накапливаются кетоновые тела, так как скорость их образования превышает возможности клеток по их использованию. Это приводит к развитию метаболического ацидоза. К дегидратации добавляются потери Na+ и K+.
Выделяют две формы диабета: 1) I-зависимый сахарный диабет (диабет 1-го типа), развивается вследствие дефицитаI, вызываемого аутоиммунным разрушением β-клеток pancreas; 2) I-независимый сахарный диабет (диабет 2-го типа), характеризуется устойчивостью к I и сниженной секрецией I. Он встречается чаще, развивается у пожилых лиц.
Глюкагон — пептид (29 аминокислот), синтезируемый α-клетками pancreas. Он действует через 7-TMС-(R). Гормон усиливает распад гликогена за счёт активации гликогенфосфорилазы (с участием цАМФ) и фосфолипазы C (увеличивая уровень цитоплазматического Ca2+). Гликогенолиз стимулируется в печени, но не в мышцах. Глюкагон — мощный стимулятор липолиза. Повышая содержание цАМР в адипоцитах, он активирует гормончувствительную липазу. Образующиеся при этом в большом количестве жирные кислоты могут использоваться в качестве источников энергии или превращаться в кетоновые тела. Глюкагон стимулирует глюконеогенез.
Основной регулятор секреции глюкагона — глюкоза: увеличение в ответ на гипогликемию и снижение при повышении уровня глюкозы в крови; секреция гормона возрастает также при потреблении белков.
|
|
|
|
СТЕРОИДНЫЕ ГОРМОНЫ |
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
Структурные |
особенно- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
Стероидные гормоны |
|
|
|
|
|
|
|
|
||||||||||||||
сти различных стероидных гор- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Радикал |
|||||||||||||
монов |
можно |
иллюстрировать |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
в положении С17 |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
следующей схемой: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
Эстрогены и |
|
|
|
|
|
|
Другие |
|
|
|
|
||||||||||
|
Синтез |
гормонов |
коры |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
андрогены |
|
|
|
|
|
|
стероиды |
|
|
|
|
||||||||||||||
надпочечников. В |
гломеруляр- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
ной зоне синтезируются мине- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
Фенольное |
|
|
|
|
|
-СН3 в |
|
|
|
|
-СН2ОН в |
|||||||||||||||
ралокортикоиды, |
в |
пучковой |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
(средней) — глюкокортикоиды, |
|
|
А-кольцо |
|
|
|
|
|
С21 |
|
|
|
|
С21 |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
в ретикулярной |
сосредоточены |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Эстрогены |
|
|
Андрогены |
|
Прогестерон |
|
|
Кортикосте- |
|
|
|||||||||||||||||
ферменты для синтеза андроге- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
роны |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
нов. |
Общими в |
синтезе |
всех |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-СНО в |
||||||||||
стероидных гормонов |
являются |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С19 |
||||||||
первые две реакции: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Альдостерон |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
1. Превращение холестерола в прегненолон в результате отщепления |
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||
|
6Сфрагмента |
|
|||||||||||||||||||||||||
от боковой цепи (фермент С20-22 десмолаза). Десмолаза — ключевой фермент в биосинтезе стероидов. Его фосфорилирование (активацию) стимулирует АКТГ.
С |
С22 |
|
|
СН3 |
|
|
С20 |
С |
С |
АКТГ |
С=О |
|
|
|
|
|
|
|||
|
С С |
|
|
|
||
|
С |
(цАМФ) |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
С20-22 |
|
|
|
|
|
|
Десмолаза |
+ |
Н |
С |
|
|
|
|
О С-С-С-С |
С |
|
НО |
|
|
|
НО |
|
|
Холестерол |
|
|
|
Прегненолон |
С6 альдегид |
|
95
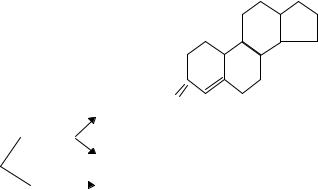
2. Окисление и изомеризация прегненолона в прогестерон. Прегненолон является
предшественником всех стероидных гормонов. |
|
|
|
|
|
|
СН3 |
|||
В желтом теле (в яичниках) синтез стероидов останавлива- |
Прогестерон |
| |
||||||||
ется на этапе образования прогестерона. Во всех других стероид- |
С=О |
|||||||||
|
|
|
|
|||||||
продуцирующих тканях прогестерон является только промежуточ- |
|
|
|
|
||||||
|
|
|
|
|||||||
|
|
|
|
|||||||
ным продуктом синтеза других стероидов. |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|||
Превращения прогестерона. Сначала прогестерон подверга- |
|
|
|
|
||||||
|
|
|
|
|||||||
ется гидроксилированию в положениях С-17 или С-21, в результа- |
|
|
|
|
||||||
|
|
|
|
|||||||
те чего образуются различные функциональные классы стероидов. |
|
|
|
|
||||||
|
|
|
|
|
|
|
О |
|
|
|
|
|
|
|
|
|
секс стероиды |
|
|
||
17-гидроксила за |
|
|
|
глюкоко ртикоиды |
|
|
||||
|
|
|
|
|
||||||
П р огестерон |
|
|
|
|
|
|
|
|||
|
|
|
|
|
минера локортикоиды |
|
|
|||
21-гидроксила за |
|
|
|
|
|
|||||
|
|
|
|
|
||||||
Гидроксилирование прогестерона в положении С-21 или С-11 приводит к образованию минералокортикоидов, в С-17 — глюкокортикоидов.
Функция минералокортикоидов (альдостерона) заключается в реабсорбцииNa+ в дистальных канальцах почек (о механизмах рецепции стероидных гормонов см. выше).
Глюкокортикоиды (кортизол и гидрокортизон) оказывают катаболическое влияние на скелетные мышцы и анаболическое — на печень, где они стимулируют синтез ферментов глюконеогенеза, в результате чего уровень глюкозы в крови повышается. Кроме того, глюкокортикоиды регулируют реакции иммунитета и в терапевтических дозировках оказывают выраженное противовоспалительное действие.
Регуляция синтеза кортикостероидов: как указывалось, ключевой фермент синтеза стероидов — С20–22 десмолаза. Важнейшим регулятором синтеза альдостерона является ангиотензин II — пептид, образующийся из белка плазмы в результате отщепления от него двух олигопептидов: вначале под действием ренина образуется ангиотензин I, затем под действием ангиотензинпревращающего фермента из ангиотензина I образуется ангио-
тензин II. Ангиотензин II связывается с поверхностью клеток клубочковой зоны коры надпочечников и стимулирует фосфорилирование С20–22 десмолазы.
На секрецию кортизола влияют АКТГ, физический и эмоциональные стрессы, состояние тревоги, страха, волнения и боль. Эти реакции могут нивелировать воздействия системы отрицательной обратной связи и суточного ритма. Свободные глюкокортикоиды ингибируют секрецию АКТГ.
Глюкокортикоиды в высоких концентрациях нашли широкое применение длялечения аутоиммунных заболеваний или для подавления реакции отторжения при пересадке тканей. Высокие дозы глюкокортикоидов подавляют воспалительную реакцию.
Недостаточность ферментов, катализирующих синтез кортикостероидов, ведет к гиперплазии надпочечников. При избытке глюкокортикоидов развивается синдром Кушинга. Основные проявления этого синдрома вызваны усилением распада белков. Отмечается своеобразное отложение жира: ожирение туловища и «лунообразное» лицо, в то время как подкожножировая клетчатка конечостей атрофируется. Недостаточность надпочечников проявляется Аддисоновой болезнью (внешнее проявление — гиперпигментация кожи).
ПОЛОВЫЕ ГОРМОНЫ
Изменения секреции половых гормонов оказывают существенное влияние на интенсивность метаболических процессов и лежат в основе развития организма и механизмов старения. Половые гормоны действует через внутриклеточные рецепторы
96
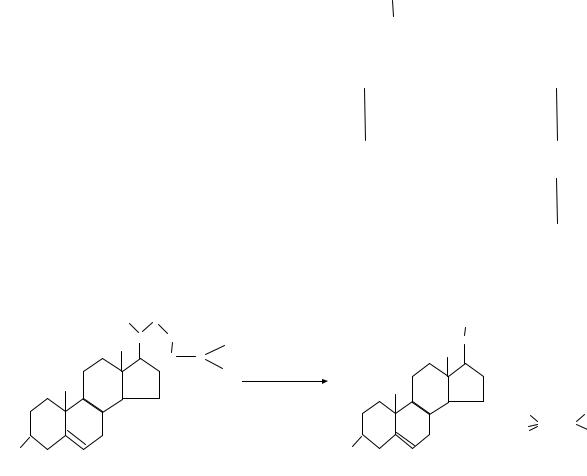
Синтез андрогенов в яичках. Вначале из прегненолона (или прогестерона) при участии 17-гидроксилазы образуется С17-ОН производное — 17-ОН прегненолон (17-ОН про-
гестерон).
Затем от Д-кольца отщепляется боковая цепь с помощью С17–20 лиазы. При этом обра-
зуются мужские половые гормоны дигидроэпиандростерон, андостендион и тестосте-
рон, которые могут взаимопревращаться друг в друга под действием изомеразы. Важнейшим мужским половым гормоном являетсятестостерон. Однако в большинстве периферических тканей основным активным андрогеном являетсядигидротестостерон, рецепторы для которого обнаружены в простате, семенных пузырьках, коже гениталий и наружных половых органах. Фермент, катализирующий превращение тестостерона в дигидротестостерон, называется 5-a-редуктазой.
Синтез мужских половых гормонов стимулирует лютеинизирующий гормон гипофиза, синтез и секреция которого, в свою очередь, регулируется гонадолиберином.
О Н |
|
О Н |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5-a-редуктаза НАДФН.Н+
|
О |
|
|
О |
Н |
||
|
Т е с т о с т е р о н |
Д и г и д р о т е с т о с т е р о н |
|
|
|
||
|
|
|
( Д Г Т ) |
Мужские половые гормоны влияют на дифференцировку тканей, развитие вторичных половых структур, участвуют в процессах сперматогенеза. Они оказывают выраженное анаболическое действие, усиливая процессы синтеза белков, что выражается в увеличении мышечной массы, росте костей; способствуют задержке натрия, калия, воды, кальция, сульфата и фосфата.
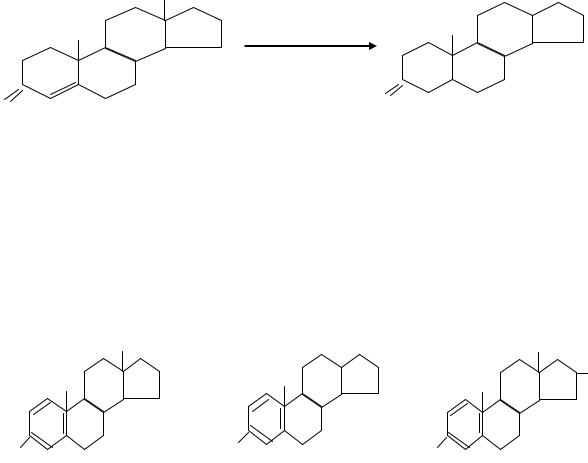
Синтез эстрогенов в клетках яичников. Субстратами для синтеза эстрогенов являются андрогены. Синтез эстрогенов регулируют лютеинизирующий гормон и гонадолиберин.
ОН |
|
О |
ОН |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ОН
НО |
НО |
|
НО |
|
Эстрон |
||
17b-эстрадиол |
|
Эстриол |
|
|
|
К эстрогенам относятся также эстрон и эстрадиол. Эстрогены регулируют синтез белков. Подобно другим стероидам эстрогены, проникая в клетку, взаимодействуют с внутриклеточным рецептором. Комплекс гормон – рецептор затем связывается со специфической нуклеотидной последовательностью на ДНК и регулирует синтез иРНК.
Транспорт стероидных гормонов осуществляется с помощью белков-переносчиков, синтезируемых в печени. Это — транскортин (белок, связывающий кортикостероиды) и секс- стероид-связывающий белок. Неспецифический транспорт осуществляется альбуминами.
Катаболизм стероидных гормонов. В клетках организма отсутствуют ферменты, которые раскрывали бы стероидную циклическую структуру, но имеются механизмы, посредством которых циклическая структура приобретает растворимость в водной среде и за счет этого становится возможным её экскреция из организма. Этими механизмами являются:
97
1) восстановление двойных связей в составе циклической структуры; 2) реакции конъюгации с УДФ-глюкуроновой кислотой или ФАФС(глюкуроновая кислота или активный сульфат связываются с ОН-группой в составе стероидной циклической структуры) — эти конъюгаты растворимы.
БИОХИМИЯ ПИТАНИЯ. МАКРО- И МИКРОЭЛЕМЕНТЫ
Все минеральные вещества в зависимости от их концентрации, подразделяются на макро- и микроэлементы. Содержание макроэлементов превышает 50 мг/кг массы тела (натрий и калий, кальций, магний, фосфат, хлорид, сульфат). Содержание микроэлементов составляет менее 50 мг/кг массы тела (медь, цинк, селен, кобальт и др.). К микроэлементам относят также и железо, хотя его концентрация превышает указанную величину.
МАКРОЭЛЕМЕНТЫ
Электролиты К+ и Na+ важны для поддержания электролитного баланса, надлежащего осмотического давления; они создают определённые условия растворимости, участвуют в механизмах возбудимости, влияют на обменные процессы путём активирования или ингибирования ферментов, используются в процессах минерализации костей скелета и зубов.
Концентрация электролитов вне и внутри клетки существенно различается: натрий и кальций преобладают во внеклеточном пространстве, калий и магний — внутри клетки.
Кальций
Общее содержание кальция в плазме крови — 2,2–2,7 ммоль/л. Половину составляет диффузионный Са2+ (способен проходить через биомембраны), часть Са2+ связана с белками крови (недиффузионный кальций), некоторое количество находится в составе цитратов и фосфатов плазмы крови. Основное депо кальция — Са-апатиты костной ткани. Кальций всасывается из кишечника в кровь с помощью специального Са2+-связывающего протеина, синтезируемого слизистой кишечника. Этот белок осуществляет свою функцию совместно с
2+ 2+
Са -зависимой АТФ-азой. Стимулятором синтеза Са -связывающего протеина является 1,25-(ОН)2-D3 (кальцитриол, витамин D3).
Роль кальция в организме. Соли кальция составляют основу скелета и зубов. Ионы кальция принимают участие в многочисленных процессах: регуляции нервно-мышечной возбудимости, сократительной и секреторной активности, проницаемости клеточных мембран. Са2+ активирует процесс свёртывания крови, адгезию и рост клеток. Наряду с циклическими нуклеотидами Са2+ считается вторичным посредником в реализации механизма действия гормонов.
Регулируется уровень кальция в крови гормонами-антагонистами: паратирином и тиреокальцитонином, а также витамином D.
Кальцитонин
Кальцитонин секретируется С-клетками щитовидной железы (ЩЖ). Это — полипептид (32 аминокислоты). Регулятор секреции — повышение концентрации Са++ в крови более 2,25 ммоль/л. Основной эффект гормона — снижение уровней Са++ и фосфора в крови. Он ускоряет минерализацию костной ткани и стимулирует включение в неё фосфора, ингибирует активность и уменьшает количество остеокластов. В почках гормон, связываясь с 7-ТМС-(R), которые расположены в дистальных канальцах, усиливает выведение фосфатов и кальция.
98
Паратирин (паратгормон)
Гормон синтезируется паращитовидными железами. Он является полипептидом (84
++
аминокислоты). Краткосрочная регуляция секреции паратгормона осуществляется Са , а в течение длительного времени — 1,25(ОН)2D3 cовместно с кальцием.
Паратгормон взаимодействует с 7-ТМС-(R), что приводит к активации аденилатциклазы и повышению уровня цАМФ. Помимо этого, в механизм действия паратгормона включаются Са++, а также ИТФ и диацилглицерол (ДАГ). Основная функция паратгомона за-
++
ключается в поддержании постоянного уровня и Са . Эту функцию он выполняет, влияя на кости, почки и (посредством витамина D) кишечник. Влияние паратгормона на остеокласты ткани осуществляется в основном черезИТФ и ДАГ, что в конечном итоге стимулирует распад кости. В проксимальных канальцах почек паратгормон угнетает реабсорбцию фосфатов, что ведет к фосфатурии и гипофосфатемии, он увеличивает также реабсорбцию кальция, т. е. уменьшает его экскрецию. Кроме того, в почках паратгормон повышает активность 1-гидроксилазы. Этот фермент участвует в синтезе активных форм витамина D.
Поступление кальция в клетку регулируется нейрогормональными сигналами, одни из
+
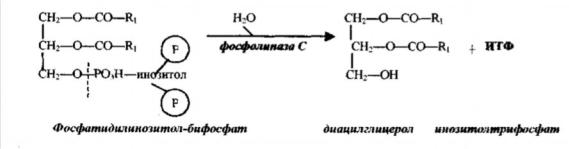
которых увеличивают скорость вхождения Са в клетку из межклеточного пространства, другие — высвобождения его из внутриклеточных депо. Из внеклеточного пространства Са2+ попадает в клетку черезкальциевый канал (белок, состоящий из 5 субъединиц). Кальциевый канал активируется гормонами, механизм действия которых реализуется через цАМФ. Высвобождение Са2+ из внутриклеточных депо происходит под действием гормонов, активирующих фосфолипазу С — фермент, способный гидролизовать фосфолипид плазматической мембраны ФИФФ (фосфатидилинозитол-4,5- бифосфат) на ДАГ (диацилглицерол) и ИТФ (инозитол-1,4,5-трифосфат):
ИТФ присоединяется к специфическому рецептору кальцисомы(где Са2+ аккумулируется). При этом изменяется конформация рецептора, что влечёт за собой открытие ворот, запиравших канал для прохождения Са2+ из кальцисомы. Высвободившийся из депо кальций связывается с протеинкиназой С, активность которой увеличивает ДАГ. Протеинкиназа С, в свою очередь, фосфосфорилирует различные белки и ферменты, изменяя тем самым их активность.
Ионы кальция действуют двумя путями: 1) связывают отрицательно заряженные группы на поверхности мембран, изменяя тем самым их полярность; 2) связываются с белком калмодулином, активируя тем самым множество ключевых ферментов обмена углеводов и липидов.
Недостаток кальция приводит к развитиюостеопороза (хрупкости костей). К недостатку кальция в организме приводят дефицит его в пище и гиповитаминоз Д.
Суточная потребность — 0,8–1,0 г/сут.
В обмене кальция наряду с паратирином и тиреокальцитонином исключительно важную роль играет витамин Д.
Витамин Д (кальциферол), антирахитический
В животных жирах содержится холекальциферол (витамин Д3), в растительных — эргокальциферол Д2 (кальциферол означает несущий кальций). В организме человека витамин
99
Д3 образуется |
в |
качестве |
промежуточного |
продукта |
при |
биосинтезе |
холестерол |
(из 7-дегидрохолестерола) в клетках кожи под влиянием УФ-лучей. |
|
|
|
||||
Метаболизм. Кальциферолы поступают в печень в составе хиломикронов. В печени |
|||||||
образуется 25(ОН)-Д3, т. е. 25-гидроксихолекальциферол, затем 25(ОН)-Д3 попадает в |
|||||||
кровь и, связываясь |
специфическим транспортным белком, переносится в почки. В почках |
||||||
образуется 1,25(ОН)2-Д3 (1,25-дигидроксихолекальциферол, или кальцитриол). Эта реакция активируется паратиреоидным гормоном. В реакциях гидроксилирования принимает участие витамин С. Витамин Д3 накапливается в жировой ткани.
Биохимические функции. Витамин Д3 можно рассматривать как прогормон, так как его действие во многом сходно с действием стероидных гормонов. Так, проникая в клеткимишени, он связывается с белковыми рецепторами, которые мигрируют в ядро клетки. В энтероцитах этот гормон-рецепторный комплекс стимулирует транскрипцию иРНК, передающую информацию для синтеза белка-переносчика ионов кальция. При этом всасывание кальция осуществляется как путём облегченной диффузии с участием этого переносчика, так и путём активного транспорта(с помощью Са2+-АТФ-азы). Одновременно ускоряется и всасывание фосфора.
Кроме кишечника органом-мишенью активной формы витамина Д являетсякостная ткань, где 1,25(ОН)2-Д3 стимулирует процесс деминерализации (синергично с паратирином).
Активация витамином 1,25(ОН)2-Д3 кальциевой АТФ-азы мембран почечных -ка нальцев приводит к увеличению реабсорбции Са2+; возрастает и реабсорбция фосфатов.
Кальцитриол принимает также участие в регуляции роста и дифференцировке клеток костного мозга. Он обладает антиоксидантным и антиканцерогенным действием.
Гиповитаминоз. Недостаток витамина Д у детей приводит к заболеваниюрахитом. Основные проявления этого заболевания сводятся к симптоматике недостаточности кальция. У взрослых недостаточность кальция в организме приводит к кариесу остеомаляции (размягчение кости); у пожилых — к развитию остеопороза (снижение плотности костной ткани вследствие нарушения остеосинтеза).
Гипервитаминоз Д. Избыточный приём витамина Д приводит к интоксикации и -со провождается выраженной деминерализацией костей — вплоть до их переломов. Содержание кальция в крови повышается. Это приводит к кальцификации мягких тканей, особенно почек (вторичный гиперпаратиреоидизм).
Суточная потребность для детей колеблется от 10 до 25 мкг (500–1000 МЕ), у взрослых она ниже. Витамин Д3 содержится исключительно в животной пище. Богаты им рыбий жир, печень, желток яиц. В растительных маслах, молоке, дрожжах присутствует витамин Д2 (биологически он менее активен).
Фосфор
Наибольшее его количество (85 %) находится в костной ткани. Фосфор — важнейший вне- и внутриклеточный анион. Внутри клетки он связан с белками и липидами («органический фосфор»). Фосфор внеклеточного пространства находится в виде одно- и двузамещённых фосфатов, образующих в плазме крови буферную систему(поддержка нормы рН). Фосфор является одним из ингредиентов, определяющих буферные свойства мочи.
Участие в метаболизме. Органический фосфор входит в состав нуклеиновых кислот, коферментов, фосфолипидов, он служит энергоносителем, входит в состав вторичных посредников гормонов, участвует в образовании коферментной формы водорастворимых витаминов. В клетках путём фосфорилирования осуществляется регуляция активности регуляторных ферментов.
Обмен фосфора тесно связан с процессами поступления и освобождения из костей кальция: увеличение поступление Са2+ в организм приводит к повышению выведения фосфора с мочой. Контроль внеклеточной концентрации фосфора осуществляется почками: под влиянием паратирина реабсорбция фосфатов снижается. Основными причинами гипофосфа-
100
темии являются гиперпаратиреоидизм, врожденный дефект реабсорбции фосфора в почках, недостаточность питания, онкологические заболевания.
Суточная потребность составляет около 1 г.
МИКРОЭЛЕМЕНТЫ
Железо
Содержание железа в организме— 3–5 г, наибольшее его количество (2/3) приходится на гемоглобин, 4,5 % — на миоглобин, 2 % находится в составе ферментов. Оно может быть геминовым (железо гема и других порфиринов) либо негеминовым (в составе фермента аконитазы и железосерных белков, входящих в комплексы дыхательной цепи). Fe принимает участие в связывании, транспорте и депонировании О2 (гемоглобин и миоглобин), в транспорте электронов в дыхательной (цитохромыепи), в окислительно-вос- становительных реакциях (некоторые оксидоредуктазы), реакциях гидроксилирования (цитохром Р450) и обезвреживания перекисей (каталаза и пероксидазы).
Железо всасывается в верхней части тонкого кишечника. При возрастании потребности в нём (кровопотери) Fe всасывается эффективнее. Улучшает всасывание железа витамин С. Фосфаты и фитаты зерновых растений затрудняют его всасывание. Из просвета кишечника свободное железо захватываетсямуцином слизистой. Интегрин на поверхности мембраны щёточной каёмки энтероцита облегчает транспортFe внутрь клетки, где железо связывается с белком мобилферрином. Этот белок «собирает» железо изо всех отсеков цитозоля энтероцита и переносит Fe в кровь, где Fe3+ сразу же связывается с белкомапотрансферрином — образуется трансферрин (гликопротеин). Трансферрин, помимо транспортной функции, защищает также ткани от токсического действия свободных ионов железа. Затем, связываясь со специфическим мембранным рецептором, трансферрин поступает вместе с ним в клетки кроветворных органов. После освобождения от Fe трансферриновый рецептор возвращается в плазматическую мембрану.
В клетках печени, костного мозга и селезёнки железо связывается с апоферритином. Этот белок состоит из 24 субъединиц, формирующих 6 каналов, через которые в центральную часть молекулы поступают ионы железа. 1 молекула апоферритина может заключать в себе до 4,5 тысяч атомов железа. Апоферритин, связанный с Fe, называется ферритином. Железо может быть снова использовано только после распада ферритина. При загрузке депо (феррритина) Fe откладывается в виде нерастворимого комплекса — гемосидерина.
Физиологические потери железа при обновлении эпителия кишечниканезначительны. Особенностью обмена Fe является неспособность организма экскретировать его большие количества. В норме между скоростью всасывания и выведения железа существует равновесие. Существенный дефицит железа может возникать при кровопотере (с 1 мл крови теряется 0,5 мг Fe). Недостаток Fe возникает также при потреблении бедной железом пищи
и нарушениях его всасывания. В результате развивается железодефицитная гипохромная анемия. Избыточное отложение Fe в виде гемосидерина в клетках печени и селезёнки отмечается при переливании больших объёмов крови или гемолизе эритроцитов.
Суточная потребность в железе для взрослых— 1–2 мг. Однако всасывается лишь 10 % содержащегося в рационе питания Fe.
Медь
Всасываясь из слизистой кишечника, медь в портальном кровотоке адсорбируется альбуминами и белком транскупреином и поступает в печень — центральный орган обмена меди. В печени медь либо запасается, либо включается в Cu-содержащие ферменты. В плазме крови Cu связывается с ферментом церулоплазмином (α2-глобулин), имеющим голубую окраску. Церулоплазмин обладает оксидазной активностью(окисляет аскорбиновую кислоту, адреналин, ДОФА и др.). Он играет ведущую роль во взаимосвязи обмена Cu и Fe.
101
Роль меди в обмене веществ. Медь входит в состав многих ферментов: цитохромоксидазы (фермент дыхательной цепи), моноаминоксидазы (обезвреживание биогенных аминов), церулоплазмина, каталазы (обезвреживание Н2О2), тирозиназы (синтез меланина), супероксиддисмутазы (обезвреживание О2–), лизилоксидазы (синтез коллагена и эластина).
Суточная потребность — 2–3 мг. При недостатке меди в рационе может развиваться железодефицитная анемия, так как медь непосредственно участвует в метаболизме железа.
Селен
Селен является дефицитным и абсолютно незаменимым микроэлементом. Он является мощным антиоксидантом, защищая ткани от свободнорадикальной деструкции как самостоятельно (например, защищая SH-группы от окисления), так и в составеглутатиопероксидазы (Se входит в состав её активного центра) — важнейшего фермента антиоксидантной системы организма. Селен — составная часть тироксин-5-дейодазы, обеспечивающей синтез гормона щитовидной железы — трийодтиронина. Селен — классический антиканцероген, что объясняется его антиоксидантными свойствами.
Суточная потребность — 100 мкг.
БИОХИМИЯ ПИТАНИЯ. ВИТАМИНЫ И ДРУГИЕ НЕЗАМЕНИМЫЕ ФАКТОРЫ ПИТАНИЯ. СИНДРОМ НЕДОСТАТОЧНОГО ПИТАНИЯ
Питательное вещество — компонент пищи, который обеспечивает организм струк- турно-функциональными компонентами или энергией.
Условно различают три важнейших категории питательных веществ:
▪энергодающие (белки, углеводы и липиды);
▪микрокомпоненты (витамины и минеральные соединения, необходимые для биохимических процессов);
▪волокнистые соединения (неперевариваемые полисахариды).
Незаменимый фактор питания — вещество, поступающее в организм с пищей, поскольку в самом организме оно не может образовываться в достаточном количестве.
Известные на сегодняшний день незаменимые факторы питания для человека:
▪вода;
▪энергия или калории из углеводов, жиров или белка;
▪8–10 незаменимых аминокислот;
▪незаменимые жирные кислоты;
▪14 витаминов;
▪16–20 минеральных компонентов-микроэлементов.
Энергетические потребности организма взрослого человека в состоянии покоя составляют 1300–1800 ккал. Они увеличиваются при ожогах, травмах, инфекционных заболеваниях, в послеоперационный период. При голодании они снижаются. Основными источниками энергии являются углеводы — 42 %, жиры — 40 %, белки — 15 % и алкоголь — 3 %. Желательно, чтобы 55 % АТФ образовывалось в результате расщепления углеводов, 30 % — липидов, 15 % — белков.
Энергия, выделяющаяся в ходе расщепления в организме продуктов питания— источников энергии, запасается в виде АТФ. В состоянии покоя 22 % образовавшегося АТФ расходуется на работу Na+, K+ АТФ-азы, 21 % — на биосинтез белка, 10 % — на перенос ионов кальция через биологические мембраны и 11 % — на мышечное сокращение.
102

Витамины
Витамин |
Функции |
Гиповитаминоз |
||
|
|
|||
А |
|
Ретинол |
Зрительные пигменты в сетчатке; регуляция |
«Куриная слепота», ксероф- |
|
|
β-каротин |
экспрессии генов и клеточной дифференцировки |
талмия; кератинизация кожи, |
|
|
|
ксеростомия, гипоплазия эмали |
|
|
|
|
|
|
Д |
|
Кальциферол |
Поддержание баланса Са2+; стимуляция |
Рахит = плохая минерализация |
|
|
|
всасывания Са2+ в кишечнике и реабсорбции в |
костной ткани; остеомаляция = |
|
|
|
почках; регуляция экспрессии генов и клеточной |
деминерализация кости, |
|
|
|
дифференцировки |
гипоплазия эмали и |
|
|
|
|
патологическая стираемость |
|
|
|
|
зубов |
|
|
|
|
|
Е |
|
Токоферолы |
Антиоксидант, особенно в клеточных мембранах; |
Чрезвычайно редко — выра- |
|
|
токотриенолы |
роль в передаче клеточного сигнала |
женные неврологические рас- |
|
|
|
стройства |
|
|
|
|
|
|
К |
|
Филлохинон |
Кофермент в образовании g-карбоксиглутамата в |
Нарушение свертывания крови, |
|
|
менахиноны |
составе ферментов свертывания крови и матрикса |
геморрагический синдром, |
|
|
кости |
нарушение минерализации |
|
|
|
|
|
тканей зуба и кости |
|
|
|
|
|
В1 |
|
Тиамин |
Кофермент пируват и a-кетоглутарат дегидроге- |
Поражение периферической |
|
|
|
наз, транскетолазы; участвует в проведении нерв- |
нервной системы (бери-бери) |
|
|
|
ного импульса, регулируя Сl–-каналы |
или ц. н. с. (синдром Вернике- |
|
|
|
|
Корсакова) |
|
|
|
|
|
В2 |
|
Рибофлавин |
Кофермент в окислительно-восстановительных |
Повреждение уголков рта, губ |
|
|
|
реакциях; простетическая группа флавопротеинов |
и языка, себорейный дерматит |
|
|
|
|
|
РР |
|
Ниацин, |
Кофермент в окислительно-восстановительных |
Пеллагра — синдром 3-х «Д» |
|
|
никотиновая |
реакциях, составной компонент НАД+ и НАДФ+; |
|
|
|
кислота, |
роль в регуляции внутриклеточного Са2+ и прове- |
|
|
|
никотинамид |
дении сигнала в клетку |
|
|
|
|
|
|
В6 |
|
Пиридоксин |
Кофермент в реакциях трансаминирования и |
Нарушение метаболизма |
|
|
пиридоксаль |
декарбоксилирования аминокислот, гликоген |
аминокислот, судороги |
|
|
фосфорилазы; модуляция действия стероидных |
|
|
|
|
пиридоксамин |
гормонов |
|
|
|
|
|
|
|
|
|
|
|
Фолиевая кислота |
Кофермент в транспорте одноуглеродных |
Мегалобластическая анемия |
||
|
|
|
фрагментов |
|
|
|
|
|
|
В12 |
|
Кобаламин |
Кофермент в транспорте одноуглеродных |
Пернициозная анемия = |
|
|
|
фрагментов и метаболизме фолиевой кислоты |
мегалобластическая анемия и |
|
|
|
|
дегенерация спинного мозга |
|
|
|
|
|
|
Пантотеновая |
Функциональная часть КоА и ацилпереносящего |
Поражение периферической |
|
|
белка в составе ацилсинтетазы |
нервной системы («синдром |
||
|
|
кислота |
||
|
|
|
жжения стоп») |
|
|
|
|
|
|
|
|
|
|
|
Н |
|
Биотин |
Кофермент в реакциях карбоксилирования |
Нарушение липидного и |
|
|
|
(глюконеогенез, синтез жирных кислот); роль в |
углеводного обменов, дерматит |
|
|
|
регуляции клеточного цикла |
|
|
|
|
|
|
С |
|
Аскорбиновая |
Кофермент в гидроксилировании пролина и |
Цинга (плохое заживление, |
|
|
кислота |
лизина (синтез коллагена); антиоксидант; |
потеря цемента зубов, |
|
|
|
усиливает всасывание железа |
подкожные кровоизлияния) |
|
|
|
|
|
103
