
- •Билет 1
- •Билет 2
- •Билет 3
- •Досліди Перрена по визначенню числа Авогадро за допомогою розподілу Больцмана. Частинки у полі тяжіння розподіляються за законом
- •Билет 4
- •Билет 4
- •Билет 5
- •Билет 5
- •Билет 6
- •Билет 7
- •Билет 7
- •Билет 8
- •Билет 9
- •Билет 13
- •Билет 14
- •2. Тиск під викривленою поверхнею (формула Лапласа)
- •Билет 15
- •Билет 16
- •Билет 17
- •Билет 18
- •1. Третій закон термодинаміки
- •Изменение температуры
Билет 1
1. Ідеальний газ - це ідеалізована модель реальних газів, згідно якої : відсутня взаємодія між молекулами; молекули – матеріальні точки певної маси (займають безмежно малий об’єм в порівнянні з об’ємом посудини); при зіткненні між собою та зі стінками посудини ведуть себе як пружні кульки; молекули рівномірно розподілені по об’єму.
Ідеальний газ при будь-яких умовах завжди перебуває у стані газу.
З
першого припущення виходить, що відстані
між молекулами набагато перевищують
розміри молекул, і тому молекули можна
розглядати як матеріальні точки. З
іншого боку, при великих відстанях між
молекулами можна зневажити силами
притягання й відштовхування між
молекулами. Ця обставина виправдує
друге припущення. Нагадаємо, що пружним
називається удар, при якому механічна
енергія тіл, що набувають зіткнення,
залишається постійною. Виявляється, що
дуже багато реальних газів при нор-
мальних умовах (кімнатній температурі
й атмосферному тиску) можна вважати
ідеальними. Реальні
розріджені гази за своїми властивостями
є дуже близькими до ідеального газу.
,
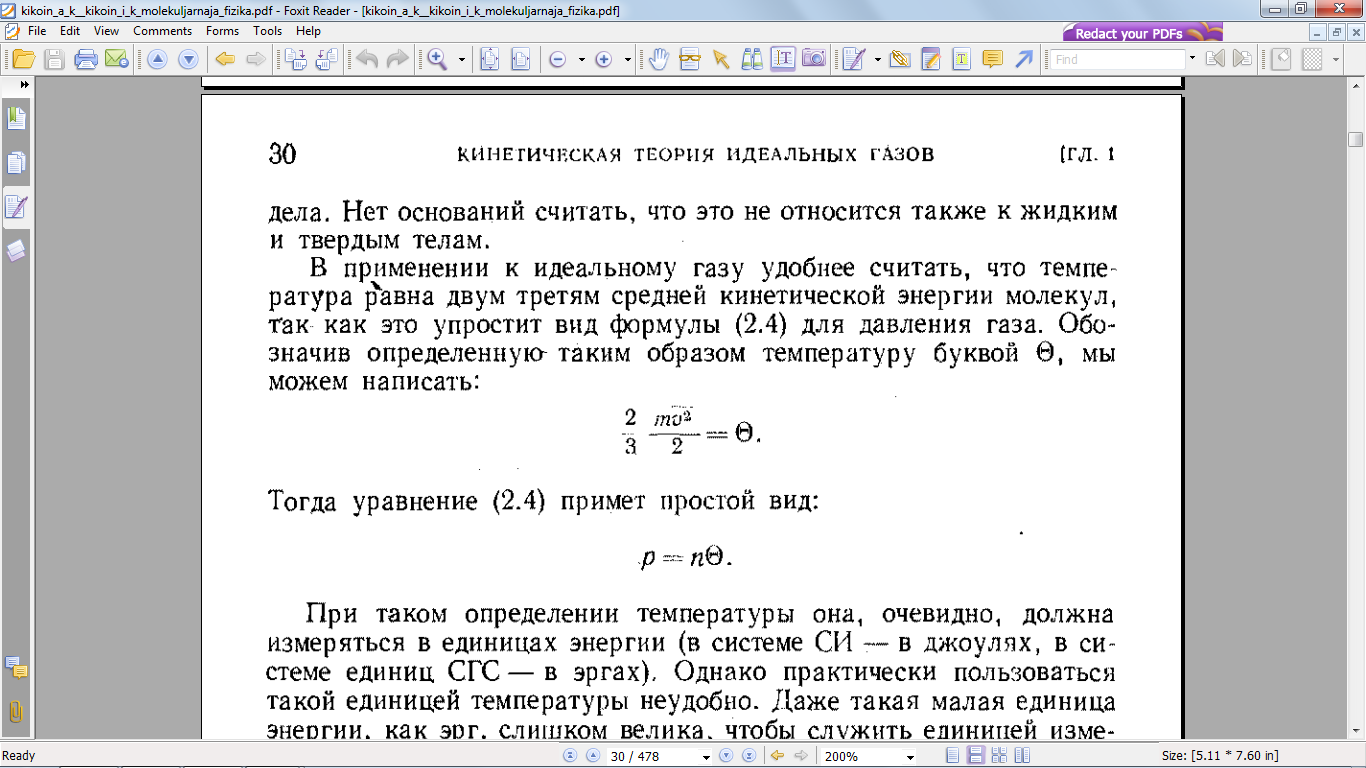
Билет 1 2. Термодинамі́чні потенціа́ли — це набір функцій стану термодинамічної системи, який характеризує її поведінку при термодинамічних процесах. У випадку внутрішньої енергії і вільної енергії, їхня зміна у самочинних процесах дорівнює виконаній системою роботі.
До термодинамічних потенціалів належить внутрішня енергія, ентальпія, вільна енергія (потенціал Гельмгольца), вільна ентальпія (потенціал Ґіббса) та інші.
З чотирьох основних фізичних величин, які характеризують термодинамічну систему: тиску, об'єму, температури й ентропії, термодинамічні потенціали залежать тільки від двох. Дві інші визначаються, як похідні від термодинамічних потенціалів. Наприклад, знаючи вільну енергію, яка є функцією об'єму й температури, можна знайти тиск, встановивши, таким чином, рівняння стану.



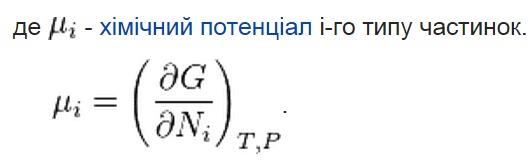
Билет 2

Закон
Бойля—Маріотта:
для даної маси газу при постійнійтемпературі
добуток тиску газу на його об'єм є
величина постійна:
pV = const.

Процес, що відбувається при постійній температурі, називаютьізотермічним. Графік залежності між параметрами стану газу припостійній температурі називають ізотермою. Ізотерми в координатах р, V є гіперболами, розташованими на графіку тим вище, чим вища температура,при якій проходить процес (рис. 1.1).
Закон Гей-Люссака: об'єм даної маси газу при постійному тискузмінюється лінійно з температурою: V = V0 (1 + αt). (1.2) Процес, що відбувається при постійному тиску, називають ізобарним.Графік залежності між параметрами стану газу при постійному тискуназивають ізобарою, яка в координатах V, t зображується прямою.
 2.
2.

Рівнова́га термодинамі́чної систе́ми — стан, при якому термодинамічні параметри усіх тіл, що входять у термодинамічну систему тривалий час не змінюються. Такий стан є тоді, коли тиск,температура і хімічний склад системи в усіх її частинах є однаковими. Якщо в термодинамічній системі, що не має теплоізоляційних й абсолютно жорстких перегородок, тіла або їх частини перебувають не в однаковому стані, то за відсутності нових зовнішніх впливів через певний час у системі настане термодинамічна рівновага. При термодинамічній рівновазі передавання теплоти від одних тіл системи до інших та механічне відносне переміщення окремих частин і частинок системи відсутні, тобто має місце теплова, механічна й дифузійна рівновага.
