
Тема 15 16
.docxТема: Окислительно-восстановительные процессы.
План:
1. Окисленность элементов.
2. Окислительно-восстановительные реакции.
3. Электрохимия.
3.1 Гальванические элементы.
3.2 Электродные потенциалы.
3.3Электролиз.
4.Применение электролиза.
1.
Когда элемент находится в свободном состоянии — образует простое вещество, тогда движение электронов около всех атомов этого вещества происходит одинаково. Это справедливо для всех простых веществ, независимо от их структуры. Например, в молекуле водорода электроны в равной мере движутся около обоих атомов: молекула Н2 неполярна. В случае кристаллов с ковалентной связью химические связи между атомами также симметричны относительно связуемых атомов. В случае металлов распределение как связанных, так и свободных электронов в среднем также является равномерным.
Иначе обстоит дело в сложных веществах. Химические связи между атомами различных элементов несимметричны; в молекулах сложных веществ осуществляются, как правило, полярные ковалентные связи. В ионных соединениях эта неравномерность распределения электронов максимальна — при образовании веществ с ионной связью валентные электроны практически полностью переходят от атома одного элемента к атому другого.
Неравномерность распределения электронов между атомами в соединениях получила название окисленности. Прн этом элемент, электроны которого смещаются к атомам другого элемента (полностью в случае ионной связи или частично в случае полярной), проявляет положительную окисленность. Элемент, к атомам которого смещаются электроны атома другого элемента, проявляет отрицательную окисленность.
Число электронов, смещенных от одного атома данного элемента (при положительной окисленности) или к одному атому данного элемента (при отрицательной окисленности), назыпается степенью окисленности элемента*.
В простых веществах степень окисленности элемента всегда равна нулю. В соединениях некоторые элементы проявляют всегда одну и ту же степень окисленности, но для большинства элементов она в различных соединениях различна.
Постоянную степень окисленности имеют щелочные металлы (+1),щелочноземельные металлы (+2), фтор ( —1)
Для установления степени окисленности элементов в соединениях можно пользоваться таблицей электроотрицательностей элементов
При этом следует иметь в виду, что при образовании химической связи электроны смещаются к атому более электроотрицательного элемента. Так, относительная электроотрицательность фосфора равна 2,2, а иода 2,6. Поэтому в соединении Р1з общие электроны смещены к атомам иода и степени окисленности фосфора и иода равны соответственно -f-З и —1. Однако в нитриде иода NI3 степени окисленности азота и иода равны —3 и +1, поскольку электроотрицательность азота (3,07) выше элек-троотрнцательности иода.
2.
Все химические реакции можно разбить на две группы. В реакциях первой группы окисленность всех элементов, входящих в состав реагирующих веществ, остается неизменной, а в реакциях второй группы окисленность одного или нескольких элементов изменяется.
В качестве примера реакций первой группы можно привести реакцию нейтрализации:
НС1 + NaOH = NaCl + Н20
Примером реакции второй группы может служить взаимодействие металла с кислотой:
Zn + 2НС1 = ZnCl2 + Н2|
Если при реакции нейтрализации ни один элемент не изменяет степень своей окисленности, то во втором примере степень окисленности цинка изменяется от 0 до +2, а водорода—от +1 до 0.
Реакции, в результате которых изменяются степени окисленности элементов, называются окислительно-восстановительными.
Такой процесс — отдача электронов, сопровождающаяся повышением степени окисленности элемента,— называется окислением.
Присоединение электронов, сопровождающееся понижением степени окисленности элемента, называется восстановлением.
Вещество, в состав которого входит окисляющийся элемент, называется восстановителем, а вещество, содержащее восстанавливающийся элемент, окислителем.
Общее число электронов в системе при химических реакциях не изменяется: число электронов, отдаваемых молекулами (атомами, ионами) восстановителя, равно числу электронов, присоединяемых молекулами (атомами, ионами) окислителя. Поэтому одна молекула хлора может окислить два атома натрия.
Составление уравнений окислительно-восстановительных реакций . Применяются два метода составления уравнений окислительно-восстановительных реакций — метод электронного баланса и метод полуреакций.
Метод электронного балланса
В этом методе сравнивают степени окисления атомов в исходных и конечных веществах, руководствуясь правилом: число электронов, отданных восстановителем, должно равняться числу электронов, присоединенных окислителем. Для составления уравнения надо знать формулы реагирующих веществ и продуктов реакции. Последние определяются либо опытным путем, либо на основе известных свойств элементов. Рассмотрим применение этого метода на примерах.
Пример 1. Составление уравнения реакции меди с раствором нитрата палладия (II). Запишем формулы исходных и конечных веществ реакции и покажем изменения степеней окисления:
![]()
Медь, образуя ион меди, отдает два электрона, ее степень окисления повышается от 0 до +2. Медь - восстановитель. Ион палладия, присоединяя два электрона, изменяет степень окисления от +2 до 0. Нитрат палладия (II) -окислитель. Эти изменения можно выразить электронными уравнениями
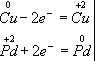
из которых следует, что при восстановителе и окислителе коэффициенты равны 1. Окончательное уравнение реакции:
Cu + Pd(NO3)2 = Cu(NO3)2 + Pd
Как видно, в суммарном уравнении реакции электроны не фигурируют.
Чтобы проверить правильность составленного уравнения, подсчитываем число атомов каждого элемента в его правой и левой частях. Например, в правой части 6 атомов кислорода, в левой также 6 атомов; палладия 1 и 1; меди тоже 1 и 1. Значит, уравнение составлено правильно.
Переписываем это уравнение в ионной форме:
Cu + Pd2+ + 2NO3- = Cu2+ + 2NO3- + Рd
И после сокращения одинаковых ионов получим
Cu + Pd2+ = Cu2+ + Pd
Пример 2. Составление уравнения реакции взаимодействия оксида марганца (IV) с концентрированной соляной кислотой (с помощью этой реакции в лабораторных условиях получают хлор).
Запишем формулы исходных и конечных веществ реакции:
НCl + МnО2 → Сl2 + MnСl2 + Н2О
Покажем изменение степеней окисления атомов до и после реакции:
![]()
Эта реакция окислительно-восстановительная, так как изменяются степени окисления атомов хлора и марганца. НCl - восстановитель, MnО2 — окислитель. Составляем электронные уравнения:

и находим коэффициенты при восстановителе и окислителе. Они соответственно равны 2 и 1. Коэффициент 2 (а не 1) ставится потому, что 2 атома хлора со степенью окисления -1 отдают 2 электрона. Этот коэффициент уже стоит в электронном уравнении:
2НСl + MnO2 → Сl2 + MnСl2 + Н2О
Находим коэффициенты для других реагирующих веществ. Из электронных уравнений видно, что на 2 моль HCl приходится 1 моль MnО2. Однако, учитывая, что для связывания образующегося двухзарядного иона марганца нужно еще 2 моль кислоты, перед восстановителем следует поставить коэффициент 4. Тогда воды получится 2 моль. Окончательное уравнение имеет вид
4НCl + МnО2 = Сl2 + MnСl2 + 2Н2О
Проверку правильности написания уравнения можно ограничить подсчетом числа атомов одного какого-либо элемента, например хлора: в левой части 4 и в правой 2 + 2 = 4.
Поскольку в методе электронного баланса изображаются уравнения реакций в молекулярной форме, то после составления и проверки их следует написать в ионной форме.
Перепишем составленное уравнение в ионной форме:
4Н+ + 4Сl- + МnО2 = Сl2 + Мn2+ + 2Сl- + 2Н2О
и после сокращения одинаковых ионов в обеих частях уравнения получим
4Н+ + 2Cl- + MnO2 = Сl2 + Mn2+ + 2Н2О
Пример 3. Составление уравнения реакции взаимодействия сероводорода с подкисленным раствором перманганата калия.
Напишем схему реакции - формулы исходных и полученных веществ:
Н2S + КМnO4 + Н2SО4 → S + МnSО4 + К2SO4 + Н2О
Затем покажем изменение степеней окисления атомов до и после реакции:
![]()
Изменяются степени окисления у атомов серы и марганца (Н2S - восстановитель, КМnО4 - окислитель). Составляем электронные уравнения, т.е. изображаем процессы отдачи и присоединения электронов:

И наконец, находим коэффициенты при окислителе и восстановителе, а затем при других реагирующих веществах. Из электронных уравнений видно, что надо взять 5 моль Н2S и 2 моль КМnО4, тогда получим 5 моль атомов S и 2 моль МnSО4. Кроме того, из сопоставления атомов в левой и правой частях уравнения, найдем, что образуется также 1 моль К2SО4 и 8 моль воды. Окончательное уравнение реакции будет иметь вид
5Н2S + 2КМnО4 + ЗН2SО4 = 5S + 2МnSО4 + К2SО4 + 8Н2О
Правильность написания уравнения подтверждается подсчетом атомов одного элемента, например кислорода; в левой части их 2.4 + 3.4 = 20 и в правой части 2.4 + 4 + 8 = 20.
Переписываем уравнение в ионной форме:
5Н2S + 2MnO4- + 6H+ = 5S + 2Мn2+ + 8Н2О
Известно, что правильно написанное уравнение реакции является выражением закона сохранения массы веществ. Поэтому число одних и тех же атомов в исходных веществах и продуктах реакции должно быть одинаковым. Должны сохраняться и заряды. Сумма зарядов исходных веществ всегда должна быть равна сумме зарядов продуктов реакции.
Метод полуреакций
 Как показывает само
название,
этот метод основан на составлении ионных уравнений для процесса
окисления и
процесса восстановления с последующим
суммированием их в общее уравнение. В
качестве примера составим уравнение той же реакции,
которую использовали
при объяснении метода
электронного баланса. При пропускании сероводорода Н2S через подкисленный раствор
перманганата калия КМnО4 малиновая окраска исчезает и раствор мутнеет.
Опыт показывает,
что помутнение раствора происходит в результате образования элементной серы,
т.е. протекания процесса:
Как показывает само
название,
этот метод основан на составлении ионных уравнений для процесса
окисления и
процесса восстановления с последующим
суммированием их в общее уравнение. В
качестве примера составим уравнение той же реакции,
которую использовали
при объяснении метода
электронного баланса. При пропускании сероводорода Н2S через подкисленный раствор
перманганата калия КМnО4 малиновая окраска исчезает и раствор мутнеет.
Опыт показывает,
что помутнение раствора происходит в результате образования элементной серы,
т.е. протекания процесса:
Н2S → S + 2H+
Эта схема уравнена по числу атомов. Для уравнивания по числу зарядов надо от левой части схемы отнять два электрона, после чего можно стрелку заменить на знак равенства:
Н2S - 2е- = S + 2H+
Это первая полуреакция - процесс окисления восстановителя Н2S.
Обесцвечивание раствора связано с переходом иона MnO4- (он имеет малиновую окраску) в ион Mn2+ (практически бесцветный и лишь при большой концентрации имеет слабо-розовую окраску), что можно выразить схемой
MnO4- → Mn2+
В кислом растворе кислород, входящий в состав ионов МnО4, вместе с ионами водорода в конечном итоге образует воду. Поэтому процесс перехода записываем так:
MnO4- + 8Н+→ Мn2+ + 4Н2О
Чтобы стрелку заменить на знак равенства, надо уравнять и заряды. Поскольку исходные вещества имеют семь положительных зарядов (7+), а конечные - два положительных (2+), то для выполнения условия сохранения зарядов надо к левой части схемы прибавить пять электронов:
MnO4- + 8Н+ + 5e-= Mn2+ + 4Н2О
Это вторая полуреакция - процесс восстановления окислителя, т.е. перманганат-иона
Для составления общего уравнения реакции надо уравнения полуреакций почленно сложить, предварительно уравняв числа отданных и полученных электронов. В этом случае по правилам нахождения наименьшего кратного определяют соответствующие множители, на которые умножаются уравнения полуреакций. Сокращенно запись проводится так:

И, сократив на 10Н+, окончательно получим
5Н2S + 2MnO4- + 6H+ = 5S + 2Mn2+ + 8Н2О
Проверяем правильность составленного в ионной форме уравнения: число атомов кислорода в левой части 8, в правой 8; число зарядов: в левой части (2-)+(6+) = 4+, в правой 2(2+) = 4+. Уравнение составлено правильно, так как атомы и заряды уравнены.
Методом полуреакций составляется уравнение реакции в ионной форме. Чтобы от него перейти к уравнению в молекулярной форме, поступаем так: в левой части ионного уравнения к каждому аниону подбираем соответствующий катион, а к каждому катиону - анион. Затем те же ионы в таком же числе записываем в правую часть уравнения, после чего ионы объединяем в молекулы:

Таким образом, составление уравнений окислительно-восстановительных реакций с помощью метода полуреакций приводит к тому результату, что и метод электронного баланса.
Сопоставим оба метода.
Достоинство
ыметода полуреакций по сравнению с методом электронного баланса в том.
что в нем применяются
не гипотетические ионы,
а реально существующие. В самом деле,
в растворе нет ионов
![]() а есть ионы
а есть ионы
![]()
При методе полуреакций не нужно знать степень окисления атомов. Написание отдельных ионных уравнений полуреакций необходимо для понимания химических процессов в гальваническом элементе и при электролизе. При этом методе видна роль среды как активного участника всего процесса. Наконец, при использовании метода полуреакций не нужно знать все получающиеся вещества, они появляются в уравнении реакции при выводе его.Поэтому методу полуреакций следует отдать предпочтение и применять его при составлении уравнений всех окислительно-восстановительных реакций, протекающих в водных растворах.
3.
ЭЛЕКТРОХИМИЯ , раздел физ. химии, который изучает системы, содержащие ионы (р-ры, расплавы и твердые электролиты), а также процессы и явления с участием заряженных частиц (ионов и электронов), имеющие место на границе раздела двух фаз. Обычно одной из фаз является металл или полупроводник, другая фаза - р-р или расплав электролита либо твердый электролит. Для таких двухфазных систем термин "Э." имеет более узкий смысл как наука, изучающая взаимод. зарядов металла или полупроводника с ионами и молекулами р-ра (расплава, твердого электролита). Часто это взаимод. сопровождается возникновением в цепи электрич. тока, тогда Э. можно определить как науку, изучающую физ.-хим. процессы, которые сопровождаются появлением электрич. тока или, наоборот, возникают под действием электрич. тока на хим. соединения. Последнее определение широко распространено, хотя и является наиб. узким.
3.1
Проводники первого рода (твердые) и второго рода (жидкие электролиты) совместно используются в гальванических элементах, служащих источниками постоянного тока.
В гальванических элементах во время их работы происходит движение ионов и оседание на электродах элемента, выделяющегося из электролита вещества.
Простейшим гальваническим элементом является медно-цинковый. В стеклянный сосуд,, наполненный раствором серной кислоты H2SO4 в воде Н20, погружены медная Cu и цинковая Zn пластины, которые представляют собой положительный и отрицательный полюсы элемента.
При замыкании цепи элемента каким-либо проводником внутри этого элемента будет протекать ток от цинковой отрицательной пластины к медной положительной, а во внешней цепи — от медной к цинковой. Под действием тока внутри элемента положительные ионы водорода Н2 движутся по направлению тока, отрицательные ионы кислотного остатка SO4 — в противоположном направлении. Приходя в соприкосновение с медной пластиной, положительные ионы водорода отдают ей свои заряды, а водород в виде пузырьков газа скопляется на ее поверхности. В это же время отрицательные ионы остатка серной кислоты отдают свои заряды цинковой пластине. Таким образом происходит непрерывный заряд пластин элемента, поддерживающий разность потенциалов (напряжение) на его зажимах.
Выделение водорода на медной пластине элемента ослабляет его действие, поляризует элемент. Явление поляризации состоит в том, что скопляющийся на положительном электроде водород создает в совокупности с металлом электрода дополнительную разность потенциалов, называемую электродвижущей силой поляризации. Эта э. д. с. направлена противоположно электродвижущей силе элемента. Кроме того, пузырьки водорода, покрывающие часть медной пластины, уменьшают ее действующую поверхность, а это увеличивает внутреннее сопротивление элемента.
Поляризация в рассмотренном элементе настолько значительна, что делает его непригодным для практических целей. Устранение явления поляризации в современных элементах осуществляется посредством поглотителей, вводимых в состав элемента и носящих название деполяризаторов, которые предназначены для поглощения водорода и не допускают скопления его на положительном полюсе элемента. Такими деполяризаторами могут служить химические препараты, богатые кислородом или хлором.
Э. д. с. гальванического элемента зависит от химических и физических свойств веществ, его составляющих и, как показывает опыт, не зависит ни от формы и размеров элемента, ни от его внутреннего устройства. Но внутреннее устройство и размеры отдельных частей элемента имеют большое влияние на величину его внутреннего сопротивления, так как они зависят от расстояния между полюсами (при уменьшении этого расстояния внутреннее сопротивление элемента уменьшается), от размера погруженной в жидкость поверхности полюсов (при увеличении этой поверхности внутреннее сопротивление уменьшается), от химического состава жидкости элемента. Необходимо отметить, что внутреннее сопротивление гальванических элементов не является величиной постоянной (по мере работы элемента оно постепенно возрастает).
В зависимости от способа деполяризации гальванические элементы могут быть подразделены на два типа: элементы, в которых в качестве деполяризатора применяют раствор какой-либо соли, например медно-цинковые, и элементы, в которых анод окружен перекисью марганца, например, угольно-цинковые. Гальванические элементы указанных двух типов широко применяют в электротехнике.

Э. д. с. медно-цинкового элемента равна 1,1 в, а внутреннее сопротивление в зависимости от времени работы — 5 - 10 ом.
В угольно-цинковом элементе положительным полюсом служит угольная пластина, а отрицательным — цинковый стержень. Деполяризатором в этом элементе является спрессованная под большим давлением смесь, называемая агломератом. Она состоит из перекиси марганца и графита. В качестве электролита в угольно-цинковом элементе применяют водный раствор хлористого аммония NН4Cl. Электродвижущая сила угольно-цинкового элемента 1,4—1,5 в в начале разряда при среднем значении 0,9 - 1,1 в, а внутреннее сопротивление в зависимости от конструкции элемента— 0,25 -0,7 ом в начале разряда и 1,4—5 ом в конце.
Угольно-цинковые элементы выпускает отечественная промышленность в виде так называемых сухих элементов стаканчикового и галетного типов, весьма удобных для переноски и перевозки.
В сухих элементах стаканчикового типа (рис. 24) положительный полюс 8 с агломератом 2 помещают внутри цинковой коробки 9, которая служит отрицательным полюсом элемента. Пространство между стенками цинковой коробки и агломератом заполняют, пастой 1, состоящей из раствора хлористого аммония и картофельной муки. Над агломератом укладывают картонную прокладку 3,1 на которую насыпают прослойку 4 из опилок; сверху опилки закрывают картонной прокладкой 5. Затем элемент заливают смолой 7, в которую вставляют трубку 6. Назначение этой трубки — удалять образующиеся внутри элемента газы.
На выходящий из смолы угольный электрод насаживают медный колпачок с винтом и гайкой для присоединения проводника. К верхней части цинковой коробки (отрицательному полюсу) припаивают изолированный гибкий проводник. На дно коробки укладывают изолирующую прокладку 10.
В галетном элементе отрицательным электродом является цинковая пластина, положительным — спрессованный в виде галеты порошок двуокиси марганца с углем. Между электродами помещают картонную пластинку, пропитанную раствором нашатырного спирта. Наружная поверхность цинковой пластины покрыта слоем канифоли с частицами графита для электропроводности.
В качестве изоляции используются хлорвиниловые пленки. Галетные элементы компактны и их активные материалы (особенно цинк) используются лучше, чем в стаканчиковых элементах.
В окисно-ртутных элементах отрицательным электродом является цинк, а положительным — окись ртути. Их преимущество по сравнению с угольно-цинковыми элементами состоит в хорошей сохранности при повышенной температуре, меньшем изменении напряжения при разряде и большой удельной энергии на единицу объема, что особенно ценно для использования в переносной аппаратуре в условиях теплого климата.
В настоящее время широко применяют элементы ВДЛ, электродами которых служит цинк и активированный пористый уголь, адсорбирующий кислород из воздуха, а электролитом — раствор едкого калия. Достоинство этих элементов - малое изменение напряжения при разряде. Вследствие герметичности элементов ВДЛ не происходит заметного ухудшения свойств едкого калия, поэтому они могут храниться неограниченное время. После полного разряда элемента угольный электрод сохраняет работоспособность и элемент может быть восстановлен путем замены цинка и электролита. Такое восстановление элемента можно производить дважды. Э. д. с. элемента ВДЛ 1,4 в, напряжение при нормальном режиме разряда 1,2—1,25 в, напряжение в конце разряда 0,9 в.
Ввиду дефицитности и высокой стоимости цинка желательно использовать в качестве отрицательного электрода какой-либо другой металл, например железо.
В последние годы разработаны железо-угольные щелочные элементы ВДЖ, применяемые для питания радиоустройств в трудно доступных для обслуживания местностях. Однако замена цинка железом привела к уменьшению э. д. с. элемента. Начальное напряжение элемента ВДЖ 0,75 в, напряжение в конце разряда 0,45 в. Элементы ВДЖ выдерживают длительное хранение и нормально работают при температуре 0° С,
Для составления батарей гальванические элементы соединяют между собой последовательно, параллельно и смешанно. При последовательном соединении положительный полюс первого элемента соединяется с отрицательным полюсом второго элемента, положительный полюс второго — с отрицательным третьего и т. д.
Если батарея состоит из n последовательно соединенных элементов с э. д. с. каждого элемента Е0 и с внутренним сопротивлением r0 ом, то э. д. с. батареи Е=nЕ0, а внутреннее сопротивление ее r = nr0
При параллельном соединении элементов положительные полюсы всех элементов соединяют между собой и отрицательные полюсы также соединяют между собой. В результате получают два общих полюса батареи: положительный и отрицательный. Если батарея состоит из m параллельно соединенных элементов с э. д. с. Каждого элемента E0 в и с внутренним сопротивлением r0 ом, то
э.
д. с. батареи Е = Е0,
а внутреннее сопротивление ее
![]()
Для составления батареи из смешанно соединенных элементов разделяют все элементы на группы с одинаковым числом их в каждой группе. Элементы в каждой группе соединяют параллельно или последовательно, а группы между собой в первом случае — последовательно, а во втором — параллельно.
Если
n
— число групп или элементов в группе,
соединенных поcледовательно,
m
— число групп или элементов в группе,
соединении параллельно, Е0
— э. д. с. каждого элемента, а r0
—внутреннее сопротивление, то э. д. с.
батареи Е = nЕ0,
а ее внутреннее сопротивление
![]() .
.
3.2
Если же процессы окисления и восстановления пространственно разделить, то любую окислительно-восстановительную реакцию можно использовать для получения электрической энергии. Такие устройства называют химическими источниками тока (ХИТ). Простейший ХИТ – гальваническая ячейка (рис. 7.1) – представляет собой сосуды, в которых два электрода, помещенные в раствор соответствующих электролитов, соединены солевым мостиком (проводником второго рода *), представляющим собой стеклянную трубку, заполненную раствором такого электролита, катионы и анионы которого характеризуются одинаковой подвижностью. При замыкании внешней цепи проводником первого рода начинается окислительно-восстановительная реакция, о чем свидетельствует возникновение электродвижущей силы (ЭДС).
