
- •М о д у л ь 1. Основні поняття і закони хімії т е м а 1 (вступна). Основні поняття і закони хімії.
- •1.4. Список рекомендованої літератури
- •2.1. Рекомендації до вивчення теоретичного матеріалу
- •2.4. Лабораторна робота
- •2.5. Список рекомендованої літератури
- •3.1.Рекомендації до вивчення теоретичного матеріалу
- •3.2. Приклади розвязування типових задач
- •3.3. Задачі для самостійного рішення: 182, 183, 190, 208
- •3.4. Лабораторна робота
- •3.5. Список рекомендованої літератури
- •4.1. Рекомендації до вивчення теоретичного матеріалу
- •4.2. Приклади розвязування типових задач.
- •4.3. Задачі для самостійного рішення: 720, 724, 736
- •4.4. Лабораторна робота
- •Дослід 3. Утворення сольватокомплексів
- •Дослід 6. Стійкість комплексів
- •4.5. Список рекомендованої літератури
- •М о д у л ь 2. Основні закономірності протікання хімічних реакцій т е м а 5. Енергетика хімічних процесів
- •5.1. Рекомендації до вивчення теоретичного матеріалу
- •5.2. Приклади розвязування типових задач
- •Розв’язок: Температуру початку реакції розрахуємо за формулою:
- •5.3. Задачі для самостійного рішення: № 283, 285, 303, 311
- •5.4. Лабораторна робота
- •5.5. Список рекомендованої літератури
- •Тема 6. Швидкість протікання хімічних реакцій та хімічна рівновага
- •6.2.Приклади розвязування типових задач
- •6.3. Задачі для самостійного рішення: 330, 332, 334, 352
- •6.4. Лабораторна робота
- •Загальні вказівки
- •М о д у л ь 3. Розчини т е м а 7. Розчинність. Способи вираження концентрації
- •8.1. Рекомендації до вивчення теоретичного матеріалу
- •8.3. Задачі для самостійного розвязування: 1030, 1031, 1035, 1037
- •8.4. Лабораторна робота
- •8.5. Список рекомендованої літератури
- •Т е м а 9. Властивості розчинів. Рівноваги у розчинах електролітів
- •9.1. Рекомендації до вивчення теоретичного матеріалу
- •9.2. Приклади розвязування типових задач
- •9.3. Задачі для самостійного рішення: № 516, 544, 586
- •9.4. Лабораторна робота
- •9.5. Список рекомендованої літератури
- •Тема 10. Окисно-відновні реакції
- •10.1. Рекомендації до вивчення теоретичного матеріалу
- •10.2. Приклади рішення типових задач
- •10.3. Задачі для самостійного рішення: 624, 625, 626, 640
- •10.4. Лабораторна робота
- •10.5. Список рекомендованої літератури
- •М о д у л ь 4. Електрохімічні процеси
- •Т е м а 11. Гальванічні елементи
- •11.1. Рекомендації до вивчення теоретичного матеріалу
- •11.2. Приклади розвязування типових задач
- •1.3. Задачі для самостійного рішення: 658, 660, 661
- •11.4. Лабораторна робота
- •11.5. Список рекомендованої дітератури
- •12.1. Рекомендації до вивчення теоретичного матеріалу
- •12.2. Приклади розв’язку типових задач
- •12.4. Лабораторна робота
- •12.5. Список рекомендованої літератури
- •13.1. Рекомендації до вивчення теоретичного матеріалу
- •13.2. Приклади рішення типових задач
- •13.3. Задачі для самостійного рішення 689, 690, 695, 709
- •13.4. Лабораторна робота
- •13.5. Список рекомендованої літератури
- •Тема 14. Властивості неметалів viiа групи (f, Cl, Br, I)
- •14.1. Рекомендації до вивчення теоретичного матеріалу
- •14.2. Приклади розв’язку типових задач
- •14.3. Задачі для самостійного розв’язування: 823, 824, 831.
- •14.4. Лабораторна робота
- •14.5. Список рекомендованої літератури
- •Тема 15. Властивості неметалів viа групи (o, s, Se, Te)
- •15.1 Рекомендації до вивчення теоретичного матеріалу
- •15.2. Приклади розв’язку типових задач
- •15.3. Задачі для самостійного розв’язку
- •15.4. Лабораторна робота
- •15.5. Список рекомендованої літератури
- •Тема 16. Властивості неметалів vа групи (n, p, As, Sb)
- •16.1. Рекомендації до вивчення теоретичного матеріалу
- •16.2. Приклади розв’язування типових задач
- •16.3. Задачі для самостійного розв’язку: 901, 902, 917
- •16.4. Лабораторна робота
- •Дослід 8. Гідроліз фосфатів
- •16.5. Список рекомендованої літератури
- •Тема 17. Властивості неметалів іvа групи (с, Sі)
- •17.1. Рекомендації до вивчення теоретичного матеріалу
- •17.2. Приклади розв’язування типових задач
- •17.3. Задачі для самостійного розв`язку: № 944, 949, 964.
- •17.4. Лабораторна робота
- •17.5. Список рекомендованої літератури
- •М о д у л ь 5. Властивості конструкційних і інструментальних металів і їхніх сполук. Полімерні матеріали
- •18.1. Рекомендації до вивчення теоретичного матеріалу
- •18.2. Приклади розвязування типових задач
- •18.3. Задачі для самостійного рішення: 1009, 1051, 1053
- •18.4. Лабораторна робота
- •Дослід 6. Окисно-відновні властивості сполук титана
- •Дослід 7. Електрохімічне оксидування (анодирування) алюмінію (елементи ндрс)
- •Сполуки водних розчинів для фарбування анодируваного алюмінію
- •18.5. Список рекомендованої літератури
- •Т е м а 19. Властивості заліза, кобальту, нікелю
- •19.1. Рекомендації до вивчення теоретичного матеріалу
- •19.2. Приклади розвязування типових задач
- •19.3. Задачі для самостійного рішення: 1113,1114, 1117, 1118
- •19.4. Лабораторна робота
- •19.5. Список рекомендованої літератури
- •Т е м а 20. Властивості металів підгрупи Cr і Mn і їх сполук
- •20.1. Рекомендації до вивчення теоретичного матеріалу
- •20.2. Приклади розвязування типових задач
- •20.3. Задачі для самостійного рішення: 1084, 1096, 1097
- •20.4. Лабораторна робота
- •20.5. Список рекомендованої літератури
- •21. Властивості металів vb групи (підгрупи ванадію)
- •21.1 Рекомендації до вивчення теоретичного матеріалу
- •21.2. Приклади розв’язування типових задач
- •21.3. Задачи для самостійного розв’язування : №1081, 1082
- •21.4. Лабораторна робота
- •21.5. Список рекомендованої літератури
- •22.1. Рекомендації до вивчення теоретичного матеріалу
- •22.2. Приклади розвязування типових задач
- •22.3. Задачі для самостійного рішення: 1071, 1072, 1077
- •2.4. Лабораторна робота
- •Дослід 3. Окисно-відновні властивості сполук станума і плюмбума
- •Дослід 6. Електролітичне лудіння (з елементами ндрс)
- •22.5. Список рекомендованої літератури
- •Т е м а 23. Властивості конструкційних металів ib і iib груп
- •23.1. Рекомендації до вивчення теоретичного матеріалу
- •23.2. Приклади розвязування типових задач
- •22.3. Задачі для самостійного рішення 995, 984, 1025
- •23.4. Лабораторна робота
- •23.5. Список рекомендованої літератури
- •24.1. Рекомендації до вивчення теоретичного матеріалу
- •24.2. Лабораторна робота
- •24.3. Список рекомендованої літератури
- •Питання до колоквіуму за темами «Будова атома. Періодичний закон. Властивості елементів. Хімічний зв'язок. Комплексні сполуки. Типи взаємодії молекул»
- •Тиск водяної пари при різних температурах
- •Добуток розчинності (др) важкорозчинних сполук (25оС)
- •Індивідуальні завдання до теми «Основні поняття і закони хімії»
- •Індивідуальні завдання до теми : "Електролітична дисоціація, рН, гідроліз солей"
- •Тема 1. (вступна). Основні поняття і закони хімії
- •Тема 2. Закон еквівалентів…………………………………………………………………....7
- •Тема 3. Будова атома. Періодичний закон. Властивості елементів..................................10
- •Тема 4. Хімічний зв'язок. Комплексні сполуки……………………….....................................15
- •Тема 5. Енергетика хімічних процесів………………………………….................................21
- •Тема 6. Швидкість хімічних реакцій і хімічна рівновага……................................................29
- •Тема 7. Розчинність. Способи вираження концентрації……………..................................33
- •Тема 18. Властивості легких конструкційних металів
20.5. Список рекомендованої літератури
Фролов В.В. Химия. – М.: Высш. шк., 1986. – С. 340 - 360.
Глинка Н.Л. Общая химия. – Л.: Химия, 1988. – С. 633 – 645; 2004. – С. 511-521.
Глинка Н.Л. Задачи и упражнения по общей химии. – Л.: Химия, 1985. – С. 238 – 241.
Ахметов Н.С. Общая и неорганическая химия. – М.: Высш. шк., 1981.-С. 548 – 579; 2001. – С. 597-629.
21. Властивості металів vb групи (підгрупи ванадію)
21.1 Рекомендації до вивчення теоретичного матеріалу
З






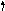

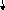
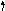 агальна
формула металівVB
групи (N,Nb,Ta) – (n-1)
агальна
формула металівVB
групи (N,Nb,Ta) – (n-1)![]() , але у елемента41Nbспостерігається «провал»
електрона, тобто його електронна формула
, але у елемента41Nbспостерігається «провал»
електрона, тобто його електронна формула
![]() .
.





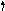
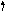
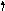
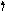

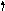 23V , 73Ta
41Nb
23V , 73Ta
41Nb
Максимальний позитивний ступінь окиснення дорівнює 3+2 або 4+1=5;
Найнижчий ступінь окиснення +2. Але відомі чисельні сполуки металів зі ступенями окиснення +3 і +4. Найбільш характерні оксиди:
EO, E2O3– основні оксиди (E = V, Nb, Ta)
EO2– амфотерні оксиди
E2O5– кислотні оксиди ( ангідриди кислот)
Для ванадія відомі численні різнобарвні оксиди нестехіометрічного складу: сірий VO (VO0.9-1.2) , чорний V2O3 (VO1.6-1.8) , синій VO2 (VO1.8-2.17) , червоний V2O5. Стандартні електродні потенціали металів VB групи (Me0 – zē → Mez+) (E,B):
Me = V (-1,19; z = 2); Nb (-1,10; z = 3); Ta (-1,13; z = 5).
За звичайних температур у
компактному вигляді ванадій, ніобій і
тантал інертні: лише ванадій повільно
розчиняється у плавиковій кислоті (HF)
і концентрованій ![]() ,
утворюючи сполуки ванадію (+5):
3V+5HNO3
→ 3HNO3+5NO+H2O.
,
утворюючи сполуки ванадію (+5):
3V+5HNO3
→ 3HNO3+5NO+H2O.
Ніобій і тантал розчиняються у суміші HNO3 і HCl («царська водка»), або, краще у суміші HNO3 і HF:
3Nb + 5HNO3 + 21HF=3H2[NbF7] + 5NO + 10H2O
У стані порошків ванадій, ніобій і тантал реагують при високих температурах з більшістю оксидів (О2,S,Se,галогени) з утворенням сполук Ме (+5).Порошки V,NbiTa адсорбують водень, утворюючи тверді розчини змішаного складу.
За звичайних умов найбільш характерними є ступені окиснення +4 і +5, наприклад, МеHal5, MeO2Hal, MeOHal3 , MeOHal2 (Hal – галоген).У водних розчинах вказані сполуки гідролізуються. Слід уважно розглянути по підручнику властивості сполук ванадію +2, +3, +4 і +5, звернувши особливу увагу на схильність V (+4) і V(+5) до реакції полімеризації з утворенням ізо- і гетерополіванадатів: V2О74- , V6О174- , НV6О173- , V10О286- і інші. Ступінь полімеризації залежить від рН і концентрації іонів ванадію у розчині. У нейтральному і лужному середовищах ванадій (+5) існує у вигляді мономерного ванадат-іона VО3-.
Слід звернути увагу на виробництво металів VВ групи і застосування їх у техніці і промисловості (виробництво сплавів, електронна промисловість, виробництво скла і кераміки, тощо).
21.2. Приклади розв’язування типових задач
Задача1. Яка з двох солей: VCl2 чи VCl5 підлягають більшому гідролізу і чому?
Розв’язок.
Дихлород ванадія VCl2![]() має
іонний тип зв’язку, тому такі солі
гідролізуються переважно по першому
ступеню і утворюють прозорі розчини:
має
іонний тип зв’язку, тому такі солі
гідролізуються переважно по першому
ступеню і утворюють прозорі розчини:
VCl2 + HOH ↔ V(OH)Cl + HCl
Пентахлорид VCl5 - молекула з ковалентним типом зв’язку. Будучи кислотними сполуками, солі такого типу підлягають значно більшому гідролізу. Отже, VCl5 привзаємодії з водою сильно гідролізується з утворенням амфорного осаду гідратованого оксиду:
![]()
Задача 2.
Як взаємодіє ванадій сульфат з розчинами
![]() та
та ?
Складіть рівняння електронно- іонного
балансу.
?
Складіть рівняння електронно- іонного
балансу.
Розв’язок.
Ванадій сульфат
![]() з сильними окисниками виявляє відновні
властивості:
з сильними окисниками виявляє відновні
властивості:
![]()
а)![]()
![]()
![]() 2
2
![]() 5
5
![]()
Або після скорочення
![]() і
і![]() :
:
![]()
б)
![]()
![]()
![]() 1
1
![]() 6
6
![]()
Після скорочення
![]() і
і![]() сумарне іонне рівняння має вигляд:
сумарне іонне рівняння має вигляд:
![]()
Таким чином, сильні окисники
окиснюють іон ванадію до
![]() (у
гідратованій формі).
(у
гідратованій формі).
