
- •Предисловие
- •1. физические основы механики
- •1.1. кинематика материальной точки
- •1.1.1. Общие понятия механики.
- •1.1.2. Кинематика точки
- •1.1.3. Скорость
- •1.1.4. Ускорение
- •1.1.5. Примеры
- •1.2. ДИНАМИКА МАТЕРИАЛЬНОЙ ТОЧКИ
- •1.2.1. Основные понятия
- •1.2.2. Законы динамки поступательного движения
- •1.2.3. Вес тела
- •1.2.4. Инерциальные системы отсчета
- •1.2.5. Принцип относительности Галилея
- •1.2.6. Неинерциальные системы отсчета. Силы инерции
- •1.2.7. Закон сохранения импульса
- •1.2.9. Центр инерции
- •1.3. работа и энергия
- •1.3.1. Работа
- •1.3.2. Энергия
- •1.3.3. Кинетическая и потенциальная энергии
- •1.3.4. Закон сохранения механической энергии
- •1.3.5. Удар абсолютно упругих и неупругих тел
- •1.4. вращательное движение твердого тела
- •1.4.1. Кинематика вращательного движения
- •1.4.2. Кинетическая энергия вращательного движения. Момент инерции
- •1.4.3. Основное уравнение динамики вращательного движения
- •2. МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
- •2.1.1. Предмет молекулярной физики
- •2.1.2. Термодинамические параметры
- •2.1.3. Идеальный газ
- •2.1.4. Основное уравнение МКТ газов для давления
- •2.2. движение газовых молекул
- •2.2.1. Скорость теплового движения молекул
- •2.2.2. Распределение молекул по скоростям (закон Максвелла)
- •2.2.3. Закон распределения Больцмана
- •2.2.4. Число столкновений и средняя длина свободного пробега молекул
- •2.3. первое начало термодинамики
- •2.3.1. Внутренняя энергия идеального газа
- •2.3.3. Работа при расширении газа
- •2.3.5. Адиабатический процесс
- •2.4. второе начало термодинамики
- •2.4.1. Характеристики тепловых процессов
- •2.4.2. Принцип действия тепловой машины
- •2.4.3. Второе начало термодинамики
- •2.4.4. Энтропия
- •2.5. реальные газы
- •2.5.1. Отклонение свойств газов от идеальных
- •2.5.3. Критическое состояние вещества
- •2.6. жидкости
- •2.6.1. Свойства жидкостей
- •2.6.2. Поверхностное натяжение
- •2.6.3. Явление смачивания
- •2.6.5. Капиллярность
- •2.6.6. Тонкие слои жидкости
- •2.6.7. Поверхностно-активные вещества. Адсорбция
- •3. электричество и магнетизм
- •3.1. электрические заряды и электрическое поле
- •3.1.1. Взаимодействие тел
- •3.1.2. Электрический заряд
- •3.1.3. Закон Кулона
- •3.1.4. Единицы заряда
- •3.1.5. Электрическое поле
- •3.1.7. Теорема Гаусса
- •3.2. потенциал электрического поля
- •3.2.1. Работа сил электрического поля
- •3.2.3. Потенциал электрического поля
- •3.2.5. Эквипотенциальные поверхности
- •3.3. электростатика диэлектриков
- •3.3.1. Проводники и диэлектрики
- •3.3.2. Поляризационные заряды в диэлектриках
- •3.3.4. Типы диэлектриков
- •3.3.5. Вектор поляризации
- •3.3.6. Поляризация диэлектриков
- •3.3.7. Вектор поляризации и связанные заряды
- •3.3.8. Электрическое поле в диэлектриках
- •3.3.9. Теорема Гаусса для диэлектриков. Электрическое смещение
- •3.3.10. Сегнетоэлектрики
- •3.4.1. Электрическое поле заряженного проводника
- •3.4.2. Электроемкость
- •3.4.3. Емкость проводящей сферы
- •3.4.4. Конденсаторы
- •3.4.5. Энергия электростатического поля
- •3.5. постоянный электрический ток
- •3.5.1. Электрический ток
- •3.5.2. Сила и плотность тока
- •3.5.3. Источники тока. ЭДС
- •3.5.4. Закон Ома. Сопротивление проводников
- •3.5.5. Правила Кирхгофа
- •3.5.6. Работа и мощность тока
- •3.6. электропроводность металлов
- •3.6.1. Свободные электроны в проводниках
- •3.6.2. Свойства электронного газа
- •3.7. ток в полупроводниках
- •3.7.1. Полупроводники
- •3.7.2. Собственная проводимость полупроводников
- •3.7.3. Примесная проводимость полупроводников
- •3.7.4. Применение полупроводников
- •3.8. магнитное поле
- •3.8.1. Магнитные силы
- •3.9. магнитное поле проводников с током
- •3.9.1. Магнитное поле токов
- •3.9.3. Магнитный поток
- •3.9.5. Закон полного тока
- •3.10. электромагнитная индукция
- •3.10.1. Закон электромагнитной индукции
- •3.10.2. Правило Ленца
- •3.10.3. Возникновение индукционного тока в витке
- •3.10.4. Явление самоиндукции
- •3.10.5. Магнитная проницаемость вещества
- •3.10.6. Энергия магнитного поля
- •3.11. магнитные свойства веществ
- •3.11.1. Магнитное поле в веществе. Вектор намагничивания
- •3.11.3. Элементарные носители магнетизма
- •3.11.4. Диамагнетизм
- •3.11.5. Парамагнетизм
- •3.11.6. Ферромагнетики
- •3.12. уравнения максвелла
- •3.12.1. Общая характеристика уравнений
- •3.12.3. Второе уравнение Максвелла. Ток смещения
- •3.12.4. Полная система уравнений Максвелла
- •4. КОЛЕБАНИЯ И ВОЛНЫ
- •4.1. колебательное движение
- •4.1.1. Общие сведения о колебаниях
- •4.1.2. Механические колебания
- •4.1.4. Гармонические колебания в электрической системе
- •4.1.6. Сложение двух перпендикулярных гармонических колебаний
- •4.2. свободные и вынужденные колебания
- •4.2.1. Затухающие колебания
- •4.2.2. Характеристики затухания
- •4.2.3. Вынужденные колебания
- •4.3.1. Образование и распространение волн в упругой среде
- •4.3.2. Уравнение бегущей волны
- •4.3.3. Энергия упругих волн
- •4.4. электромагнитные волны
- •4.4.1. Свойства электромагнитных волн
- •4.4.3. Шкала электромагнитных волн
- •5. ОПТИКА
- •5.1. ИНТЕРФЕРЕНЦИЯ СВЕТА
- •5.1.1. Предмет оптики
- •5.1.2. Световая волна
- •5.1.3. Интерференция волн. Когерентность
- •5.2. Дифракция света
- •5.2.2. Метод зон Френеля. Прямолинейное распространение света
- •5.2.3. Дифракция на щелях
- •5.3.1. Естественный и поляризованный свет
- •5.3.4. Закон Малюса
- •5.3.5. Поляризация при отражении и преломлении
- •5.3.6. Вращение плоскости поляризации
- •5.3.7. Применение поляризации
- •5.4.1. Проблема теплового излучения
- •5.4.2. Законы теплового излучения абсолютно черного тела
- •5.4.3. «Ультрафиолетовая катастрофа»
- •5.4.4. Квантовая гипотеза Планка
- •5.4.5. Фотоэффект
- •5.4.6. Фотон и его свойства
- •6. ЭЛЕМЕНТЫ АТОМНОЙ ФИЗИКИ
- •6.1. введение в квантовую механику
- •6.1.1. Волновые свойства частиц
- •6.1.2. Физический смысл волн де Бройля
- •6.1.3. Волновая функция
- •6.1.4. Соотношение неопределенностей
- •6.2. квантовомеханическое описание движения частиц
- •6.2.1. Уравнение Шредингера
- •6.2.2. Частица в потенциальной яме
- •6.3. строение атома
- •6.3.1. Корпускулярная модель атома
- •6.3.2. Квантовомеханическое описание водородного атома
- •6.4. многоэлектронные атомы
- •6.4.1. Спин электрона
- •6.4.2. Принцип Паули
- •6.4.3. Электронная структура оболочек атомов
- •6.4.4. Рентгеновские лучи
- •7. ЭЛЕМЕНТЫ ЯДЕРНОЙ ФИЗИКИ
- •7.1. атомное ядро
- •7.1.1. Состав атомного ядра
- •7.1.2. Энергия связи ядра
- •7.1.3. Ядерные силы
- •7.1.4. Модели ядра
- •7.2. радиоактивный распад ядер
- •7.2.1. Явление радиоактивности
- •7.2.3. Альфа-распад
- •7.3. ядерные реакции
- •7.3.1. Уравнение ядерной реакции
- •7.3.2. Законы сохранения в ядерных реакциях
- •7.3.3. Составное ядро
- •7.3.4. Типы ядерных реакций
- •7.3.5. Трансурановые элементы
- •7.4. физические основы ядерной энергетики
- •7.4.1. Деление ядер
- •7.4.2. Термоядерные реакции
- •8. ВВЕДЕНИЕ В ТЕОРИЮ ФИЗИЧЕСКИХ ИЗМЕРЕНИЙ
- •8.1. Единицы и размерности физических величин
- •8.2.1. Погрешности прямых измерений
- •8.2.3. Учет инструментальной и случайной погрешностей
- •8.2.4. Исключение промахов
- •8.2.6. Точность измерительных приборов
- •8.2.7. О точности вычислений
- •8.2.8. Графические методы обработки результатов измерений
- •СОДЕРЖАНИЕ
- •Конспект лекций по физике
−
7.4.ФИЗИЧЕСКИЕ ОСНОВЫ ЯДЕРНОЙ ЭНЕРГЕТИКИ
7.4.1.Деление ядер
В 1938 г. немецкие ученые О. Ган и Ф. Штрассман, исследуя состав урана, облученного нейтронами, обнаружили в нем барий. Появление бария, расположенного в середине периодической системы Менделеева, объяснилось впоследствии способностью урана делиться под действием нейтронов на два новых ядра – осколки деления.
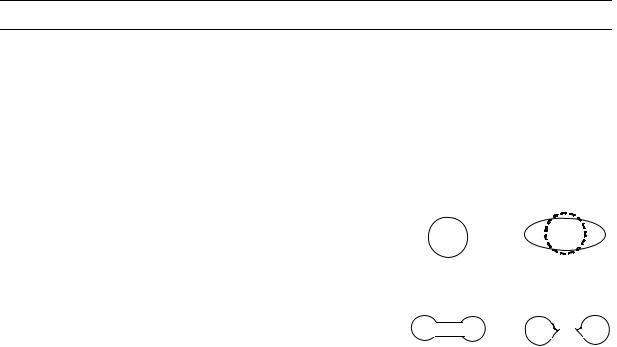
При поглощении нейтрона ядро возбуждается и начинает деформировать-
ся. Этот процесс может пройти ряд фаз (рис. 7.4.1). |
|
|
|
||||
Сначала сферическое |
ядро (а) |
принимает |
|
|
|
||
форму эллипсоида |
(б). Если возбужденное ядро |
|
|
|
|||
опять принимает сферическую форму, то ядро ис- |
|
а) |
б) |
||||
пускает |
γ-кванты и переходит в основное состоя- |
|
|
|
|||
ние. Если же энергия возбуждения больше энергии |
|
|
|
||||
порога деления ЕД, |
то ядро может принять форму |
|
в) |
г) |
|||
гантели |
(в) и под действием кулоновских сил от- |
|
|||||
талкивания разорваться по перемычке на два оскол- |
|
Рис. 7.4.1 |
|
||||
ка деления (г). |
|
|
|
|
|
||
|
|
|
|
|
|
||
Исследования процесса деления урана выявили ряд особенностей для та- |
|||||||
кой реакции. |
|
|
|
|
|
|
|
Деление ядра урана сопровождается выделением большого количества |
|||||||
энергии – около 200 Мэв на каждое деление. |
92U235 |
(0,7%) и |
92U238 |
||||
Природный уран состоит из двух изотопов |
|||||||
(99,33%) |
любых энергий, |
а U235 |
делится только нейтронами с энергией |
||||
~ 1 МэВ.
При расщеплении ядра урана выделяются вторичные нейтроны в количестве от двух до трех на каждый акт деления. Эти вторичные нейтроны при столкновении с другими ядрами могут ими захватываться и вызывать уже их деление, что при определенных условиях приводит к возникновению цепной реакции деления.
Осколки деления могут быть самыми разнообразными. Всего образуется около 80 различных осколков, но наиболее вероятным является деление на ос-
колки, массы которых относятся как 2:3. |
Например, возможны следующие ре- |
акции деления: |
|
92 U235 + n →34 Xe139 +38 Sr95 + 2n; |
92 U235 + n →56 Ba139 +36 Kr94 + 3n |
Энергия, выделяющаяся при делении, может быть рассчитана по дефекту масс. Так, для первой из указанных реакций деления находим
W = [M (U235 )+ mn − M (Xe139 )− M (Sr95 )− 2mn ]931 ≈ 200 МэВ.
Эта энергия распределяется следующим образом:
− |
|
|
кинетическая энергия осколков – 162 МэВ, |
N |
K > 1 |
энергия нейтронов деления – 6 МэВ, |
|
|
энергия радиоактивного излучения – 30 МэВ. |
|
K = 1 |
Размножение нейтронов при делении одних |
|
|
ядер создает условие для деления других. Если по- |
|
K < 1 |
сле каждого деления испускаются три нейтрона – |
|
|
нейтроны первого поколения, то после следующе- |
|
t |
го акта деления они создадут 32 = 9 нейтронов |
|
Рис. 7.4.2 |
второго поколения. В третьем поколении будет уже |
|
|
33 = 27 нейтронов и т.д. Такова схема размножения нейтронов. Реакции с размножением нейтронов являются цепными реакциями. Условие существования цепной реакции выражается через коэффициент размножения К. Коэффициентом размножения нейтронов называют отношение числа нейтронов в данном
поколении N |
1 |
к числу нейтронов N в предыдущем: |
K = |
N1 |
. Из этого опре- |
|
|||||
|
|
|
N |
||
|
|
|
|
||
деления следует, что приращение нейтронов за одно поколение равно N1 – N = N (K – 1). Если τ - среднее время между двумя актами деления, то увели-
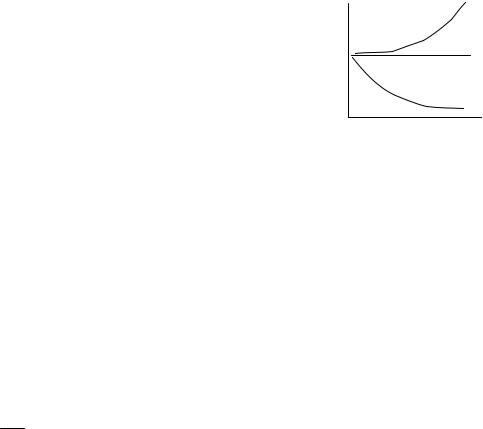
чение числа нейтронов за время dt равно dN = N (K −1)dtτ , откуда
−K−1
N = N0e τ . (7.4.1)
Графически эта зависимость изображена на рис. 7.4.2. При K < 1 цепная реакция невозможна, при К = 1 поддерживается цепная реакция с постоянным количеством нейтронов; такая реакция применяется в ядерных реакторах, при К > 1 число нейтронов непрерывно возрастает и реакция может стать взрывной, такая реакция соответствует атомной бомбе.
В действительности не все нейтроны вызывают деление.
Часть нейтронов теряется при радиационном захвате, другая часть вылетает из объема. Эти потери влияют на ход цепной реакции и коэффициент размножения. Чтобы снизить уход нейтронов из объема, надо сократить поверхность делящегося вещества, т.е. придать ему шарообразную форму. Увеличивая массу делящегося вещества, можно достичь такого состояния, при котором К = 1, и реакция деления становится незатухающей. Предельная масса, при которой выполняется такое условие, называется критической массой. Для чисто-
го U235 она составляет 40 кг (для шарообразной формы).
7.4.2. Термоядерные реакции
Получение ядерной энергии возможно и за счет реакции синтеза легких ядер, например, гелия из ядер водорода. Чтобы произошло слияние ядер, необходимо сообщить им достаточную кинетическую энергию для преодоления электрических сил отталкивания. Такая энергия может быть достигнута за счет нагревания до высоких температур, поэтому реакция синтеза называют термоядерными реакциями. Подсчитаем, например, температуру, до которой необхо-
−
димо нагреть водород, чтобы преодолеть силы электростатического отталкивания между ядрами. Для этого необходимо двум протонам сблизиться до рас-
стояния 10-12 см, |
т.е. преодолеть электростатический потенциальный барьер: |
|||||||||
W = |
e2 |
= |
(4,8 |
10−10 )2 |
= 2,3 10 |
−7 |
эрг = 0,14 МэВ. |
|||
r |
10−12 |
|
||||||||
|
|
|
|
|
|
|||||
Эта энергия соответствует температуре |
||||||||||
W = |
3 kT T = |
2 2,3 10−7 |
≈1,1 109 K . |
|||||||
3 1,38 10−16 |
||||||||||
|
2 |
|
|
|
|
|
|
|||
Однако, синтез легких ядер может протекать и при более низких температурах (~107) вследствие туннельного эффекта. В искусственных условиях термоядерный синтез впервые был осуществлен при взрыве водородной бомбы. Высокая температура, необходимая для начала термоядерной реакции, создава-
лась при взрыве обычной атомной бомбы (Т~107 К). Синтез дейтерия 1Н2 и трития 1Н3
1 H2 +1H3→2 He4 + n
сопровождается выделением энергии 17,6 МэВ или ~3,5 МэВ на нуклон. Это значительно больше, чем при реакции деления, где на один нуклон выделяется ~0,85 МэВ.
Вводородной бомбе термоядерная реакция носит неуправляемый характер. Для осуществления управляемой термоядерной реакции необходимо создать и поддерживать очень высокую температуру. При такой температуре вещество представляет полностью ионизированный газ или плазму. Для удержания плазмы в ограниченном объеме изолировано от стенок сосуда используют магнитное поле. Осуществление управляемых термоядерных реакций даст неисчерпаемый источник энергии.
Энергия, выделяемая при этом в расчете на один нуклон, составляет примерно от 1 до 4 МэВ/нуклон, что значительно больше, чем при реакциях деления (0,85 МэВ/нуклон).
Вестественных условиях такие реакции протекают в недрах Солнца и звезд. Солнце и звезды состоят в основном из водорода, поэтому главное зна-
чение в «жизни» звезды имеют реакции синтеза ядер водорода 1Н1 в более тя-
желые ядра, чем 2Н2.
Четыре ядра водорода при слиянии в ядро гелия выделяют два позитрона и огромную энергию (26,7 МэВ). За счет этой энергии термоядерные реакции являются самоподдерживающимися.
В настоящее время считают, что существуют два возможных пути слияния ядер водорода в ядра гелия.
Протонно-протонный цикл состоит из следующей цепочки превращений:
1H1 +1 H1 →1 He2 +β+ + ν 1 H2 +1 H1 →1 H3 + γ
