
6 курс / Кардиология / Аритмии_сердца_Механизмы,_диагностика,_лечение_в_3_х_томах_Том_2
.pdf
Рис. 1.9. Периодика Венкебаха, сопровождающаяся расширением комплексов QRS.
При АВ-блокаде II степени часто наблюдаются отдельные реципрокные предсердные возбуждения, нарушающие типичную последовательность Венкебаха. Пример такого явления с широкими комплексами QRS дан на рис. 1.10; на представленной ЭКГ первые три Р-волны проводятся в желудочки с прогрессивно возрастающим (от 0,28 до 0,34 с) интервалом P—R, что предполагает наличие АВблокады типа I. Однако зубец Г третьего сокращения деформируется и появление следующей синусовой Р-волны задерживается, что показывает наложение преждевременного зубца Р. Прогрессивное увеличение времени АВ-проведения перед возникновением столь ранней предсердной деполяризации четко указывает на возврат возбуждения в предсердие [41—45], поэтому последовательность активации интерпретируется так, как показано на лестничной диаграмме.
После возвратного предсердного возбуждения два последовательных синусовых импульса вновь успешно проводятся в желудочки с увеличивающимся интервалом Р—R. Но на этот раз третий синусовой импульс, возникающий своевременно, не сопровождается комплексом QRS. Таким образом, налицо типичная периодика Венкебаха с отношением проведения 3:2. Основываясь на анализе предыдущих сокращений, можно приписать проведение 3:2 скрытому отражению второго синусового импульса, которое вызывает рефрактерность АВ-соединения к моменту прихода третьего синусового импульса. Некоторые исследователи склонны подчеркивать роль этого механизма во всех случаях блокады, протекающей по типу Венкебаха, и скрытое отражение волны возбуждения действительно может иметь место в АВсоединении (см. рис. 1.8). Изменение формы комплекса QRS в сокращениях, появляющихся после долгой паузы (сокращения 4 и 6 на рис. 1.10), может объясняться либо более полным восстановлением проводимости в угнетенной ножке (или ветви) пучка Гиса, либо задержкой проведения в других ветвях вследствие деполяризации в фазу 4 (так называемый блок во время фазы 4), несколько изменяющей характер желудочковой активации. Следует также отметить, что не во всех случаях появление эктрасистолических Р-волн в ходе периодики Венкебаха может быть отнесено на счет механизма отражения; возникшие внутри предсердий в определенный момент эктопические импульсы также способны нарушить течение АВблокады типа I.

Рис. 1.10. ЭКГ во II стандартном отведении: прерывание цикла Венкебаха отраженным предсердным импульсом (слева) и блокада II степени (тип I) с отношением проведения 3:2 (справа).
Феномен Венкебаха, или прогрессивное увеличение времени проведения вплоть до полного блокирования импульса, может наблюдаться в любой области миокарда, где проводимость подавлена и имеется состояние декрементного проведения. Другими словами, этот феномен не является исключительным свойством АВ-узла и может иметь место даже в волокнах Пуркинье или в пределах прилегающих волокон желудочкового миокарда [б, 46,47]. В некоторых клинических случаях электрография пучка Гиса также показывает существование периодики Венкебаха ниже АВ-узла или в системе Гиса—Пуркинье [26]. Более того, в отдельных случаях постепенное изменение формы QRS предполагает прогрессивное замедление проведения в одной из ножек или ветвей пучка Гиса вплоть до полного блока проведения, хотя при этом обычно не наблюдается увеличения интервала Р—R, соответствующего периодике Венкебаха [17,48]. Таким образом (по крайней мере в большинстве случаев), АВ-блокада II степени типа I предполагает задержку проведения в АВ-узле, как это было показано в эксперименте [8]. Полученные данные позволяют сделать вывод, что периодика Венкебаха предполагает локализацию нарушений проведения в пределах АВ-узла, тогда как сопутствующие признаки блокады правой ножки указывают на аномалии внутрижелудочкового проведения, как в случае, показанном на рис. 1.9 [30]. Электрография пучка Гиса, очевидно, сыграет большую роль в изучении подобных случаев. Однако при невозможности использования данного метода обсуждавшиеся выше предположения о двух уровнях нарушений проведения могут служить надежной базой для клинического ведения больных с такого рода аритмией [17,30].
Рис. 1.11. Электрограмма пучка Гиса (Гис) при АВ-блокаде с широкими комплексами QRS.
Р — зубец Р; А — предсердия; Н — пучок Гиса; V — желудочки.
На рис. 1.11 представлена электрограмма пучка Гиса, полученная при АВблокаде 2:1 с широкими комплексами QRS. В этом случае каждый второй синусовый импульс проводится в желудочки с интервалом P—R 190 мс, причем интервал Р—А (от начала зубца Р до момента активации нижней части правого предсердия на электрограмме пучка Гиса) составляет 30 мс, интервал А—Н — 95 мс, а Н—V (от Н- потенциала до начала желудочковой активации) — 65 мс. Хотя длительность интервала Н—V лишь незначительно превышает норму, блокированные предсердные импульсы всегда сопровождаются Н-потенциалом, что свидетельствует об успешном проведении по крайней мере в определенной части пучка Гиса. Следовательно, место блока должно быть ниже регистрирующего электрода. Необходимо отметить, что
точное определение области пучка Гиса, расположенной наиболее близко к регистрирующему электроду, невозможно. Поэтому бывает трудно установить место блокирования импульсов — ниже бифуркации пучка Гиса или между точкой регистрации и бифуркацией этого пучка, хотя наличие расширенных комплексов QRS, указывающих на внутрижелудочковые нарушения проведения, говорит в пользу блокады на уровне ножек или ветвей пучка Гиса,
Как отмечается в более поздних исследованиях, наличие двух уровней блока при так называемом скрытом проведении является наиболее вероятной причиной альтерации интервала Р—R в случае стабильного проведения 2:1 [9, 32]; это показано на рис. 1.12. В данном эксперименте, проведенном на изолированном перфузируемом сердце кролика, одновременно осуществлялись предсердная электрография области синусового узла, желудочковая электрография и регистрация трансмембранных потенциалов в области NH АВ-узла. Синусовый цикл составил 530 мс, что соответствует частоте 113 уд/мин. В верхней части записи (см. рис. 1.12, А) каждый предсердный импульс сопровождается деполяризацией волокна NH с нормальной амплитудой и нарастанием скорости потенциала действия, что предполагает проведение 1 :1 по области N АВ-узла. Однако после каждого второго потенциала действия волокна NH не наблюдается желудочкового возбуждения, что указывает на наличие блока проведения 2: 1 ниже АВ-узла или в системе Гис— Пуркинье. Нарушение внутрижелудочкового проведения определяется здесь по аномальному и уширенному желудочковому комплексу, а также по существенному увеличению времени поду зло во го проведения (до 160 мс; сравните с его нормальным значением 30—35 мс). Время проведения от синусового узла до дистальной части волокна NH составляет 102—104 мс. Поскольку по другим записям время внутрипредсердного проведения определялось в 35 мс, время внутриузлового проведения также увеличивалось до 67—69 мс. Эти наблюдения свидетельствуют о наличии нарушений проведения как в АВ-узле, так и в системе Гис—Пуркинье, хотя нарушение распространения возбуждения отмечается только в системе Гис—Пуркинье.
На нижней записи (см. рис. 1.12, Б), полученной через 3 мин после верхней (см. рис. 1.12, А), присутствие АВ-блока 2:1 четко видно на желудочковой электрограмме. Однако при этом наблюдается чередование (альтерация) коротких (234 мс) и длинных (262—264 мс) интервалов АВ-проведения. Это обусловливает и чередование коротких и продолжительных желудочковых циклов. Механизм такой альтерации становится очевидным при исследовании записи мембранного потенциала области NH. Как показывает анализ, здесь каждый четвертый синусовый импульс не может активировать волокно NH, что указывает на проведение через N-область АВузла в отношении 4:^3. Этот внутриузловой блок характеризуется типичной периодикой Венкебаха с прогрессивным увеличением интервала проведения от синусового узла до области NH (от 104 до 116 и 124 мс). Второй из трех синусовых импульсов, успешно прошедших через АВ-узел, блокируется ниже области NH, как показано на рис. 1.2, А, тогда как первый и третий импульсы оказываются в состоянии достичь желудочков. Время проведения импульса в сокращении 3 гораздо больше, чем в сокращении 1, что обусловлено не только замедлением внутриузлового проведения, но и возрастанием длительности проведения по системе Гис—Пуркинье со 130 до 140 мс. Такое увеличение времени проведения по системе Гис—Пуркинье может объясняться частичным проникновением второго предсердного импульса в эту систему, что создает рефрактерность проводящей ткани. После блокирования четвертого синусового импульса выше области NH АВ-узла уменьшается длительность проведения как внутри узла, так и в системе Гис—Пуркинье, в результате чего время АВ-проведения вновь составляет 234 мс. Таким образом, ясно, что в данном случае АВ-блокада 2:1 с альтернацией интервала АВ-проведения вызвана наличием двух уровней нарушения проведения и чередованием внутриузлового и подузлового блоков.

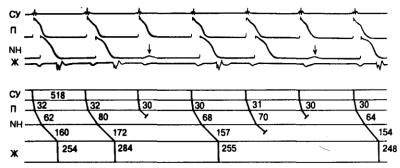
Рис. 1.12. Потенциалы действия, зарегистрированные в сердце кролика при АВ-блокаде 2:1 с чередованием коротких и длинных интервалов АВ-проведения.
СУ — синусовый узел; NH — область NH АВ-узла; Ж — желудочки.
Хотя более длительный интервал АВ-проведения на рис. 1,12, Б почти равен постоянному АВ-интервалу на рис. 1.12, А, где нарушение проведения всегда отмечается ниже АВ-узла, отношение внутриузлового и подузлового времени проведения значительно отличается на этих двух записях. Это наглядно показывает, что интервал Р—R на ЭКГ, полученной в клинических условиях, представляет сумму внутрипредсердного, внутриузлового и подузлового времени проведения, и вклад каждого из указанных компонентов оценить непросто. Тем не менее представленные здесь экспериментальные данные весьма напоминают данные клинических электрограмм, что говорит в пользу концепции скрытого проведения как механизма наблюдаемых явлений [6]. Следует также отметить, что АВ-блокада 2:1 с чередованием коротких и длинных интервалов АВ-проведения может .наблюдаться только при отношении внутриузлового проведения 4:3. При наличии внутриузлового проведения 3:2 желудочковые ответы будут следовать либо в отношении 3:2, либо в отношении 3:1 (см. рис. 1.15). Классификация по типу I или II вряд ли может быть использована в случаях, представленных на рис. 1.11 и 1.12. В подобных случаях классификация, как и клинические подходы, должна основываться на предположении о самом нижнем уровне блока. С другой стороны, интерпретация чередования длинных и коротких интервалов Р—R при наличии проведения 2: 1 может базироваться на предположении о существовании двух функционально (или анатомически) независимых групп проводящих волокон, что соответствует концепции так называемых двойных путей АВ-проведения [41—45,49]. В самом деле, в ряде клинических и экспериментальных исследований показана возможная роль двойных путей при АВпроведении и внутрипредсердном или межпредсердном проведении 4 [41,42]. Однако микроэлектродные исследования четко показали, что типы проведения, наблюдаемые при наличии двойных путей, могут объясняться неоднородным (в различной степени) проведением и существованием задержки проведения на нескольких уровнях (см. рис. 1.12 и 1.13).
Продвинутая атриовентрикулярная блокада второй степени и бл о када третьей степени типа А 1
1 По классификации авторов, тип А обозначает вариант АВ-блокады с нормальной формой комплекса QRS, а тип Б — вариант АВ-блокады с расширенным комплексом QRS. — Примеч. переводчика.
|
Термин «продвинутая АВ-блокада II степени» применяется в тех случаях, |
когда |
блокируется более двух последовательных наджелудочковых импульсов [9]. |
Хотя |
отличить этот вариант блокады от АВ-блокады III степени (при ее наличии) |

бывает трудно, все же при блокаде III степени большинство желудочковых комплексов является следствием импульсов, возникающих во вторичном источнике автоматизма, тогда как при продвинутой блокаде II степени активация желудочков контролируется преимущественно незаблокированными наджелудочковыми импульсами. Тип проведения, при котором один синусовый импульс проводится в желудочки и за ним следуют два заблокированных импульса, называется проведением 3:1, тогда как успешное проведение только одного из четырех предсердных импульсов определяется как проведение 4:1. Несколько примеров этого типа блокады обсуждаются ниже.
На рис. 1.13 показана экспериментальная регистрация трансмембранных потенциалов действия в области АВ-узла, а также электрокардиограмма и лестничная диаграмма для анализа последовательности активации [9]. В начальной части рис.
1.13отмечается несколько периодов АВ-проведения 2:1, в которых АВ-интервал
обнаруживает чередование коротких и длительных циклов, составляющих 202, 138, 190 и 150 мс. Нарушение проведения происходит всегда выше волокна NH, а время проведения по системе Гис—Пуркинье (или подузловое время) остается постоянным и почти соответствующим норме. Судя по желудочковым комплексам на ЭКГ, нарушения внутрижелудочкового проведения отсутствуют. Таким образом, здесь, по-видимому, имеется только один уровень блока. Однако колебания амплитуды местных ответов волокна NH наводят на мысль, что альтернация времени АВ-проведения обусловлена различием в глубине проникновения в АВ-узел блокированных предсердных импульсов. Например, вторая и шестая волны предсердного возбуждения (низкоамплитудные двухфазные колебания на электрокардиограмме) едва ли сопровождаются какими-либо изменениями мембранного потенциала покоя волокна NH, в то время как четвертый предсердный импульс вызывает некоторое изменение потенциала (местный ответ), что указывает на несколько более глубокое проникновение возбуждения. Это увеличивает время АВ-проведения пятого предсердного импульса по сравнению с другими неблокированными импульсами — эффект скрытого проведения. Как отмечалось выше, за периодом АВ-проведения 2:1 следует период проведения 4:1. Во время проведения 4: 1 второй из трех последовательных заблокированных импульсов вызывает несколько большее изменение потенциала, что предполагает более глубокое проникновение этого импульса в узел. Аналогичное явление обычно наблюдается при наличии проведения 4:1.
Рис. 1.13. Продвинутая АВ-блокада II степени с переменной глубиной проникновения предсердного импульса в АВ-узел (АВУ).
На представленной на рис. 1.13, Б записи, полученной через 3 мин после регистрации, показанной на рис. 1.13, А, за тремя периодами АВ-проведения 2: 1 следуют ответы 3:1 и 4:1. Регистрация трансмембранного потенциала в N-области АВ-узла во время проведения 2:1 вновь демонстрирует колебания уровня нарушения проводимости, обусловливающие чередование периодов времени АВ-проведения. Когда блокированный импульс проникает глубже в АВ-узел, последующий потенциал действия
волокна обнаруживает снижение скорости нарастания фронта при смазывании или зазубривании нулевой фазы. Получение таких данных предполагает наличие либо декрементного, либо неравномерного проведения. Исходя из последовательности чередования степени проникновения возбуждения — во время периодов проведения 2:1, следовало бы ожидать, что шестой предсердный импульс заблокируется где-то в проксимальной части АВ-узла, однако он, по-видимому, проникает все глубже, судя по амплитуде соответствующего локального ответа. Внутриузловое блокирование последующего (седьмого) предсердного импульса и возникновение отношения проведения 3:1 скорее всего обусловлено этим более глубоким скрытым проведением. Таким образом, при продвинутой АВ-блокаде II степени вариации глубины проникновения возбуждения, видимо, являются правилом, даже если нарушение проведения всегда происходит в ткани АВ-узла.
Развитию АВ-блокады способствуют и другие механизмы, такие как скрытая циркуляция возбуждения [9].
Когда условия, сходные с трепетанием предсердий, создаются экспериментально с помощью повышения частоты предсердной стимуляции в изолированном сердце кролика, АВ-проведение 2: 1 обычно отмечается при достаточно высокой частоте стимуляции. В таких случаях каждый второй предсердный импульс блокируется внутри АВ-узла, хотя явления, аналогичные показанным на рис. 1.12, также иногда наблюдаются.
При АВ-блокаде III (или высокой) степени активация желудочков контролируется главным образом вторичным водителем ритма, а синусовые или предсердные импульсы редко проводятся в желудочки. Очевидно, что классификация типов I и II АВ-блокады II степени неприменима для этого варианта блокады.
В примере АВ-блокады III степени, представленном на рис. 1.14, А, наблюдается синусовая брадикардия с умеренной синусовой аритмией. Однако зубцы Р и комплексы QRS независимы друг от друга при постоянном желудочковом ритме 30 уд/мин. Ширина комплекса QRS не выходит за пределы нормы (0,07 с); следовательно, автоматический фокус скорее всего располагается выше .бифуркации пучка Гиса. Это предполагает локализацию блока над вторичным водителем ритма, вероятно, внутри АВ-узла [17,30,33].
На рис. 1.14, Б мелкие волны на уровне изолинии указывают на мерцание предсердий, при этом желудочковые комплексы появляются весьма регулярно при частоте 40 уд/мин. Таким образом, наличие вторичного водителя ритма вполне очевидно [15—17]. Для того чтобы такой механизм ускользания (escape) ритма сохранял свою активность, нужно постулировать очень высокую степень нарушения проведения с блокированием большинства импульсов, исходящих из мерцающих предсердий. Нормальная ширина комплексов QRS в этом случае предполагает локализацию блока проведения в предсердно-желудочковом соединении,- вероятнее всего, в АВ-узле. При введении высоких доз сердечных гликозидов и наличии нарушения проведения следует заподозрить прежде всего дигиталисную интоксикацию как механизм такого рода нарушений. С другой стороны, если желудочковые циклы на фоне мерцания предсердий не являются абсолютно регулярными, как в этом случае, а
многие |
интервалы |
R—R одинаковы, можно предположить частое возникновение |
импульсов ускользания как результат АВ-блокады II степени. Однако при отсутствии |
||
четких |
критериев |
оценки процентного отношения идентичных интервалов R—R |
(предполагающих ускользание ритма в каком-либо продолжительном фрагменте записи)
следует заподозрить блокаду II степени. Итак, |
диагноз в таких слу чаях может |
быть скорее субъективным, нежели эмпирическим, в отличие от случаев блокады III |
|
степени, представленных на рис. 1.14, Б. Тем |
не менее в подобных ситуациях |
клиницист не должен забывать о возможном влиянии |
препаратов наперстянки. |

Рис. 1.14. АВ-блокада III степени с неширокими комплексами QRS при синусовом ритме (А) и мерцании предсердий (Б).
Продвинутая атриовентрикулярная блокада второй степени и бл о када третьей степени типа Б
Продвинутая АВ-блокада II степени и АВ-блокада III степени могут также определяться при наличии широких комплексов QRS [33].
Экспериментальная запись, показанная на рис. 1.15, была получена через несколько минут после записи, представленной на рис. 1.12. На рис. 1.15 регистрация трансмембранных потенциалов в предсердном волокне, прилегающем к АВузлу (II), а также в области NH АВ-узла (NH) представлена вместе с электрограммами области синусового узла (СУ) и желудочков (Ж). В начальной части этого рисунка два последовательных предсердных импульса полностью деполяризуют волокно NH и проводятся в желудочки, но время проведения (как внутриузловое, так
ив системе Гис—Пуркинье) увеличивается при втором сокращении. Третий
предсердный импульс вызывает неполную деполяризацию волокна NH (показано стрелкой на рис. 1.15) и оказывается не в состоянии активировать желудочки. Следовательно, определяется проведение 3:2 с периодикой Венкебаха. Далее два предсердных импульса вновь вызывают нормальный потенциал действия в волокне NH,
что свидетельствует об успешном внутриузловом проведении. Однако только первый импульс проникает в желудочки, тогда как второй — блокируется ниже области NH, скорее всего в системе Гис—Пуркинье. Нарушение проведения третьего импульса возникает выше волокна NH, как в начальном цикле Венкебаха, в результате чего наблюдается ответ 3:1. Обратите внимание, что наличие двух уровней блока (внутри и ниже АВ-узла) сочетается с нарушением внутрижелудочкового проведения, о чем свидетельствует расширение комплексов QRS и увеличение времени проведения в системе Гис— Пуркинье. В отличие от отношения внутриузлового проведения 4; 3, наблюдаемого на рис. 1.12, отношение 3 : 2 на рис. 1.15 вполне может отражать дальнейшее угнетение внутриузлового проведения. И действительно, через некоторое время после регистрации, представленной на рис. 1.15, развилась внутриузловая блокада 2:1. Возможно, что когда нарушения внутрижелудочкового проведения достаточно выражены, чтобы вызвать АВ-блокаду, лежащие в их основе патофизиологические механизмы часто включают и область АВ-узла.
На рис. 1.15 второй из двух предсердных импульсов, успешно проходящих через АВ-узел, один раз активирует желудочки, а во второй раз блокируется в системе Гис — Пуркинье, хотя на уровне АВ-узла сохраняется отношение проведения 3:2. Краткое обсуждение этого механизма представляется нам необходимым. Вопервых, возможно, что проводимость системы Гис—Пуркинье обнаруживает временные колебания [9, 32]; таким образом, некоторое улучшение проводимости вызовет ответ 3:2. Тогда как ее ухудшение обусловит отношение проведения 3: 1 (как это видно в правой половине рис. 1.15). С другой стороны, блокирование третьего предсердного импульса внутри АВ-узла при наличии отношения 3:2 приведет к снижению частоты возбуждений в системе Гис—Пуркинье. Поэтому первое после такой паузы проведенное возбуждение будет сопровождаться заметным увеличением длительности потенциала действия и рефрактерного периода волокон Пуркинье. Вследствие повышения рефрактерности второй после паузы предсердный импульс может заблокироваться на уровне системы Гис—Пуркинье (механизм, часто относимый к блоку во время фазы 3). В рассматриваемом случае для действия данного механизма нужно предположить, что длительность потенциала действия волокон Пуркинье превышает 500 мс. Хотя такая длительность представляется довольно большой, подобные величины потенциала действия волокон Пуркинье часто отмечаются в различных экспериментальных условиях.
Рис. 1.15. Два уровня блока в сердце кролика (в АВ-узле и системе Гис-Пуркинье), обусловливающие АВ-проведение 3:2 и 3:1. СУ — синусовый узел; П — предсердия; Ж — желудочки.
Рис. 1.16 иллюстрирует случай АВ-блокады III степени с широкими комплексами QRS (сравните с QRS на рис. 1.19) [30,33]. На двух верхних фрагментах записи, произведенной 21 июня (рис. 1.16), синусовые зубцы Р, как и несколько эктопических зубцов Р, не имеют постоянной связи с желудочковыми возбуждениями и комплексы QRS следуют регулярно с частотой 44 уд/мин. Широкие комплексы QRS с признаками блокады правой ножки указывают на локализацию вторичного водителя ритма в системе левой ножки пучка (или вблизи нее). Диагноз АВ-блокады III степени не вызывает затруднений. В нижней части рис. 1.16 представлена электрокардиограмма, полученная двумя днями позже: регулярный желудочковый ритм сохраняется несмотря на наличие мерцания предсердий, определяемого по мелким волнам на уровне изолинии. Желудочковый ритм здесь

несколько ускорился (49 уд/мин). То, что конфигурация комплекса QRS не изменилась, видно в отведениях aVF и V1; это указывает на контроль желудочков со стороны того же вторичного фокуса, который наблюдался двумя днями раньше. Третье сокращение в отведении aVp и второе сокращение в отведении aVF (форма последнего искажена вследствие наложения калибровочного импульса 1 мВ) представляют желудочковые экстрасистолы. Поскольку интервал между экстрасистолическим комплексом QRS и следующим комплексом QRS ритма ускользания либо равен остальным интервалам R—R (в отведении aVp), либо несколько больше их (в отведении aVF), можно предположить преждевременную разрядку дополнительного пейсмекера при ретроградном проведении экстрасистолических импульсов и восстановление его автоматизма. В этом случае место нарушения проведения, вероятнее всего, находится ниже бифуркации пучка Гиса.
Рис. 1.16. АВ-блокада высокой степени с ритмом ускользания, возникающим в области левой ножки пучка Гиса как при синусовом ритме (вверху), так и при мерцании предсердия (внизу).
Однако следует отметить, что когда АВ-блокада высокой степени наблюдается на фоне мерцания предсердий, вероятность внутриузловых нарушений проведения (помимо подузлового блока) гораздо выше, чем в случаях синусового ритма при АВблокаде высокой степени. Причина этого заключается в следующем: поскольку волны предсердного возбуждения во время мерцания предсердий весьма нерегулярны и менее эффективны как стимулы АВ-узла [53—56], внутриузловой блок развивается значительно легче, чем при синусовом ритме. Следовательно, если имеется только электрокардиограмма, аналогичная представленной в нижней части рис. 1.16, особенно в случае приема дигиталиса, то прежде чем поставить диагноз блокады высокой степени на уровне системы Гис — Пуркинье, нужно заподозрить развитие АВблокады III степени на уровне АВ-узла в дополнение к предшествующей блокаде ножки пучка. При дифференциальной диагностике целесообразны сравнительный анализ аналогичных ЭКГ и временная отмена препаратов наперстянки, однако для окончательного диагноза в определенных случаях может потребоваться электрография пучка Гиса.
Другие механ измы, сп особствующие нарушению атриовентрик у лярного проведения

Хотя неоднородное проведение и фрагментация электрической активности проводящего пути обычно ведут к задержке и блоку проведения, другие явления, такие как одностороннее проведение, суммация и так называемое супернормальное проведение, могут служить объяснением необычных признаков, наблюдаемых на представленных далее рисунках.
В отношении перечисленных выше феноменов проведения определенный интерес представляют экспериментальные данные, полученные на изолированном сердце кролика (рис. 1.17). В течение периода АВ-проведения 4:3, наблюдаемого в средней части представленной записи, время АВ-проведения сначала возрастает со 190 до 210 мс, а затем вновь сокращается до 197 мс. Такие данные противоречат классическим признакам блокады типа I (периодика Венкебаха), и парадоксальное уменьшение АВ-интервала (вместо дальнейшего удлинения) может интерпретироваться как супернормальное проведение. При анализе трансмембранного потенциала волокна N-области АВ-узла (N) первый импульс цикла 4:3 имеет нормальную форму потенциала действия, тогда как второй предсердный импульс вызывает появление зазубренного потенциала действия при значительно сниженной скорости деполяризации, что приводит к увеличению времени проведения из N-области в желудочки (от 78 до 100 мс). Потенциал действия волокна N, связанный с третьим предсердным импульсом, дает сглаженное нарастание в нулевую фазу, хотя скорость деполяризации здесь ненамного больше, и время проведения в желудочки вновь сокращается до 85 мс. Последний (четвертый) предсердный импульс вызывает лишь неполную деполяризацию волокна N и не проводится в желудочки. Эти данные могут объясняться нашей концепцией неравномерного проведения следующим образом: значительная неравномерность внутриузлового проведения при втором сокращении обусловливает снижение эффективности волны возбуждения, тем самым замедляя проведение ниже N- области. Напротив, третье сокращение связано с более однородным фронтом возбуждения в АВ-узле, и его большая эффективность как стимулирующий фактор обусловливает более успешное под-узловое проведение. Таким образом, легкие колебания проводимости в пределах АВ-соединения вполне могут вызвать супернормальное проведение такого типа [9, 32, 33], хотя причины подобных колебаний определить нелегко.
Рис. 1.17. Экспериментальная регистрация так называемого супернормального проведения (условные обозначения те же, что и на предыдущих рисунках).
Некоторые явления аномального проведения, возникающие в результате изменений первичных детерминант проводимости (см. перечень факторов в начале этой главы), заслуживают короткого комментария. Во-первых, термин «декрементное проведение» можно определить. как постепенное уменьшение стимулирующей эффективности и амплитуды ответа на пути проведения импульса по анатомически однородной, но функционально подавленной ткани [38,40]. Из предыдущего обсуждения нетрудно понять, что декрементное проведение легче возникнет в N- области АВ-узла, где потенциалы действия обнаруживают малую крутизну фронта и снижение амплитуды даже в физиологических условиях [45, 57]. Верно то, что последовательные изменения характеристик потенциала действия на пути от
