
6 курс / Гастроэнтерология / Российский_журнал_гастроэнтерологии,_гепатологии,_колопроктологии (54)
.pdf
|
|
3, |
2009 |
|
|
|
|
Редакционная |
|
|
|
|
|
|
|
|
|
|
|
комбинированным выключением NEMO и IKK1 |
со стороны CD8+ цитотоксических |
Т-клеток) |
|||||||
в печеночных паренхиматозных клетках также |
и экспрессию молекул HLA класса II на анти- |
||||||||
спонтанно заболевают тяжелой |
холестатической |
генпрезентирующих клетках и на гепатоцитах, |
|||||||
болезнью печени, сходной по своим проявлениям |
что расширяет масштаб активации Th0-клеток. |
||||||||
с таковой при комбинированном печеночно-спе- |
Th-2-клетки продуцируют преимущественно IL-4, |
||||||||
цифическом выключении IKK1/IKK2. В целом |
IL-10 и IL-13, которые благоприятствуют продук- |
||||||||
указанные данные позволяют считать, что комби- |
ции аутоантител В-лимфоцитами. Th-17-клетки |
||||||||
нированное ингибирование канонического NF-kB- |
играют важную роль |
в развитии |
воспаления |
||||||
сигнального пути и IKK1-специфических функ- |
и аутоиммунной реактивности. Процесс распо- |
||||||||
ций повышает готовность печени к спонтанной |
знавания аутоантигенов |
строго контролируется |
|||||||
воспалительной |
деструкции |
внутрипеченочных |
регуляторными механизмами, в частности CD4+ |
||||||
желчных протоков и развитию холестатической |
CD25+ регуляторными Т-клетками, которые диф- |
||||||||
болезни [13]. |
|
|
|
|
|
ференцируются из Th0-клеток при наличии в |
|||
Вместе с тем выключение NEMO в пече- |
микроокружении TGF-β. Дефект иммунорегу- |
||||||||
ночных паренхиматозных клетках вызывает у |
ляции вследствие дефицита или функциональ- |
||||||||
мышей спонтанное развитие гепатоцеллюлярной |
ной недостаточности CD4+ CD25+ регуляторных |
||||||||
карциномы (ГЦК). Появлению опухоли предше- |
Т-клеток обнаружен у нелеченных больных ауто- |
||||||||
ствует развитие хронического заболевания пече- |
иммунным гепатитом и в период обострения забо- |
||||||||
ни, напоминающего неалкогольный стеатогепатит |
левания. Обладатели аллелей HLA-DRB1*0301 и |
||||||||
человека. Результаты терапии антиоксидантами |
HLA-DRB1*0401 предрасположены к развитию |
||||||||
и генетического выключения FADD у мышей |
аутоиммунного гепатита. |
|
|
||||||
этой модели указывают на то, что патогенез ГЦК |
При первичном билиарном циррозе эпитопами |
||||||||
включает повреждение дефицитных по NEMO |
для антимитохондриальных антител класса IgG |
||||||||
гепатоцитов, которое обусловлено активацией |
служат протеины внутренней митохондриальной |
||||||||
рецепторов гибели и оксидативным стрессом. |
мембраны, которые представлены энзимами пиру- |
||||||||
Отсюда следует, что NEMO-опосредуемая акти- |
ват дег дрогеназного комплекса. Основным анти- |
||||||||
|
|
|
|
|
|
Вести |
|
|
|
вация NF-kB в гепатоцитах выполняет сущест- |
геном при ПБЦ (обнаруживается у 90% пациен- |
||||||||
венную физиологическую функцию по предупре- |
тов) выс упает дигидролипамид ацилтрансфераза |
||||||||
ждению |
спонтанного развития |
стеатогепатита |
(Е2-компонент пируват дегидрогеназного ком- |
||||||
ГЦК. Дополнительно эти факты позволяют пред- |
пл к а). Аутореактивные CD4+ и CD8+ Т-клетки |
||||||||
|
|
|
|
|
|
- |
обнаруживаются у пациентов с ПБЦ независимо |
||
положить, что NF-kB может представлять моле- |
|||||||||
кулярное звено, соединяющее воспалительные, |
от наличия или отсутствия антимитохондриаль- |
||||||||
защитные и |
метаболические |
реакции в печени, |
ных антител, а инфильтрация аутореактивными |
||||||
а также служить одним из клеточных факто- |
Т-клетками паренхимы и перидуктулярных про- |
||||||||
ров патогенетических механизмовМ, сопрягающих |
странств печени является важнейшей характери- |
||||||||
неалкогольный стеатогепатит и гепатоцеллюляр- |
стикой аутоиммунного статуса у больных ПБЦ. |
||||||||
ную карциному у человека. |
|
|
Одним из ключевых факторов патогенеза ПБЦ |
||||||
|
|
|
|
|
|
|
служит снижение популяции CD4+ CD25+ при- |
||
Заключение |
|
|
родных регуляторных Т-клеток. Холангиоциты, |
||||||
|
|
подвергающиеся апоптозу, фагоцитируются не |
|||||||
|
|
|
|
|
|
|
|||
При |
аутоиммунном гепатите повреждение |
только макрофагами, но и соседними холангио- |
|||||||
печени инициируют CD4+ Т-клетки, распознаю- |
цитами и становятся источником аутоантигенов, |
||||||||
щие аутоантигенные пептиды на поверхности |
представляемых аутофагами на своей мембране |
||||||||
гепатоцитов. |
Первоначально |
аутоантигенные |
в комплексе с молекулами HLA клеток класса I, |
||||||
пептиды |
интернализуются |
профессиональными |
что превращает их в объект атаки аутореактивны- |
||||||
антигенпрезентирующими клетками (макрофаги, |
ми цитотоксическими CD8+ Т-клетками. |
||||||||
дендритные клетки) по механизму рецепторопо- |
Антигенпрезентирующие клетки |
иннатной |
|||||||
средуемого эндоцитоза и проходят стадию процес- |
(врожденной) иммунной системы при ПБЦ про- |
||||||||
синга. Затем аутоантигенный эпитоп в комплексе |
дуцируют повышенные количества провоспали- |
||||||||
с молекулами МНС класса II презентируется |
тельных цитокинов. Повышенное содержание |
||||||||
некоммитированным (наивным) CD4+ Т-хелпер- |
IgM при ПБЦ отражает чрезмерную активацию |
||||||||
ным (Th0) клеткам. Активированные Th0-клетки |
макрофагов/дендритных клеток консервативным |
||||||||
дифференцируются в функциональные фенотипы |
бактериальным компонентом CpG-B, который |
||||||||
Th1 и Th2 при наличии в микроокружении IL-12 |
служит лигандом толл-подобного рецептора 9. |
||||||||
и IL-18 для Th1 и IL-4 для Th2-клеток. Th1-клет- |
Врожденные или приобретенные дефекты экс- |
||||||||
ки секретируют преимущественно IL-2 и IFN-γ и |
прессии MDR3/ABCB4 (кодирующего транс- |
||||||||
тем самым повышают экспрессию молекул HLA |
портер фосфолипидов на каналикулярной мем- |
||||||||
класса I на гепатоцитах (это увеличивает чувст- |
бране гепатоцитов), гена CFTR (кодирующего |
||||||||
вительность гепатоцитов по отношению к атакам |
Cl–-транспортер эпителиальных клеток печени, |
||||||||
11

3, 2009
тельность печени к LPS/TNF-индуцируемому апоптозу. Комбинированное выключение в эксперименте регуляторных субъединиц IKK1 и IKK2 в печеночной паренхиме сопровождается спонтанным развитием тяжелой холестатической болезни, обусловленной воспалительной деструкцией малых портальных желчных протоков. NF-kB может представлять молекулярное звено, соединяющее воспалительные, защитные и метаболические реакции в печени, а также служить одним из ключевых факторов патогенетических механизмов, сопрягающих неалкогольный стеатогепатит и гепатоцеллюлярную карциному у человека.
Список литературы |
|
|
|
|
|
|
|
11. Mix H., Weiler-Norman C., Thimme R. et al. Antigen- |
|||||||
1. Ивашкин В.Т. |
Механизмы иммунной толерантности и |
|
specific T cells in autoimmune hepatitis. |
Abstracts: |
|||||||||||
|
Monothematic |
Conference: Immune Mediated Liver |
|||||||||||||
патологии печени // Рос. журн. гастроэнтерол. гепа- |
|
||||||||||||||
|
Injury. – Hamburg, Germany, December 4–6, 2008. – |
||||||||||||||
тол. колопроктол. – 2009. – Т. 19, № 2. – С. 8–13. |
|
||||||||||||||
|
P. 45. |
|
|
|
|
||||||||||
2. Ивашкин В.Т. |
Основные понятия и положения фун- |
|
|
|
|
|
|||||||||
12. |
Monothematic |
Conference: Immune Mediated Liver |
|||||||||||||
даментальной |
иммунологии // |
Рос. журн. гастроэн- |
|||||||||||||
|
Injury. – Hamburg, Germany, December 4–6. – 2008. |
||||||||||||||
терол. гепатол. колопроктол. – 2008. – Т. 18, № 4. |
|
||||||||||||||
13. |
Pasparakis M. NF-kB: liver injury and cancer. Abstracts: |
||||||||||||||
– С. 4–13. |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
Monothematic Conference: Immune Mediated Liver Injury. |
||||||
3. Ивашкин В.Т., Буеверов А.О. |
Аутоиммунные заболе- |
|
|||||||||||||
|
– Hamburg, Germany, December 4–6, 2008. – P. 51. |
||||||||||||||
вания печени в практике клинициста. – М.: Изд. дом |
|
||||||||||||||
14. |
Salas J.T., |
Banales J.M., Sarvide S. et |
al. Ae2a,b |
||||||||||||
«М-Вести», 2001. – 102 с. |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
– deficient |
mice |
develop antimitochondrial |
antibodies |
|||||
4. Chuang Y.H., Ridgway W.M., UenoY., Gershwin M.E. |
|
||||||||||||||
|
and other features |
resembling primary biliary cirrhosis |
|||||||||||||
Animal models of primary biliary cirrhosis // Clin. Liver |
|
||||||||||||||
|
// Gastroenterology. – 2008. – Vol. 134, N 5. – P. |
||||||||||||||
Dis. – 2008. – Vol. 12, N 2. – P. 333–347. |
|
|
|
||||||||||||
|
|
|
1482–1493. |
|
|
|
|
||||||||
5. Fickert P., Wagner M., Marschall H.U. et al. 24-norUr- |
|
|
|
|
|
||||||||||
15. |
Schramm C. PSC pathogenesis. Abstracts: Monothematic |
||||||||||||||
sodeoxycholic acid is superior to ursodeoxycholic acid in |
|||||||||||||||
|
Conference: Immune Mediated Liver Injury. – Hamburg, |
||||||||||||||
the treatment of sclerosing |
cholangitis in Mdr2(Abcb4) |
|
|||||||||||||
|
Germany, December 4–6, 2008. – P. 50. |
|
|||||||||||||
Knockout mice // Gastroenterology. – 2006. – Vol. 130, |
|
|
|||||||||||||
16. |
Steinman L. A brief history of T(H)17, the first major |
||||||||||||||
N 2. – P. 465–481. |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
revision in the T(H)1/T(H)2 hypothesis of T cell – medi- |
|||||||
6. Gershwin M. The etiopathogenesis of primary |
biliary |
|
|||||||||||||
|
ated tissue damage // Nat. Med. – 2007. – Vol. 13. – |
||||||||||||||
|
|
|
|
|
- |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
cirrhosis. Abstracts: Monothematic Conference:ВестиImmune |
|
|
|
||||||||||||
Mediated Liver Injury. – Hamburg, Germany, December |
|
P. 139–145. |
|
|
|
|
|||||||||
17. |
Trauner M., Fickert P., Wagner M. MDR3 (ABCB4) |
||||||||||||||
4–6, 2008. – P. 47 |
|
|
М |
|
|||||||||||
|
|
|
|
defects: a paradigm for the genetics of adult cholestatic |
|||||||||||
|
|
|
|
|
|
|
|
||||||||
7. von Herrath M., Filippi C., Christen U. Viral infections |
|
||||||||||||||
|
syndromes // |
Semin. Liver Dis. – 2007. – Vol. 27, |
|||||||||||||
and autoimmunity. Abstracts: Monothematic Conference: |
|
||||||||||||||
|
N 1. – P. 77–98. |
|
|
||||||||||||
Immune Mediated Liver Injury. – Hamburg, Germany, |
|
|
|
||||||||||||
18. |
Ueno Y., Moritoki Y., Shimosegawa T., Gershwin M.E. |
||||||||||||||
December 4–6, 2008. – P. 42. |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
Primary biliary cirrhosis: what we know and we want to |
|||||||||
8. Longhi M.S., |
Hussain |
M.J., |
Bogdanos |
D.P. et al. |
|
||||||||||
|
know about human PBC and spontaneous PBC mouse |
||||||||||||||
Cytochrome P450IID6 |
– |
specific |
effector |
CD8 |
T-cell |
|
|||||||||
|
model // J. Gastroenterol. – 2007. – Vol. 42, N 3. |
||||||||||||||
immune responses mirror |
disease |
activity |
in autoim- |
|
|||||||||||
|
– P. 189–195. |
|
|
|
|||||||||||
mune hepatitis type 2 // Hepatology. – 2007. – Vol. |
|
|
|
|
|||||||||||
19. |
Weaver C.T., |
Harrington L.E., Morgan R.P. et al. |
|||||||||||||
46. – P. 472–484. |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
Th17: an effector CD4 T cells lineage with regulatory T |
|||||||
9. Longhi M.S., Hussain M.J., Mitry R.R. et al. Functional |
|
||||||||||||||
|
cells ties // Immunity. – 2006. – Vol. 24. – P. 677– |
||||||||||||||
study of CD4+CD25+ |
regulatory |
T cells |
in |
health |
|
||||||||||
|
678. |
|
|
|
|
||||||||||
and autoimmune hepatitis |
// |
J. |
Immunol. |
– |
2006. |
|
|
|
|
|
|||||
|
|
|
|
|
|
||||||||||
– Vol. 176. – P. 4484–4491.
10.Ma Y., Bogdanos D.P, Hussain M.J. et al. Polyclonal T cell responses to cytochrome P450IID6 are associated with disease activity in autoimmune hepatitis type 2 // Gastroenterology. – 2006. – Vol. 130. – P. 868–882.
12

3, 2009 |
Лекции и обзоры |
|
|
УДК 616.36-002.12-578.91
Современные подходы к лечению больных хроническим гепатитом В
С.Ф. Галимова, М.В. Маевская, В.Т. Ивашкин
(Клиника пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В.Х. Василенко Московской медицинской академии им. И.М. Сеченова)
Modern approaches to the treatment of patients with chronic hepatitis B
S.F.Galimova, М.V. Mayevskaya, V.Т. Ivashkin
Цель обзора. Представить современные реко- |
The aim of review. To present up-to-date referenc- |
мендации, позволяющие выбрать оптимальную |
es, that allows to choose the optimal mode of antiviral |
схему противовирусной терапии для больного хро- |
therapy for patient with chronic hepatitis B (CHB). |
ническим гепатитом В (ХГВ). |
Original positions. Chronic HBV-infection repre- |
Основные положения. Хроническая HBV-инфек- |
sents a major epidemiologic and economic problem |
ция представляет большую эпидемиологическую и |
all over the world. Liver cirrhosis (LC) and hepatocel- |
экономическую проблему во всем мире. Циррозпече- |
lular carcinoma (HCC) related to HBV infection are |
ни (ЦП) и гепатоцеллюлярная карцинома (ГЦК) HBV |
the causes for over 1 million deaths and 5–10% of |
этиологии служат причинами более 1 млн смертей и |
transplantations of liver per year. The comprehension |
5–10% трансплантаций печени ежегодно. Понимание |
of the role of viral load in development of LC and HCC |
Вести |
|
роли вирусной нагрузки в развитии ЦП и ГЦК появ- |
and introduction to the pharmaceutical market of new |
ление на фармацевтическом рынке новых препара- |
agents allow to improve guidelines on management of |
тов позволило усовершенствовать рекомендации по |
patients with chronic HBV-infection. The main criterion |
ведению больных с хронической HBV-инфекцией. |
of efficacy of antiviral therapy (AVT) – the level of viral |
Главный критерий эффективности противовирус- |
load. Monitoring of HBV DNA on the 12, 24, 48-th weeks |
ной терапии (ПВТ) – величина вирусной нагрузки. |
of treatment enables to predict its efficacy and risk of |
Мониторирование HBV DNA на 12, 24, -48 й неде- |
development of resistance to nucleoside/nucleotides |
лях лечения дает возможность составить прогноз его |
analogues. |
эффективности и определить рискМразвития рези- |
It is recommended to consider patients with CHB with |
стентности к аналогам нуклеозидов/нуклеотидов. |
viral load of over 2000 МЕ/ml (≈10000 copies/ml) and/ |
В качестве кандидатов для проведения ПВТ реко- |
or elevation of alanineaminotransferase (ALT) activity, |
мендуется рассматривать больных ХГВ с вирусной |
with signs of moderate to severe inflammatory-necrotic |
нагрузкой более 2000 МЕ/мл (≈10 000 копий/мл) |
changes and/or liver fibrosis as candidates for AVT. |
и/или повышением активности аланинаминотранс- |
Patients with LC are considered as candidates for |
феразы (АлАТ), с признаками умеренных или тяже- |
AVT even at normal ALT levels irrespective of level of |
лых воспалительно-некротических изменений и/или |
viral load. For decompensated LC patients nucleoside/ |
фиброзом печени. Пациенты с ЦП рассматриваются |
nucleotides analogues are the drugs of choice. New |
вкачествекандидатовдляПВТдажепринормальных |
analogues nucleoside/nucleotides (telbivudine, ente- |
значениях АлАТ независимо от величины вирусной |
cavir, tenofovir) have direct antiviral action and good |
нагрузки. Для больных с декомпенсированным ЦП |
tolerability at long application. |
препаратами выбора служат аналоги нуклеозидов/ |
Conclusion. Modern international references on |
нуклеотидов. Новые аналоги нуклеозидов/нуклео- |
management of patients with HBV-infection allows to |
тидов (телбивудин, энтекавир, тенофовир) облада- |
increase efficacy of treatment by of rational application |
ют прямым противовирусным действием и хорошей |
of antiviral agents, to improve survival rate, to reduce |
переносимостью при длительном применении. |
mortality and risk of LC and HCC development, to opti- |
Заключение. Современные международные |
mize treatment cost. |
рекомендации по ведению больных с HBV-инфек- |
Key words: chronic hepatitis B, antiviral therapy, |
цией позволяют повысить эффективность лечения |
viral load, nucleoside/nucleotides analogues. |
посредством рационального применения проти- |
|
вовирусных препаратов, улучшить выживаемость, |
|
уменьшить летальность и риск развития ЦП и ГЦК, |
|
оптимизировать затраты на лечение. |
|
Ключевые слова: хронический гепатит В, про- |
|
тивовирусная терапия, вирусная нагрузка, аналоги |
|
нуклеозидов/нуклеотидов. |
|
13

Лекции и обзоры |
|
3, 2009 |
|
|
|
момента открытия Б. Бламбергом «авст- |
и доступность противовирусных препаратов на |
|
ралийского антигена» прошло 44 года [1]. |
фармацевтическом рынке страны. |
|
СЗа этот отрезок времени определена рас- |
Больные, не соответствующие указанным кри- |
|
пространенность HBV-инфекции в мире, изучены |
териям, объединены в специальные группы: |
|
механизмы взаимодействия вируса гепатита В и |
1) иммунотолерантные пациенты: в боль- |
|
организма человека и, что наиболее важно, синте- |
шинстве случаев это лица в возрасте до 30 лет, с |
|
зирован широкий спектр препаратов, обладающих |
высокой вирусной нагрузкой (свыше 107 МЕ/мл) |
|
прямым противовирусным действием в отношении |
и стойко нормальными значениями аминотранс- |
|
HBV. Вместе с тем лечение больных хроническим |
фераз, без признаков активности гепатита и ука- |
|
гепатитом В (ХГВ) по-прежнему остается слож- |
заний на ГЦК и ЦП в семейном анамнезе. Такие |
|
ной клинической задачей. В свете новых пред- |
пациенты не нуждаются в неотложном проведе- |
|
ставлений о роли вирусной нагрузки в развитии |
нии биопсии печени и противовирусном лечении, |
|
цирроза печени (ЦП) и гепатоцеллюлярной кар- |
им показано динамическое наблюдение; |
|
циномы (ГЦК) [3, 8, 21], оценке эффективности |
2) пациентам с легким течением ХГВ с актив- |
|
лечения, а также с появлением на фармацевти- |
ностью АлАТ, менее чем в 2 раза превышающей |
|
ческом рынке новых противовирусных препара- |
верхний лимит нормы, и умеренно выраженными |
|
тов стала очевидной необходимость пересмотра |
гистологическими изменениями в печени (менее |
|
разработанных ранее рекомендаций по ведению |
А2 и F2 по шкале METAVIR) проведение про- |
|
пациентов с хронической HBV-инфекцией. Так, |
тивовирусной терапии не обязательно. Показано |
|
за последние годы было опубликовано несколько |
динамическое наблюдение; |
|
международных документов, созданных с уча- |
3) больные компенсированным ЦП и с опре- |
|
стием практикующих врачей, экспертов и дру- |
деляемым уровнем HBV DNA могут рассматри- |
|
гих сотрудников здравоохранения, занимающихся |
ваться в качестве кандидатов для противовирус- |
|
данной проблемой: рекомендации Американской |
ной терапии даже в случае нормальных значений |
|
ассоциации по изучению заболеваний печени |
АлАТ, независимо от величины вирусной нагруз- |
|
(AASLD, 2007) [15], рекомендации Европейской |
ки (менее 2000 МЕ/мл или ≈10 000 копий/мл); |
|
ассоциации по изучению заболеваний печени |
4) пац ентам с декомпенсированным ЦП |
|
(EASL, 2008) [4], рекомендации Международного |
про ивов русную терапию необходимо начинать |
|
семинара по лечению больных хроническим гепа- |
в кра чайшие сроки. Данная категория лиц осо- |
|
титом В аналогами нуклеозидов – «дорожная |
б нно остро нуждается в профилактике развития |
|
- |
р зистентности к аналогам нуклеозидов, а также |
|
карта» (2007) и др. [10]. Учитывая изменения |
||
в подходах к тактике ведения таких пациентов, |
в быстрой выраженной супрессии репликации |
|
наиболее подробными и обоснованными представВестиHBV, поскольку именно эти факторы ассоции- |
||
ляются рекомендации EASL. Ниже будут затро- |
руются с клиническим улучшением. При отсут- |
|
нуты вопросы выбора противовируснойМтерапии |
ствии эффекта от лечения у больных с тяжелым |
|
(ПВТ) и тактики ведения больных хроническим |
декомпенсированным ЦП рассматривается вопрос |
|
гепатитом В. |
о трансплантации печени. |
|
Показания к противовирусной терапии
Обсуждая проблему ПВТ, первоначально необходимо ответить на вопрос: нуждается ли пациент в лечении? В рекомендациях EASL показания к ПВТ для пациентов с HBeAg-позитивным и HBeAg-негативным ХГВ учитывают три фактора – вирусную нагрузку, активность аланинаминотрансферазы (АлАТ), гистологическую активность и/или степень фиброза печени [4].
В качестве кандидатов для проведения ПВТ рекомендуется рассматривать больных ХГВ с вирусной нагрузкой более 2000 МЕ/мл (≈10 000 копий/мл) и/или повышением активности АлАТ, с признаками умеренных или тяжелых воспали- тельно-некротических изменений и/или фиброзом печени (например, А2 и F2 по шкале METAVIR) согласно результатам биопсии печени или неинвазивных методов исследования. Также важно учитывать возраст, сопутствующие заболевания
Цели лечения
Цели лечения хронического гепатита В заключаются в улучшении качества жизни и выживаемости пациентов посредством предотвращения прогрессирования в цирроз, декомпенсации цирроза, предупреждении развития ГЦК и снижении летальности. В клинической практике полная эрадикация HBV – задача трудновыполнимая ввиду способности вируса к существованию в форме сверхскрученной ковалентно замкнутой ДНК (сссDNA) в ядре гепатоцитов. Принимая во внимание этот факт, достижение поставленных целей возможно только при сочетании двух условий – стойкого подавления репликации HBV до уровня, не превышающего нижний лимит опреде-
ления HBV DNA методом полимеразной цепной реакции (ПЦР), и улучшения гистологических изменений в печени. Наименьшую концентрацию HBV DNA, которая составляет 10–15 МЕ/мл (≈50–75 копий/мл), можно измерить методом
14

3, 2009
ПЦР в режиме реального времени (real-time |
Ответ на интерферонотерапию |
|||
PCR). Отличительными чертами данного мето- |
• Первичный ответ оценивают через 12 нед |
|||
да в сравнении с классической ПЦР служит |
||||
отсутствие стадии электрофореза, что позволяет |
от начала лечения. Об отсутствии первично- |
|||
минимизировать риск контаминации продуктами |
го ответа свидетельствует снижение величины |
|||
ПЦР и таким образом резко уменьшить число |
вирусной |
нагрузки менее чем на 1 lg МЕ/мл |
||
ложноположительных результатов. При отсутст- |
(10 МЕ/мл или ≈50 копий/мл) по сравнению с |
|||
вии возможности исследования вирусной нагруз- |
исходным значением. |
|
||
ки указанным методом эксперты рекомендуют |
• Вирусологический |
ответ определяют на |
||
пользоваться другими наиболее чувствительными |
24-йнеделетерапии как снижение вирусной нагруз- |
|||
доступными методами. |
ки до величины, не превышающей 2000 МЕ/мл. |
|||
В идеале для HBeAg-позитивных и для HBeAg- |
• Под серологическим ответом подразумева- |
|||
негативных пациентов конечная цель лечения – |
ют НBeAg-сероконверсию у HBeAg-позитивных |
|||
стойкое исчезновение HBsAg и/или HBsAg- |
пациентов. |
|
||
сероконверсия, что приводит к полной и стойкой |
Ответ на терапию аналогами нуклеозидов/ |
|||
ремиссии заболевания и улучшает отдаленный |
||||
нуклеотидов |
|
|||
прогноз. Для HBeAg-позитивных пациентов бла- |
|
|||
|
|
|
||
гоприятным прогностическим фактором служит |
• Под отсутствием первичного ответа пони- |
|||
стойкая HВeAg-сероконверсия. |
мают снижение вирусной нагрузки менее чем на |
|||
В последние десятилетия впервые была про- |
1 lg МЕ/мл (10 МЕ/мл или ≈50 копий/мл) по |
|||
демонстрирована роль вирусной нагрузки в про- |
сравнению с исходной величиной через 12 нед от |
|||
грессировании хронического гепатита В в цирроз |
начала лечения. |
|
||
и развитии ГЦК [3, 21]. Так, в исследовани- |
• Вирусологическим ответом принято считать |
|||
ях RЕVEAL-HBV и других крупномасштабных |
отрицательный результат HBV DNA, полученный |
|||
проспективных исследованиях приведены дока- |
методом ПЦР в режиме реального времени на |
|||
зательства прямой корреляционной зависимо- |
48-й неделе лечения. |
|
||
сти между величиной вирусной нагрузки свыше |
• Час |
чный вирусологический ответ харак- |
||
2000 МЕ/мл (≈10 000 копий/мл) и риском раз- |
теризуе ся сн жением HBV DNA более чем на |
|||
вития ЦП и ГЦК независимо от присутствия |
1 lg МЕ/мл, но выявляемой методом ПЦР в |
|||
HBeAg и активности АлАТ. Более того, указан- |
р жиме реального времени. Для пациентов, полу- |
|||
ная величина вирусной нагрузки представля |
чающих лечение ламивудином и телбивудином, |
|||
собой фактор риска развития ГЦК у пациентов |
частичный вирусологический ответ оценивают на |
|||
с ХГВ без признаков цирроза. Также установВести- 24-й неделе терапии, а при приеме энтекавира, |
||||
- |
адефовира или тенофовира (высокий генетиче- |
|||
лено, что стойкое подавление репликации HBV |
||||
уменьшает риск формированияМрезистентности к |
ский барьер) – на 48-й неделе от момента начала |
|||
аналогам нуклеозидов и повышает вероятность |
лечения. Частичный вирусологический ответ слу- |
|||
HBeAg-сероконверсии, исчезновения HBsAg как |
жит аргументом в пользу пересмотра ПВТ. |
|||
у HBeAg-позитивных, так и у HBeAg-негативных |
• Вирусологический |
прорыв – увеличение |
||
пациентов. Приведенные факты стали предпо- |
величины HBV DNA более чем на 1 lg МЕ/мл |
|||
сылкой для заключения экспертов о ключевой |
в сравнении с наименьшим значением данного |
|||
роли динамического количественного исследова- |
показателя за весь период лечения. В большин- |
|||
ния HBV DNA в составлении прогноза течения |
стве случаев за вирусологическим прорывом сле- |
|||
хронической HBV-инфекции и оценке эффектив- |
дует биохимический прорыв (повышение актив- |
|||
ности лечения [4]. В соответствии с этим новый |
ности АлАТ). Причинами прорыва могут быть |
|||
подход в наблюдении за больными ХГВ заклю- |
низкая приверженность пациента к лечению и |
|||
чается в мониторировании вирусной нагрузки |
развитие резистентности к препарату. |
|||
на определенных этапах лечения, что позволяет |
• Резистентность HBV к аналогам нуклео- |
|||
прогнозировать его эффективность, риск разви- |
зидов характеризуется |
появлением мутантных |
||
тия резистентности в случае применения аналогов |
штаммов вируса, обладающих низкой чувстви- |
|||
нуклеозидов и своевременно вносить изменения в |
тельностью к применяемому аналогу нуклеози- |
|||
схему ПВТ. |
дов/нуклеотидов. Резистентность служит основ- |
|||
|
ной причиной отсутствия первичного ответа и |
|||
Оценка эффективности лечения |
вирусологического прорыва. |
|||
|
|
|
||
Принимая во внимание изложенный выше |
Современные схемы |
|||
принципиально новый подход к оценке эффек- |
||||
противовирусной терапии |
||||
тивности лечения, выделяют следующие вариан- |
||||
|
|
|
||
ты ответа на противовирусную терапию [4]. |
Препараты, применяемые в лечении хронической |
|||
|
HBV-инфекции, можно объединить в две группы. |
|||
15

Лекции и обзоры |
|
|
|
|
3, 2009 |
||
|
|
|
|
||||
А. Препараты интерферона α (стандартный и |
У HBeAg-негативных пациентов вирусологи- |
||||||
пегилированный интерферон) |
|
ческий ответ отмечен в 63, 72, 51, 90, 88 и 91% |
|||||
Б. Аналоги нуклеозидов/нуклеотидов: |
через 1 год терапии ПЕГ-ИФН-α2а, ламивуди- |
||||||
1) L-нуклеозиды: ламивудин, |
телбивудин, |
ном, |
адефовиром, энтекавиром, телбивудином |
||||
эмтрицитабин; |
|
|
|
и тенофовиром соответственно. Исчезновение |
|||
2) аналоги деоксигуанозина: энтекавир; |
HBsAg после 1 года лечения зарегистрировано у |
||||||
3) ациклические фосфонаты нуклеозидов: аде- |
3% пациентов, принимавших ПЕГ-ИФН-α2а и ни |
||||||
фовир, тенофовир. |
|
у кого из больных на фоне приема ламивудина, |
|||||
Из аналогов нуклеозидов/нуклеотидов в |
адефовира, энтекавира, телбивудина и тенофови- |
||||||
России зарегистрированы ламивудин (Зеффикс), |
ра [6, 13, 16, 19]. |
||||||
телбивудин (Себиво), энтекавир (Бараклюд). |
Таким образом, преимущества интерфероно- |
||||||
Адефовир (Гепсера) и новый аналог нуклеозидов |
терапии перед аналогами нуклеозидов/нуклеоти- |
||||||
тенофовир (Вирид) на российском фармацевтиче- |
дов – отсутствие риска развития резистентности, |
||||||
ском рынке не зарегистрированы. |
|
возможность достижения стойкого вирусологи- |
|||||
Эффективность всех препаратов оценивалась в |
ческого ответа и исчезновение HBsAg, недос- |
||||||
рандомизированных контролированных исследова- |
татки – высокая частота побочных эффектов и |
||||||
ниях. В настоящее время опубликованы результаты |
подкожный путь введения. Декомпенсированный |
||||||
продолжительного лечения (3–5 лет) ламивудином, |
цирроз печени, аутоиммунные заболевания, тяже- |
||||||
адефовиром, энтекавиром, телбивудином и тенофо- |
лая депрессия, психоз – основные противопо- |
||||||
виром. Однако, несмотря на большое количество |
казания к терапии препаратами интерферона α |
||||||
клинических исследований, сравнение результатов |
(табл. 1) [4]. |
||||||
длительной терапии данными препаратами вызы- |
Говоря об аналогах нуклеозидов/нуклеотидов, |
||||||
вает трудности ввиду применения разных методов |
справедливо отметить, в первую очередь, риск |
||||||
количественного определения HBV DNA. |
развития резистентности, который ассоцииру- |
||||||
У HBeAg-позитивных пациентов вирусоло- |
ется с повышением активности трансаминаз и |
||||||
|
|
|
Вести |
||||
гический ответ в виде отрицательного резуль- |
снижен ем эффективности лечения. Для удоб- |
||||||
тата ПЦР через 1 год лечения пегилированным |
ства обозначен я степени риска резистентности |
||||||
интерфероном α (ПЕГ-ИФН-α2а), ламивуди- |
упо ребляе ся термин «генетический барьер». |
||||||
ном, адефовиром, энтекавиром, |
телбивудином |
Ч м выше генетический барьер, тем ниже риск |
|||||
и тенофовиром составил 24, 36–39, 21, 67, |
развития мутаций HBV и соответственно вероят- |
||||||
|
|
|
- |
ность резистентности. К препаратам с высоким |
|||
60 и 74% соответственно. HBeAg-сероконверсия |
|||||||
наблюдалась у 30% пациентов на фоне интер- |
генетическим барьером, обладающим высокой |
||||||
феронотерапии и у 20% больных, леченных |
эффективностью против HBV, относят энтека- |
||||||
аналогами нуклеозидов/нуклеотидов. По мере |
вир и тенофовир [2, 18]. Указанные свойства |
||||||
увеличения продолжительностиМлечения частота |
позволили экспертам Европейской ассоциации по |
||||||
HBeAg-сероконверсии возрастала, но вместе с |
изучению заболеваний печени рекомендовать дан- |
||||||
тем отмечался и рост резистентности к аналогам |
ные препараты в качестве средств первой линии в |
||||||
нуклеозидов/нуклеотидов. Исчезновение HBsAg |
лечении хронической HBV-инфекции [4]. |
||||||
отмечено у 3–4% пациентов через 1 год терапии |
Адефовир обладает меньшей эффективностью |
||||||
ПЕГ-интерфероном и у 3% больных, получавших |
и более низким генетическим барьером в сравне- |
||||||
лечение тенофовиром. На фоне приема ламивуди- |
нии с тенофовиром [12]. |
||||||
на, адефовира, энтекавира и телбивудина HBsAg |
Телбивудин – высокоэффективный ингибитор |
||||||
сохранялся на протяжении всего периода лечения |
HBV, по противовирусной активности значитель- |
||||||
[2, 7, 9, 11, 12, 17]. |
|
но превосходит ламивудин. Его эффективность |
|||||
|
|
|
|
|
|
|
Таблица 1 |
|
|
Основные преимущества и недостатки |
|||||
|
препаратов ПЕГ-интерферона α и аналогов нуклеозидов/нуклеотидов |
||||||
Показатель |
|
Пегилированный интерферон α |
|
|
Аналоги нуклеозидов/нуклеотидов |
||
|
|
|
|
|
|
||
Преимущества |
|
Определенная продолжительность |
|
|
Выраженное противовирусное действие |
||
|
|
лечения |
|
|
|
|
|
|
|
Отсутствие резистентности |
|
|
Хорошая переносимость |
||
|
|
Более высокая частота HBe- |
|
|
Пероральный путь введения |
||
|
|
и HBs-сероконверсии |
|
|
|
|
|
Недостатки |
|
Умеренная противовирусная активность |
|
Неопределенная длительность лечения |
|||
|
|
Плохая переносимость |
|
|
Риск резистентности |
||
|
|
Подкожный путь введения |
|
|
Более низкая частота HBe- |
||
|
|
|
|
и HBs-сероконверсии |
|||
|
|
|
|
|
|
||
16

3, 2009 |
|
|
|
|
|
Лекции и обзоры |
|||
|
|
|
|
|
|
|
|
|
|
была доказана в исследовании GLOBE – самом |
Как показали клинические исследования, ком- |
||||||||
крупном клиническом исследовании, продемонст- |
бинированная терапия ПЕГ-ИФН-α и ламивуди- |
||||||||
рировавшем роль количественного определения |
ном не имеет преимуществ перед монотерапией |
||||||||
HBV DNA на 24-й неделе терапии как фак- |
ПЕГ-ИФН-α. В связи с недостаточной инфор- |
||||||||
тора, влияющего на отдаленные последствия |
мацией об эффективности и безопасности схем |
||||||||
лечения. Так, вирусологический ответ на 24-й |
комбинированной терапии ПЕГ-ИФН-α с други- |
||||||||
неделе терапии телбивудином позволяет прогно- |
ми аналогами нуклеозидов/нуклеотидов данные |
||||||||
зировать эффективность лечения через 2 года. |
виды лечения пока не рекомендуются. |
|
|||||||
Установлено, что исходный уровень HBV DNA |
Аналоги нуклеозидов/нуклеотидов: опреде- |
||||||||
менее 9 lg копий/мл и активность АлАТ ≥2N у |
ленная продолжительность лечения в случае при- |
||||||||
HBeAg-позитивных больных хроническим гепати- |
менения аналогов нуклеозидов/нуклеотидов при- |
||||||||
том В и уровень HBV DNA менее 7 lg копий/мл у |
менима только к пациентам с HBeAg-позитивным |
||||||||
HBeAg-негативных пациентов до начала лечения |
гепатитом В, у которых в процессе противови- |
||||||||
телбивудином ассоциируются с высокой частотой |
русного лечения произошла HBeAg-сероконвер- |
||||||||
вирусологического ответа в виде отрицательного |
сия. К факторам, позволяющим прогнозировать |
||||||||
результата ПЦР через 2 года терапии и низкой |
HBeAg-сероконверсию, относят высокую актив- |
||||||||
частотой резистентности. Частота развития рези- |
ность АлАТ (более 3 N), показатель вирусной |
||||||||
стентности к телбивудину при отрицательном |
нагрузки менее 2·106 МЕ/мл (≈107 копий/мл) |
||||||||
результате ПЦР на 24-й неделе лечения у пациен- |
или 6,3 lg МЕ/мл и высокую гистологическую |
||||||||
тов с HBeAg-позитивным гепатитом В составила |
активность до начала лечения. После HBeAg- |
||||||||
4%, с HBeAg-негативным – 2%. То есть назна- |
сероконверсии |
рекомендуется продлить |
лечение |
||||||
чение телбивудина оптимально для пациентов с |
на период от 6 до 12 мес, предпочтительно на |
||||||||
HBeAg-позитивным и HBeAg-негативным гепати- |
12 мес. При соблюдении данной тактики стойкий |
||||||||
том В с полным ответом на 24-й неделе лечения. |
ответ на лечение можно ожидать у 80% боль- |
||||||||
Причиной развития резистентности к препарату |
ных. |
|
|
|
|
|
|||
|
|
Вести |
|
|
|
||||
в 80% случаев был частичный вирусологический |
Отсутств е у пациента на момент начала лече- |
||||||||
ответ на 24-й неделе терапии. Важные преиму- |
ния фак оров, способствующих HBeAg-серокон- |
||||||||
щества телбивудина – безопасность и хорошая |
вер ии, не позволяет прогнозировать продолжи- |
||||||||
переносимость при длительном приеме, прогнози- |
льно |
ь противовирусной терапии. |
|
|
|||||
руемая эффективность [12]. |
- |
Лечение аналогами нуклеозидов/нуклеоти- |
|||||||
|
|
||||||||
Ламивудин также обладает противовирусным |
дов неопределенной длительности |
|
|||||||
действием в отношении HBV, однако моноте- |
|
||||||||
|
|
|
|
|
|
||||
рапия характеризуется очень высокой частотой |
Помимо пациентов с высокой ожидаемой |
||||||||
развития резистентности [14]. |
|
эффективностью лечения, существует весьма |
|||||||
В повседневной практике трудностиМтерапии |
большая группа больных с HBeAg-позитивным |
||||||||
связаны с выбором адекватной схемы лечения и |
и HBeAg-негативным ХГВ, ЦП, не имеющих |
||||||||
определением ее длительности. С целью облег- |
факторов благоприятного |
ответа |
на |
лечение |
|||||
чения решения этой задачи предлагаются две |
(N≤АлАТ<3 N, HBV DNA>2·106 |
МЕ/мл или |
|||||||
стратегии ведения больных: первая предусмат- |
≈107 копий/мл). Именно эти категории паци- |
||||||||
ривает интерферонотерапию или терапию анало- |
ентов представляют наибольшую проблему для |
||||||||
гами нуклеозидов/нуклеотидов с определенной |
клиницистов с точки зрения выбора схемы ПВТ |
||||||||
продолжительностью лечения, вторая – лечение |
и решения вопроса о ее прекращении. Учитывая |
||||||||
аналогами нуклеозидов/нуклеотидов неуточнен- |
неопределенность длительности лечения (годы) |
||||||||
ной длительности. |
|
таких пациентов, с целью минимизации риска |
|||||||
Терапия препаратами пегилированного |
развития резистентности к назначаемым средст- |
||||||||
вам рекомендуется отдавать предпочтение препа- |
|||||||||
интерферона α или аналогами нуклеози- |
|||||||||
ратам с высоким генетическим барьером – тено- |
|||||||||
дов/нуклеотидов с четко определенной |
|||||||||
фовиру |
или |
энтекавиру. |
Однако |
отдаленные |
|||||
продолжительностью лечения |
|
||||||||
|
результаты (5–10 лет) по эффективности и |
||||||||
|
|
|
|||||||
Пегилированный интерферон α: 48-недель- |
безопасности этих препаратов пока не известны. |
||||||||
ный курс рекомендуется преимущественно для |
Особый акцент делается на необходимости под- |
||||||||
HBeAg-позитивных, реже для HBeAg-негативных |
держания на фоне лечения супрессии HBV DNA |
||||||||
больных, имеющих факторы высокой ожидаемой |
ниже концентрации, определяемой методом ПЦР |
||||||||
эффективности лечения. К их числу относят |
в режиме реального времени. |
|
|
||||||
высокую активность АлАТ (более 3 N), показа- |
Эффективность схем комбинированной тера- |
||||||||
тель вирусной нагрузки HBV DNA менее 2·106 |
пии энтекавиром и телбивудином, энтекавиром и |
||||||||
МЕ/мл (≈107 копий/мл) или 6,3 lg МЕ/мл и |
тенофовиром, а также других аналогов нуклеози- |
||||||||
высокий индекс гистологической активности на |
дов/нуклеотидов пока не определена. |
|
|||||||
момент начала лечения. |
|
|
|
|
|
|
|
||
17

Лекции и обзоры |
|
|
|
3, 2009 |
|
|
|||
Тактика ведения больных |
Результаты безопасности длительной комбиниро- |
|||
при неэффективности лечения |
ванной терапии энтекавиром и тенофовиром пока |
|||
|
неизвестны. |
|
|
|
Очень важно разграничивать отсутствие пер- |
Вирусологический прорыв – увеличение вели- |
|||
вичного ответа (снижение вирусной нагрузки |
чины HBV DNA более чем на 1 lg МЕ/мл в |
|||
менее чем на 1 lg на 12-й неделе лечения), час- |
сравнении с наименьшим значением данного |
|||
тичный вирусологический ответ и вирусологиче- |
показателя за весь период лечения. У пациентов |
|||
ский прорыв [20]. |
с хорошей приверженностью к лечению вирусо- |
|||
Отсутствие первичного ответа чаще встре- |
логический прорыв обусловлен развитием рези- |
|||
чается на фоне лечения адефовиром (10–20%) |
стентности. Причинами последней могут быть |
|||
и служит показанием для замены препарата на |
мутации HBV, возникшие в результате ранее |
|||
тенофовир или энтекавир. При применении лами- |
проводившейся терапии аналогами нуклеозидов/ |
|||
вудина, телбивудина, энтекавира или тенофовира |
нуклеотидов, исходно высокая вирусная нагрузка |
|||
отсутствие первичного ответа встречается реже |
у нелеченных пациентов, медленные темпы сни- |
|||
и, в первую очередь, требует уточнения привер- |
жения HBV DNA и частичный вирусологический |
|||
женности больного к лечению. В случае привер- |
ответ на фоне терапии (рис. 1). Как показыва- |
|||
женности рекомендуется исключить возможность |
ют клинические исследования, мониторирование |
|||
появления мутантных штаммов HBV, резистент- |
HBV DNA способствует раннему обнаружению |
|||
ных к конкретному препарату. При подтвержде- |
резистентности – еще до развития вирусологи- |
|||
нии факта резистентности возможно изменение |
ческого прорыва (повышение активности АлАТ) |
|||
схемы терапии на препарат, эффективный против |
и позволяет своевременно внести изменения в |
|||
выявленных мутантных штаммов HBV. |
схему лечения. |
|
|
|
Частичный вирусологический ответ возможен |
При обнаружении резистентности рекомендуе- |
|||
при применении любого из аналогов нуклеози- |
мая стратегия лечения заключается в добавлении |
|||
дов/нуклеотидов и также требует уточнения при- |
второго препарата, обладающего высокой эффек- |
|||
верженности пациента к лечению. При частичном |
тивностью |
не |
имеющего перекрестной рези- |
|
вирусологическом ответе на 24-й неделе монотера- |
стен нос |
(табл. |
2). Безопасность некоторых |
|
пии ламивудином, адефовиром или телбивудином |
комбинац й препаратов пока неизвестна. |
|||
рекомендованы две тактики дальнейшего веде- |
Резис ентность к ламивудину: рекомендуется |
|||
ния: первая – замена на энтекавир или тенофо- |
добавить тенофовир или адефовир. |
|||
вир, вторая – добавление к лечению препарата, |
Резистентность к адефовиру: целесообразно |
|||
не имеющего с ним перекрестной резистентности. |
перейти на тенофовир (при его наличии) и доба- |
|||
Вести |
|
|
||
Например, при отсутствии перекрестной рези- |
вить второй препарат без перекрестной резистент- |
|||
- |
ности. При выявлении мутации N236T добавить |
|||
стентности можно добавить тенофовир к ламиву- |
||||
дину или телбивудину либо добавитьМэнтекавир |
ламивудин или телбивудин, или энтекавир либо |
|||
к адефовиру. Частичный вирусологический ответ |
перейти на комбинированную терапию тенофовир |
|||
на 48-й неделе терапии препаратами с высоким |
+ эмтрицитабин (в одной таблетке). При обна- |
|||
генетическим барьером (энтекавир, тенофовир), |
ружении мутации А181Т/V добавить энтекавир |
|||
по мнению некоторых экспертов, служит поводом |
(безопасность схемы тенофовир + энтекавир |
|||
для добавления второго препарата во избежание |
неизвестна) или перейти на комбинированную |
|||
развития резистентности в более поздние сроки. |
терапию тенофовиром и эмтрицитабином. |
|||
% |
67 |
70 |
|
1 |
год |
|
|
70 |
|
|
2 |
года |
|
|
|
|
|
|
|
|
|||
|
|
|
|
3 |
года |
|
|
60 |
|
|
|
4 |
года |
|
|
|
49 |
|
|
5 |
лет |
|
|
50 |
|
|
|
|
|
|
|
40 |
38 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
29 |
|
|
|
|
30 |
24 |
|
|
|
|
22 |
|
|
|
18 |
|
|
|
|
|
|
|
|
|
|
|
|
|
20 |
|
11 |
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
3 |
0,2 |
0,5 1,2 1,2 |
1,2 |
4 |
0 |
|
|
0 |
|
||||
0 |
Ламивудин |
Адефовир |
Энтекавир |
|
Телбивудин |
Тенофовир |
|
|
|
||||||
Рис. 1. Частота резистентности на фоне лечения аналогами нуклеозидов/нуклеотидов у пациентов, ранее не получавших противовирусное лечение
18
|
3, 2009 |
|
|
|
|
|
Лекции и обзоры |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 2 |
|
|
|
|
Наиболее частые мутации HBV, ответственные |
|
|
|
|
|
|
||||
|
за перекрестную резистентность к аналогам нуклеозидов/нуклеотидов [21] |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Мутации HBV |
|
|
|
Степень чувствительности |
|
|
|
|
|
||
|
|
Ламивудин |
Телбивудин |
Энтекавир |
Адефовир |
|
Тенофовир |
|
||||
|
|
|
|
|
||||||||
«Дикий тип» |
|
|
S |
S |
S |
S |
|
|
S |
|
|
|
M204I |
|
|
|
R |
R |
I/R |
S |
|
|
S |
|
|
L180M+M204I |
|
|
R |
R |
I |
S |
|
|
S |
|
|
|
A181T/V |
|
|
|
I |
S |
S |
R |
|
|
S |
|
|
N236T |
|
|
|
S |
S |
S |
R |
|
|
I |
|
|
L180M+M204V/I±I169T±V173L±M250V |
|
R |
R |
R |
S |
|
|
S |
|
|
||
L180M±M204V/I±T184G±S202I/G |
|
R |
R |
R |
S |
|
|
S |
|
|
||
|
|
|
|
|
|
|
|
|||||
Примечание. S – чувствительный препарат, I – промежуточная/сниженная чувствительность, R – резистентный. |
|
|
||||||||||
Резистентность к телбивудину: добавить тено- |
и определение активности АлАТ, |
|
через |
12 и |
|
|||||||
фовир или адефовир, если первый еще не заре- |
24 нед – количественное исследование |
HBV |
|
|||||||||
гистрирован. Безопасность данной комбинации |
DNA. Пациентам с HBeAg-позитивным гепати- |
|
||||||||||
препаратов при длительном применении не уста- |
том В показано исследование HBeAg, анти-HBe |
|
||||||||||
новлена. |
|
|
|
|
на 24-й, 48-й неделях лечения и через 24 нед |
|
||||||
Резистентность к энтекавиру: добавить тено- |
после его отмены. После обнаружения HBeAg- |
|
||||||||||
фовир, однако безопасность такого сочетания |
сероконверсии на фоне терапии ПЕГ-ИФН-α или |
|
||||||||||
препаратов неизвестна. |
|
|
|
аналогами нуклеозидов/нуклеотидов рекоменду- |
|
|||||||
Резистентность к тенофовиру: в литературе |
ется длительное дальнейшее наблюдение ввиду |
|
||||||||||
пока не описана. При ее обнаружении рекоменду- |
возможности HBe-серореверсии или HBeAg-нега- |
|
||||||||||
|
|
|
Вести |
|
|
|
|
|
|
|||
ется гено- и фенотипирование в экспертной лабора- |
тивного вар анта гепатита В. Если HBeAg- |
|
||||||||||
тории для выявления профиля перекрестной рези- |
ероконверс |
я сопровождается |
отрицательным |
|
||||||||
стентности. Теоретически рекомендуется добавить |
р зуль а ом ПЦР в режиме реального времени, |
|
||||||||||
ламивудин или телбивудин, или эмтрицитабин. |
то рекомендуется исследование |
HBsAg каждые |
|
|||||||||
|
|
- |
6 мес. Количественное определение HBsAg пока |
|
||||||||
В обобщенном виде алгоритм ведения больных |
|
|||||||||||
хроническим гепатитом В на фоне противовирус- |
не нашло широкого применения и используется |
|
||||||||||
ной терапии известен под названием «дорожная |
лишь в исследовательских целях. Пациентам с |
|
||||||||||
карта» – |
разработан в |
2007 г. профессором |
отсутствием |
первичного |
ответа |
на |
|
лечение на |
|
|||
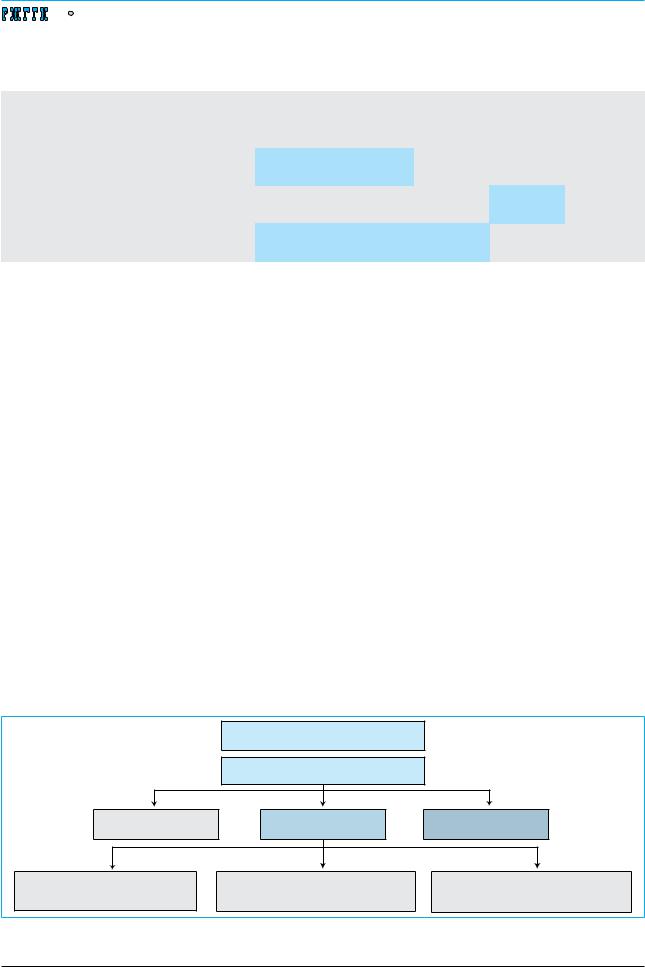
Э.Б. Кифи (рис. 2) [10]. |
М |
|
12-й неделе терапии ПЕГ-ИФН-α рекомендуется |
|
||||||||
|
|
|
|
|
отмена препарата и замена на аналоги нуклеози- |
|
||||||
Ведение пациента на фоне лечения |
дов/нуклеотидов. |
|
|
|
|
|
|
|||||
Мониторирование пациентов |
с |
HBeAg-нега- |
|
|||||||||
и после его отмены |
|
|
|
|
||||||||
|
|
|
тивным гепатитом В осуществляется так же, |
|
||||||||
|
|
|
|
|
|
|||||||
Терапия пегилированным интерфероном α |
как у пациентов с HBeAg-позитивным гепати- |
|
||||||||||
с четко |
определенной |
продолжительностью |
том В. При отсутствии HBV DNA, определяе- |
|
||||||||
лечения. На фоне лечения рекомендуются ежеме- |
мой методом ПЦР в реальном времени, показано |
|
||||||||||
сячное проведение клинического анализа |
крови |
исследование HBsAg с интервалом в 6 мес. |
|
|
||||||||
|
12 я неделя |
|
|
|
Оценка отсутствия первичного ответа |
|
|
|
24 я неделя |
|
|
|
Оценка факторов эффективности лечения |
|
|
Полный ответ |
Частичный ответ |
Неадекватный ответ |
|
HBV DNA – отрицательная |
60<HBV DNA<2000 МЕ/мл |
HBV DNA<2000 МЕ/мл |
|
Продолжить лечение |
Добавить препарат без перекрестной |
Добавить более эффективный препарат |
|
резистентности или продолжить лечение |
|||
Исследование HBV DNA каждые 6 мес |
Мониторирование HBV DNA каждые 3 мес |
||
Мониторирование HBV DNA каждые 3 мес |
|||
|
|
||
Рис. 2. «Дорожная карта» – алгоритм ведения больного хроническим гепатитом В на фоне противовирусной |
|||
терапии |
|
|
|
19

Лекции и обзоры |
3, 2009 |
На фоне интерферонотерапии требуется обязательно исключать все известные побочные эффекты.
Терапия аналогами нуклеозидов с определенной продолжительностью лечения больных с HBeAg-позитивным гепатитом В. Определение
HBV DNA проводится каждые 12 нед. Результаты клинических исследований свидетельствуют о необходимости отмены лечения не ранее 24–48 нед после HBeAg-сероконверсии, исследования HBsAg осуществляются через каждые 6 мес после HBeAg-сероконверсии.
Длительная терапия аналогами нуклеозидов:
Исследование HBV DNA рекомендуется проводить через 12 нед для оценки вирусологического ответа и затем каждые 12 и 24 нед. Оптимальное снижение вирусной нагрузки, практически исключающее риск развития резистентности, составляет менее 10–15 МЕ/мл методом ПЦР в реальном времени. У пациентов с HBeAg-позитивным гепатитом В исследование HBeAg и HBeAb рекомендуется выполнять каждые 6–12 мес.
Заключение
Современные подходы к терапии хронического гепатита В составлены с учетом роли вирусной нагрузки в прогрессировании заболевания в цирроз печени и гепатоцеллюлярную карциному, а также эффективности лечения. Рациональный выбор схемы противовирусной терапии, с одной стороны, и мониторирование HBV DNA в процессе ее проведения, с другой, позволяют прогнозировать отдаленные результаты лечения, риск развития резистентности на фоне применения аналогов нуклеозидов/нуклеотидов и своевременно принимать решение по изменению схемы терапии. Новые аналоги нуклеозидов обладают высокой эффективностью, хорошей переносимостью и профилем безопасности при длительном использовании. Адекватное применение противовирусных препаратов позволяет улучшить выживаемость пациентов, уменьшить летальность, риск развития цирроза печени и гепатоцеллюлярной карциномы, оптимизировать затраты на лечение.
Список литературы |
|
|
|
|
|
|
|
12. Lai C.L., Gane E., Liaw Y.F. et al. Telbivudine versus |
||||||||||
1. |
Blumberg B.S., |
Alter H.J. et |
al. A «new» |
antigen |
in |
|
lamivudine in |
patients with chronic hepatitis B // N. |
||||||||||
|
Engl. J. Med. – 2007. – Vol. 357. – P. 2576–2588. |
|||||||||||||||||
|
leukemia sera // JAMA. – 1965. – Vol. 191. – P. 541. |
|
||||||||||||||||
|
13. |
Lai C.L., Shuoval D., Lok A.S. et al. Entecavir versus |
||||||||||||||||
2. |
Chang T.T., Gish R.G., de Man R. et al. A comparison |
|||||||||||||||||
|
lamivudine for patients with HbeAg-negative chronic |
|||||||||||||||||
|
of entecavir and lamivudine for HBeAg-positive chronic |
|
||||||||||||||||
|
|
hepatitis B // N. Engl. J. Med. – 2006. – Vol. 354. |
||||||||||||||||
|
hepatitis B // N. Engl. J. Med. – 2006. – Vol. 354. – P. |
|
||||||||||||||||
|
|
– P. 1011–1020. |
|
|
||||||||||||||
|
1001–1010. |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
14. |
Lok A.S., Hussain M. et al. Antiviral |
drug-resistant |
||||||
3. |
Chien-Jen Sc.D., Hwai-I. Yang, MSc et al. Risk |
of |
||||||||||||||||
|
HBV: standardization of nomenclature and assays and rec- |
|||||||||||||||||
|
hepatocellular carcinoma across a biological-gradient of |
|
||||||||||||||||
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
Вестиommendations for management // Hepatology. – 2007. |
||||||||
|
serum hepatitis B virus DNA level // JAMA. – Jan 4. |
|
– Vol. 46. – P. 254–265. |
|
|
|||||||||||||
|
– 2006. |
|
|
|
|
М |
|
|
|
|
||||||||
|
|
|
|
|
|
15. |
Lok A.S., McMahon B.J. AASLD practice guidelines. |
|||||||||||
4. |
EASL |
Clinical |
Practice |
Guidelines: |
Management |
of |
||||||||||||
|
Chronic hepatitis B // Hepatology. – 2007. – Vol. 45. |
|||||||||||||||||
|
chronic |
hepatitis |
B |
// J. Hepatol. – |
50 (2009), doi: |
|
||||||||||||
|
|
– P. 507–539. |
|
|
||||||||||||||
|
10.1016/j.lhep.2008.10.001. |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
16. |
Marcellin P., Buti M., Krastev Z. et al. A randomized |
||||||||||
5. |
Fournier C., Zoulim F. |
Antiviral |
therapy of chronic |
|||||||||||||||
|
double-blind, comparison of tenofovir DF versus adefovir |
|||||||||||||||||
|
hepatitis B: prevention of drug resistance // Clin. Liver |
|
||||||||||||||||
|
|
dipivoxil |
for |
the treatment of HBeAg |
negative chronic |
|||||||||||||
|
Dis. – 2007. – Vol. 11. – P. 869–892. |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
hepatitis |
B: |
Study GS-US-174-0102 |
// |
Hepatology. |
||||||||
6. |
Hadziyannis S.J., |
Tassopoulos |
N.C., |
Heathcote E.J. |
|
|||||||||||||
|
– 2007. – Vol. 46. – P. 290–291. |
|
|
|||||||||||||||
|
et al. Long-term therapy |
with |
adefovie |
dipivoxil |
for |
|
|
|
||||||||||
|
17. |
Marcellin |
P., Chang T.T., Lim S.G. et |
al. Adefovir |
||||||||||||||
|
HBeAg-negative chronic hepatitis B for up to 5 years // |
|||||||||||||||||
|
|
dipivoxil for treatment of hepatitis B e-antigen positive |
||||||||||||||||
|
Gastroenterology. – 2006. – Vol. 131. – P. 1743–1751. |
|
||||||||||||||||
|
|
chronic hepatitis B // N. Engl. J. Med. – 2003. – Vol. |
||||||||||||||||
7. |
Heathcote E.J., Gane E., Deman R. et al. A randomized |
|
||||||||||||||||
|
348. – P. 808–816. |
|
|
|||||||||||||||
|
double-blind, comparison of tenofovir DF (TDF) versus |
|
|
|
||||||||||||||
|
18. |
Marcellin P., Jacobson I., Habersetzer F. et al. Tenofovir |
||||||||||||||||
|
adefovir dipivoxil (ADV) for treatment of HBeAg posi- |
|||||||||||||||||
|
|
disoproxil fumarate for the treatment of HBeAg-negative |
||||||||||||||||
|
tive chronic hepatitis B (CHB): Study GS-US-174-0103 |
|
||||||||||||||||
|
|
chronic hepatitis B: week 72 TDF data |
and week 24 |
|||||||||||||||
|
// Hepatology. – 2007. – Vol. 46. – P. 861. |
|
|
|
||||||||||||||
|
|
|
|
adefovir dipivoxil switch data (study 102) // J. Hepatol. |
||||||||||||||
8. |
Hoofnagle J.H., |
Doo E., |
Liang T.J. Management |
of |
|
|||||||||||||
|
– 2008. – Vol. 48 (suppl. 2). – P. 26. |
|
|
|||||||||||||||
|
hepatitis B: summary of a clinical research workshop // |
|
|
|
||||||||||||||
|
19. |
Marcellin P., Lau G.K., Bonino F. et al. Peginterferon |
||||||||||||||||
|
Hepatology. – 2007. – Vol. 45. – P. 1056–1075. |
|
||||||||||||||||
|
|
|
alfa-2a alone, lamivudine alone, and the two in combina- |
|||||||||||||||
9. |
Janssen |
H.L., van |
Zonneveld |
M., |
Senturk |
H. et |
al. |
|
||||||||||
|
tion in patients with HBeAg-negative chronic hepatitis B |
|||||||||||||||||
|
Pegilated interferon |
alfa |
2b alone |
or |
in combination |
|
||||||||||||
|
|
// N. Engl. J. Med. – 2004. – Vol. 351. – P. 1206– |
||||||||||||||||
|
with lamivudinefor |
HbeAg-positive |
chronic |
hepatitis |
|
|||||||||||||
|
|
1217. |
|
|
|
|
||||||||||||
|
B: a randomized trial // Lancet. – 2005. – Vol. 365. |
|
|
|
|
|
||||||||||||
|
20. |
Pawlotsky J.M., Dusheiko G., Hatzakis A. et al. |
||||||||||||||||
|
– P. 123–129. |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
Virologic monitoring of hepatitis B virus therapy in clini- |
|||||||
10. |
Keeffe |
E.B., Zeuzem S., |
Koff |
R.S. et |
al. Report |
of |
|
|||||||||||
|
cal trials and practice: recommendations for a standard- |
|||||||||||||||||
|
an international |
workshop: roadmap |
for |
management |
|
|||||||||||||
|
|
ized approach // Gastroenterology. – 2008. – Vol. 134. |
||||||||||||||||
|
of patients receiving oral |
therapy for |
chronic hepatitis |
|
||||||||||||||
|
|
– P. 405–415. |
|
|
||||||||||||||
|
B // Clin. Gastroenterol. Hepatol. – 2007. – Vol. 5. |
|
|
|
||||||||||||||
|
21. |
Uchenna H. Iloeje, Hwai-I. Yang et |
al. Predicting cir- |
|||||||||||||||
|
– P. 890–897 |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
rhosis risk based on the level of circulating hepatitis B viral |
|||||||
11. |
Lai C.L., Chien R.N., Leung N.W. et al. A one-year |
|
||||||||||||||||
|
load // Gastroenterology. – 2006. – Vol. 130, N 3. |
|||||||||||||||||
|
trial of lamivudine for chronic hepatitis B // N. Engl. J. |
|
||||||||||||||||
|
|
|
|
|
|
|
||||||||||||
Med. – 1998. – Vol. 339. – P. 61–68.
20
