
4 курс / Акушерство и гинекология / Akusherstvo_Aylamazyan_2015
.pdf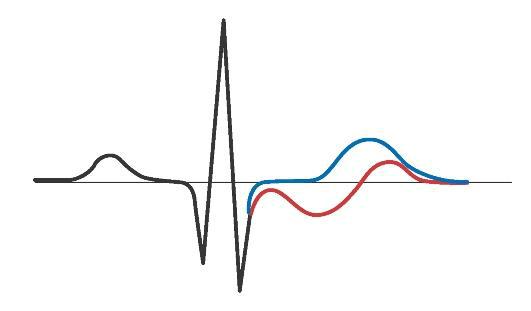
Рис. 10.18. Двухфазныйсегмент ST (Williams Obstetrics, 2010)
• эпизодическое повышение соотношения T/QRS - повышение данного соотношения в течение 10 мин с возвратом к исходному уровню; обычно это свидетельствует о кратковременной гипоксии плода;
•продолжительное увеличение соотношения T/QRS - более 10 мин; отмечается при активации процессов анаэробного метаболизма;
•появление двухфазного сегмента ST (рис. 10.17, 10.18).
Полученная информация о событиях должна интерпретироваться с учетом данных КТГ, так как даже при нормальной КТГ возможны кратковременные изменения соотношенияT/QRS или сегмента ST.
10.10. Оценка содержания в крови беременной эмбриоспецифических белков
Оценка в крови матери эмбриоспецифических белков (фетопротеина, β- субъединицы хорионического гонадотропины) проводится в рамках биохимического скрининга врожденных и наследственных заболеваний плода (см. главу 3).
Инвазивные методы
Инвазивные внутриматочные вмешательства во время беременности являются частью пренатального скрининга врожденных и наследственных заболеваний (см. главу 3), используются с целью диагностики и лечения гемолитической болезни плода (см. главу 41), многоплодной беременности (см. главу 30).
10.11. Пренатальная диагностика наследственных и врожденных заболеваний плода
Пренатальная (дородовая) диагностика - один из важнейших видов профилактики рождения детей с тяжелыми, некорригируемыми пороками развития, с социально значимыми смертельными генными и хромосомными болезнями, направленный на уменьшение генетического груза популяции.
Как научно-практическое направление пренатальная диагностика (ПД) возникла в 80-х годах ХХ в. на стыке клинических дисциплин (акушерство, гинекология, неонатология) и фундаментальных наук (генетика человека, цитогенетика, молекулярная
151
биология, эмбриология, биохимия, патофизиология). Первая в нашей стране лаборатория ПД была создана в 1987 г. в НИИ акушерства и гинекологии им. Д. О. Отта РАМН (г. Ленинград).
Как раздел практической медицины ПД представляет собой комплекс врачебных мероприятий и диагностических методов, направленных на выявление морфологических, структурных, молекулярных или устойчивых функциональных нарушений внутриутробного развития человека. Эти нарушения проявляются в виде изолированных или множественных врожденных пороков, хромосомных или моногенных болезней, в виде дисплазий, дизрупций или дисфункций жизненно важных систем, органов и тканей, которые вызывают гибель плода или приводят к тяжелым, нередко смертельным заболеваниям в постнатальном периоде.
Цель пренатальной диагностики - ранняя диагностика, профилактика и лечение наследственных и врожденных заболеваний плода. Основные задачи пренатальной диагностики:
1)обеспечение ранней диагностики внутриутробной патологии и оптимальной тактики ведения беременности;
2)предоставление будущим родителям исчерпывающей информации о степени риска рождения больного ребенка;
3)при наличии высокого риска - предоставление информации о возможности прерывания беременности и последствиях принятого родителями решения - родить больного ребенка или прервать беременность;
4)определение прогноза здоровья будущих детей.
Основные составляющие и алгоритм ПД:
1)медико-генетическое консультирование;
2)УЗ-скрининг в 10-13; 19-21 и 30-31 нед беременности;
3)биохимический скрининг в 9-13; 15-18 нед беременности;
4)лабораторная диагностика (цитогенетическая, молекулярная);
5)рекомендации по результатам пренатальной диагностики.
10.11.1. Методы оценки состояния плода
В настоящее время зародыши человека доступны для лабораторных исследований практически на любой стадии внутриутробного развития, однако методы, применяемые для этих целей, различны.
До имплантации обследование эмбрионов, диагностика генных и хромосомных болезней возможны только вне организма женщины с помощью методов и подходов, применяемых в программах экстракорпорального оплодотворения (ЭКО), т. е. в центрах вспомогательных репродуктивных технологий (ВРТ).
Подавляющее большинство ПД во всем мире и в России проводится после 10-й недели, преимущественно в I и отчасти - во II (15-21 нед) триместрах беременности. Именно на этот период приходятся все основные инвазивные операции по получению плодного материала. В III триместре инвазивная ПД проводится редко и только в связи с необходимостью решения вопроса о тактике ведения беременности и родов в зависимости от диагноза заболевания у плода.
Методы оценки состояния плода могут быть прямыми, когда исследуется сам плод, либо - непрямыми, когда объектом исследования является беременная женщина. В свою очередь, прямые методы подразделяются на инвазивные и неинвазивные (схема 10.1).
152

Непрямые методы. Цель - отбор женщин групп высокого риска по рождению детей с врожденной и наследственной патологией, требующих углубленного дополнительного обследования, включающего специальные лабораторные (цитогенетические, биохимические, молекулярные) исследования плодного материала. Непрямые методы позволяют судить о состоянии плода по биохимическим показателям в крови беременной, по результатам акушерско-гинекологического анамнеза и медико-генетического консультирования.
Схема 10.1. Методы оценки состояния плода
Последнее показано для всех супружеских пар, планирующих ребенка, для всех беременных женщин и обязательно - для женщин групп высокого риска.
Биохимические исследования (БС) маркерных сывороточных белков крови беременной, равно как ультразвуковое сканирование, являются обязательными скринирующими методами ПД, направленными на выявление женщин групп высокого риска по рождению детей с хромосомными болезнями и пороками развития.
Прямые методы, направленные на исследование самого плода, могут бытьнеинвазивными и инвазивными. Основным и наиболее эффективным прямым неинвазивным методом является исследование плода методом эхографии, т. е. с помощью ультразвукового аппарата. Совершенствование ультразвуковой (УЗ) техники, повышение ее разрешающей способности позволяет уже в конце I триместра заподозрить наличие хромосомной патологии у 80% плодов с аномальным кариотипом, а во II триместре - у 8098% плодов с анатомическими пороками. УЗ-обследование, безусловно, является наиболее эффективным современным неинвазивным методом ПД. Другие неинвазивные методы (МРТ, электрокардиография) имеют весьма ограниченное применение.
Вместе с тем многие видимые отклонения в развитии (УЗ-маркеры), в том числе и врожденные пороки развития (ВПР), позволяют только заподозрить наличие хромосомных или, реже, генных болезней у плода. Такая диагностика возможна только путем специальных лабораторных исследований плодного материала. Для его получения разработаны и широко используются в ПД различные инвазивные методы. Главные из них: хорионбиопсия и плацентобиопсия - получение ворсин хориона или плаценты (I и II триместры беременности соответственно), амниоцентез - получение образцов амниотической жидкости (II триместр) и кордоцентез - пункция пуповины с целью взятия крови плода (II-III триместры).
153
Выбор инвазивного метода определяется сроком беременности, показаниями к его проведению, инструментальной и методической оснащенностью центра ПД, а также квалификацией акушера-оператора.
10.11.2. Медико-генетическое консультирование
Медико-генетическое консультирование проводится врачом-генетиком или врачом-акушером, прошедшим специализацию по медицинской генетике и имеющим соответствующую лицензию. МГК является наиболее распространенным видом профилактики наследственных и врожденных болезней. Суть его заключается в определении рисков рождения ребенка с наследственной и врожденной патологией, в объяснении вероятности неблагоприятного исхода беременности, в помощи женщине (семье) в принятии решения о деторождении.
Прямые показания к направлению к врачу-генетику:
•установленная или подозреваемая наследственная болезнь в семье;
•значимые отклонения результатов биохимического скрининга маркерных сывороточных белков беременной;
•выявление УЗ-маркеров хромосомных болезней и ВПР у плода;
•высокий риск по результатам комбинированного УЗ и БС в I триместре;
•кровнородственные браки;
•воздействие возможных тератогенов (мутагенов) до или в течение первых 3 мес беременности.
Основной целью пренатального МГК (ПМГК) является разработка алгоритма профилактики наследственной и врожденной патологии. Важно, чтобы врач аргументированно принимал решение о целесообразности направления беременной на инвазивную диагностику для исключения хромосомной или генной патологии у плода. Рекомендации после ПД требуют не только глубоких знаний по медицинской генетике, но и широкой эрудиции в области репродукции человека, эмбриологии, тератологии, педиатрии и акушерства.
Во всех случаях первичная ПМГК проводится до инвазивной процедуры и лабораторной диагностики.
Задачами врача-генетика при ПМГК семьи по вопросам ПД являются:
•оценка рисков различных видов патологии (моногенной, хромосомной, ВПР и МВПР) при настоящей беременности;
•определение необходимости инвазивной ПД;
•оценка возможности проведения ПД в конкретной семье;
•определение объема всех пренатальных мероприятий и оптимальных сроков обследований;
•уточнение возможностей и ограничений диагностических методов;
•обсуждение с семьей вероятных результатов и вариантов возможных решений (необходимо заранее обсудить с семьей вероятную тактику поведения в случае, если предполагаемый диагноз подтвердится).
Критерии включения нозологии в группу заболеваний для инвазивной пренатальной диагностики (ИПД) следующие:
• тяжелое заболевание у будущего ребенка, наличие которого является достаточным основанием для прерывания беременности;
154
•лечение предполагаемого заболевания отсутствует или малоэффективно;
•семья согласна прервать беременность, если у плода подтвердится диагноз;
•имеются надежные лабораторные тесты для точной ПД заболевания;
•высокий генетический риск при данной беременности;
•исследование необходимо для уточнения состояния плода, тактики ведения беременности и родов, а также необходимой срочной медицинской помощи ребенку после рождения.
Срок выполнения операций по получению плодного материала, его лабораторные исследования, постановка окончательного диагноза и выдача ответа должны быть завершены к 22-й неделе беременности. Таким образом, скрининговые УЗИ плода II триместра следует выполнять на сроке 19-20 нед.
При выявлении патологии или получении неоднозначных результатов семье требуется серьезная помощь в принятии решения о прерывании беременности. Важно отметить, что все возрастающие возможности хирургической коррекции ВПР и другие виды помощи должны обсуждаться только после исключения хромосомной патологии у плода.
10.11.3. Скрининговые методы исследования
Задача пренатального скрининга - идентификация женщин групп высокого риска по рождению детей с хромосомными болезнями и ВПР. Такие женщины нуждаются в более детальном анализе состояния плода с помощью специальных лабораторных методов исследования.
Основные скринирующие программы в ПД:
•ультразвуковой скрининг;
•биохимический скрининг маркерных белков в сыворотке крови беременной (БС);
•другие типы скрининга: цитогенетический, молекулярный, иммунологический.
Центральное место в ПД занимают ультразвуковой и биохимический скрининг. Все остальные типы скрининга играют вспомогательную роль и в ПД имеют весьма ограниченное применение. Так, цитогенетический скрининг ранее широко применялся для пренатального кариотипирования плода у женщин после 35 лет. Однако в связи с повышением эффективности методов УЗ и БС (особенно комбинированного скрининга) возраст женщины перестал рассматриваться в качестве самостоятельного фактора риска для цитогенетического скрининга. Последний проводится при наличии в семье хромосомных перестроек и в условиях доимплантационной диагностики. Молекулярный скрининг используется для выявления у супругов скрытого носительства мутаций, связанных с частыми наследственными болезнями (муковисцидоз, спинальная мышечная атрофия, синдром ломкой Х-хромосомы). Широкое применение получил молекулярный скрининг для ранней диагностики некоторых частых болезней у новорожденных. Современный неонатальный скрининг направлен на раннее выявление пяти моногенных заболеваний: муковисцидоза, адреногенитального синдрома, фенилкетонурии, галактоземии и гипотиреоза. Иммунологический скрининг касается скрининга на носительство скрытых инфекций, представляющих опасность для плода, а также выявления уже на ранних сроках беременности женщин с резус-отрицательной группой крови, что важно для правильной профилактики гемолитической болезни новорожденных.
Ультразвуковой скрининг
155
Ультразвуковой скрининг - основной неинвазивный метод ПД, широко применяется для эффективного выявления врожденных пороков развития (ВПР).
Ультразвуковое исследование (УЗИ), выполненное в адекватные сроки и в соответствии с утвержденными протоколами, позволяет уже в конце I триместра заподозрить наличие хромосомной патологии у 80% плодов с аномальным кариотипом, а во II триместре - у 80-98% плодов с анатомическими пороками. В настоящее время метод широко используется для скрининга патологии и ПД.
С 2012 г. скрининговая программа УЗИ беременных проводится при сроках беременности 10-14, 18-22 и 32-34 нед с целью пренатальной диагностики нарушений развития плода.
При первом скрининговом УЗИ (11-14 нед беременности) основной целью является выявление наличия увеличения толщины воротникового пространства, как основного эхографического маркера хромосомных аномалий. Кроме того, важными задачами УЗИ при данных сроках являются оценка жизнеспособности плода, числа плодов в матке, уточнение срока беременности, исключение грубых, абсолютно летальных форм ВПР, визуализация носовых костей и т. д.
При сроке 18-22 нед беременности основное внимание обращается на анатомические особенности строения плода, его размеры, соответствие сроку беременности, выявляется большинство распространенных форм ВПР, аномалии плаценты и пуповины, проводится оценка количества околоплодных вод. Кроме обычного УЗИ, для уточнения состояния сердечно-сосудистой системы плода используется допплерометрия.
Третье скрининговое УЗИ (32-34 нед беременности) направлено на изучение темпов роста плода, его анатомических и функциональных особенностей, выявление ВПР с поздней манифестацией, проведение анализа состояния систем фетального жизнеобеспечения (сердце, плацента, пуповина, оболочки) для выработки оптимальной тактики и стратегии родов.
Основу диагностики составляет комбинированный ультразвуковой и биохимический скрининг на 10-13-й неделе беременности с обязательным автоматическим подсчетом риска болезни Дауна у плода. Алгоритм обследования начинается с консультации врача-генетика, продолжается врачом УЗ-диагностики, который измеряет толщину воротникового пространства и проводит визуализацию назальных косточек, в это же время параллельно исследуются маркерные сывороточные белки крови на два эмбриональных белка (PAPP-A и свободная β-субъединица HCG). По результатам этих двух независимых (биохимических и ультразвуковых) анализов проводится автоматический расчет риска хромосомных нарушений у плода, на основании которого принимается решение о необходимости инвазивной ПД (схема 10.2).
156

Схема 10.2. Алгоритм комбинированного ультразвукового и биохимического скрининга
При выявлении нарушений развития у плода беременная направляется на обследование второго уровня (специализированное или экспертное УЗИ), которое проводится на аппаратах высокого разрешения и позволяет осуществлять диагностику не только анатомических пороков, но и стойких функциональных нарушений.
Наличие грубых, несовместимых с жизнью анатомических пороков плода, выявленных при УЗИ, может являться основанием для рекомендации о прерывании данной беременности после проведения пренатального консилиума. Вместе с тем уместно напомнить, что УЗИ только констатирует факт наличия нарушений, но не вскрывает их причину. Соответственно, крайне важно обеспечить пациентке проведение специализированного обследования, в том числе и медико-генетического для определения этиологии (экзогенной или наследственной) выявленного порока.
Биохимический скрининг маркерных белков
Биохимический скрининг в настоящее время является общепринятым методом отбора женщин с высоким риском хромосомных болезней и врожденных пороков развития (ВПР) у плода. Суть метода заключается в исследовании отклонений сывороточных маркеров - СМ (эмбриональных сывороточных белков в крови матери) от нормы при хромосомной патологии плода. В настоящее время БС проводят преимущественно на 10-13-й неделях беременности (отбор женщин высокого риска рождения детей с хромосомными аномалиями - ХА), на 15-18-й неделях выполняют ПД хромосомных нарушений у плода и некоторых пороков развития (дефекты нервной трубки (ДЗНТ) открытого типа, незаращение передней брюшной стенки и др.).
Биохимический скрининг во II триместре позволяет выявлять от 65 до 74% (в зависимости от выбранного порогового уровня риска) женщин с трисомией 21 у плода. В I триместре беременности при комбинированном скрининге показана более высокая эффективность выявления трисомии 21 (от 82 до 94%). При положительном результате БС беременной рекомендуется консультация врача-генетика с целью направления на инвазивную ПД.
К биохимическим маркерам в крови матери относятся альфа-фетопротеин (АФП), хорионический гонадотропин (ХГЧ) и его свободная β-субъединица (свободный β-ХГЧ), свободный (неконъюгированный) эстриол (НЭ), плазменный ассоциированный с беременностью белок А (ПАББ-А, англ. РАРР-А), ингибин А и некоторые другие.
157
Все эти белки являются эмбрионспецифичными, т. е. продуцируются клетками самого плода или плаценты и поступают в кровоток матери. Их концентрация в сыворотке крови меняется в зависимости от срока беременности и от состояния плода. Оценка результатов БС как в I, так и во II триместрах беременности проводится автоматически с использованием различных компьютерных программ. Итогом БС является полный расчет индивидуального риска хромосомной патологии у плода, прежде всего, болезни Дауна.
При соблюдении всех сроков обследования 90% всех инвазивных вмешательств можно осуществить до 18-й недели беременности. Такая тактика позволяет выявить до 8792% плодов с синдромом Дауна. Самой распространенной причиной отклонений при БС является неверное определение срока беременности. Поэтому при несоответствии уровня белка норме необходимо, в первую очередь, уточнить срок беременности с помощью УЗИ.
В настоящее время принято считать, что ни УЗ, ни БС по отдельности не являются достаточными для эффективной профилактики хромосомных болезней и ВПР у плода. Стандартизация и сочетание указанных методов позволяют существенно улучшить выявление хромосомных аберраций (ХА) и сузить группу беременных высокого риска врожденной и наследственной патологии у плода.
Показания к направлению на инвазивную пренатальную диагностику
В системе мероприятий ПД одно из важнейших мест принадлежит ИПД, т. е. диагностике на плодном материале, полученном с помощью различных оперативных методов. В подавляющем большинстве случаев ПД проводится с целью кариотипирования плода и значительно реже - для диагностики моногенных болезней.
Группы риска для ИПД формируются по результатам скринирующих программ (УЗИ и БС), а также на основании медико-генетического консультирования. Стандартные показания для направления на инвазивную ПД включают:
•наличие у супружеской пары ребенка или плода с болезнью Дауна, другими хромосомными болезнями;
•наличие у супружеской пары ребенка или плода с множественными врожденными пороками развития;
•семейное носительство хромосомных перестроек;
•наличие в семье моногенных заболеваний: муковисцидоза, фенилкетонурии, гемофилии А и В, миопатии Дюшенна, миотонической дистрофии, адреногенитального синдрома, спинальной амиотрофии Верднига-Гоффмана, хореи Гентингтона и др.;
•ультразвуковые маркеры хромосомных болезней у плода;
•высокий риск болезни Дауна по результатам комбинированного (УЗ и БС) скрининга в I триместре, биохимического скрининга или наличия УЗИ-маркеров во II триместре беременности.
Несмотря на исключение возраста супругов из показаний к инвазивной ПД, в связи с внедрением комбинированного (УЗ и БС) скрининга в I триместре беременности (10-13 нед беременности) возраст женщины учитывается в программе «Астрайя» и является важным показателем при автоматическом расчете риска. Риск хромосомной патологии у плода для женщин в возрасте 35 лет и старше составляет 3,1% в I триместре и 2,2% - во II (16-17 нед беременности). Это снижение определяется естественной элиминацией значительной части плодов с хромосомными аномалиями на ранних сроках беременности. Особенно высок риск хромосомных аномалий у плода при наличии патологии, выявляемой при УЗ-обследовании. Наличие УЗ-маркеров увеличивает риск рождения ребенка с хромосомными болезнями в среднем до 11,3% и, как правило, их наличие является важнейшим показателем для кариотипирования плода.
158

В настоящее время, как указывалось выше, расчеты риска хромосомных болезней плода проводят с учетом комплекса показаний, основными критериями которого являются возраст беременной, результаты биохимического скрининга и УЗИ.
10.11.4. Инвазивные методы получения плодного материала
Инвазивными методами ПД называются внутриматочные вмешательства, выполняемые в операционных условиях под УЗ-контролем с целью получения плодного материала для последующих гистологических, биохимических, цитогенетических или молекулярных анализов. Как уже отмечалось, зародыш человека доступен для исследований, а следовательно и для диагностики, практически на любой стадии развития
(схема 10.3).
Для доимплантационной диагностики применяются методы микрургии, позволяющие удалять полярные тельца или отдельные бластомеры. Удаление единичных бластомеров на стадии морулы и клеток трофэктодермы на стадии бластоцисты проводится под микроскопом в условиях центра ЭКО. Основным методом получения плодного материала в I триместре является трансабдоминальная хорионбиопсия, а во II триместре беременности - трансабдоминальные плацентобиопсия, амниоцентез и кордоцентез.
Выбор инвазивного метода определяется сроком беременности, показаниями к его проведению, инструментальной и методической оснащенностью центра ПД, а также квалификацией акушера-оператора. Последнее обстоятельство существенно отражается на частоте ранних послеоперационных осложнений, под которыми понимают угрожающие состояния, вплоть до самопроизвольного прерывания беременности в течение 14 дней после процедуры.
Специальные лабораторные методы исследования плодного материала (бластомеров, ворсинок хориона, амниоцитов или лимфоцитов плода) могут быть различны, зависят от целей и сроков ПД. Наиболее востребованными являются цитогенетические методы и методы молекулярной (ДНК) диагностики.
Схема 10.3. Инвазивные методы пренатальной диагностики
159
10.11.5. Принципы и методы пренатальной диагностики хромосомных болезней
Основная часть инвазивных ПД с целью исключения хромосомных болезней проводится в группах риска, сформированных по результатам ультразвукового и биохимического скрининга. Анализ кариотипа плода должен сопровождать любое инвазивное внутриматочное вмешательство, проводимое и по другим показаниям (ПД моногенных болезней, лечение гемолитической болезни у плода и др.), так как геномные мутации возникают de novo, и любая беременность может завершиться рождением ребенка с хромосомной болезнью.
Внастоящее время проблема диагностики хромосомных аномалий на любом сроке беременности практически решена. Разработаны надежные и эффективные методы приготовления препаратов и анализа хромосом в клетках плода и зародышевых оболочек. Для снижения трудоемкости кариотипирования разработаны автоматические системы анализа изображений с соответствующим программным обеспечением.
Вкомплексе со стандартными цитогенетическими методами уже сегодня широко используются методы молекулярной цитогенетики, которые позволяют проводить общий
или выборочный анализ всего кариотипа и/или индивидуальных хромосом.
В диагностике частых хромосомных болезней уже широко применяются молекулярные методы, основанные на анализе ДНК: КФ-ПЦР, мультиплексная лигазная полимеразная реакция (MLPA), сравнительная геномная гибридизация на микрочипах - метод CGH. Заслуживают быть отмеченными некоторые обстоятельства диагностики хромосомных нарушений у плода, существенные для врачей-акушеров, в том числе обеспечивающих получение материала плода.
1. Наиболее часто для культивирования используют амниотические клетки, полученные на 15-18-й неделе беременности. Использование для этих целей амниоцитов более ранних (12-14 нед беременности) или более поздних (после 20-й недели беременности) сроков принципиально возможно, но, как правило, резко осложняет и удлиняет процесс диагностики. Стандартное культивирование амниоцитов с момента получения амниотической жидкости до кариотипирования занимает от 14 до 21 дня.
2.Использование во II триместре беременности метода количественной полимеразной цепной реакции (КФ-ПЦР) позволяет проводить скрининг 95% наиболее частых хромосомных болезней у плода, в том числе болезни Дауна (трисомия 21), синдрома Эдвардса (трисомия 18), синдрома Патау (трисомия 13) и аномалий половых хромосом.
3.Многие сложности, связанные с диагностикой хромосомных болезней у плода (хромосомный мозаицизм, хромосомные перестройки, наличие дополнительных маркерных хромосом), в настоящее время могут быть успешно преодолены благодаря наличию новых методов молекулярной цитогенетики (метод флуоресцентной
гибридизации in situ FISH и метод сравнительной геномной гибридизации - CGH).
10.11.6. Принципы и методы диагностики моногенных болезней
В настоящее время диагностика практически всех моногенных болезней проводится с использованием молекулярных методов, называемых также методами ДНКанализа (отсюда часто упоминаемая в современной научной литературе «ДНКдиагностика»). Принимая во внимание их высокую точность, большую чувствительность и, к сожалению, достаточно высокую стоимость, необходимо помнить, что эффективность ДНК-диагностики у плода в значительной мере определяется соблюдением следующего ряда требований:
• точностью клинического диагноза;
160
