
4 курс / Акушерство и гинекология / Akusherstvo_Aylamazyan_2015
.pdf•своевременным обследованием семьи высокого риска и больного молекулярными методами;
•правильностью оценки риска рождения больного ребенка;
•выбором оптимального срока ПД;
•возможностью получения материала плода;
•четкостью рекомендаций после ПД.
Некоторые из них имеют непосредственное отношение к клинике.
1.Для правильной и своевременной диагностики наследственной болезни у плода зачастую необходимо провести молекулярно-генетическое исследование больного ребенка в этой семье. Отсутствие такого ребенка может существенно затруднить и в ряде случаев сделать невозможной пренатальную диагностику в семье высокого риска.
2.Правильность клинического диагноза предполагает и правильность оценки риска рождения больного ребенка. Известно, что для аутосомно-рецессивных заболеваний риск составляет 25%, для аутосомно-доминантных - 50%, для болезней, сцепленных с полом, - 50% для мальчиков.
3.При полной информативности семьи для ДНК-диагностики (хорошо известна мутация, полиморфизмы) оптимальным сроком ПД для большинства наследственных заболеваний (муковисцидоз, фенилкетонурия, адреногенитальный синдром, спинальная мышечная атрофия и др.) является I триместр (10-12 нед беременности). В случае частичной информативности семьи следует привлечь дополнительные методы молекулярной или биохимической диагностики, чтобы успеть установить диагноз до 21-й
недели беременности.
4.Врачам важно знать, что ДНК-диагностика универсальна и возможна на любых клетках плода и его провизорных органов. Помимо биопсийного материала для молекулярного анализа можно использовать соскоб клеток с цитологических препаратов, ранее использованных для кариотипирования зародыша, пятна крови, нанесенные на фильтровальную бумагу, а в некоторых случаях даже секционный материал, заключенный
впарафиновые блоки.
5.Следует помнить о том, что ДНК-диагностика у плода может быть прямая, когда
всемье высокого риска, а следовательно, предположительно и у ребенка, известна мутация, вызывающая болезнь, или косвенная, когда известны генные маркеры, с которыми сцеплена болезнь. Для каждого наследственного заболевания разработан свой алгоритм молекулярной диагностики, а основным методом является отмеченная Нобелевской премией знаменитая полимеразная цепная реакция (ПЦР). Точность прямой ДНК-диагностики, как правило, очень высокая и приближается к 100%, точность косвенной диагностики зависит от выбранного молекулярного маркера, но обычно превышает 95%.
6.Большую опасность для ДНК-диагностики, учитывая огромную чувствительность этого метода, представляет контаминация тканей плода клетками материнского организма. Избежать ее можно только путем тщательного отбора ворсинок хориона или плаценты с их последующим отмыванием изотоническим раствором натрия
хлорида.
10.11.7. Прерывание беременности и верификация диагноза
При выявлении хромосомной или генной патологии обязательным этапом ПД является консультирование женщины с предоставлением ей всей информации о прогнозе
161
жизни ребенка в случае его рождения (важно, что решение вопроса о сохранении или прерывании беременности женщина принимает самостоятельно).
Важным этапом ПД является верификация диагноза. В случае хромосомной патологии необходимо не только подтвердить хромосомную аномалию у плода, но и провести патоморфологическое изучение абортуса. В настоящее время разработана представленная ниже схема верификации пренатального диагноза, которая предусматривает активное участие патоморфолога, врача-генетика, врача УЗД, цитогенетика и молекулярного биолога.
1.После установления факта хромосомного дисбаланса у плода рекомендуется повторное УЗИ высокого уровня, которое позволяет выявить аномалии развития у плода, не отмеченные при первичном осмотре.
2.После прерывания беременности в I триместре проводится цитогенетический анализ хромосомных препаратов из тканей и органов абортусов с использованием традиционных цитогенетических методов, а также методов гибридизации in situ (методы FISH) и молекулярных методов.
3.После искусственного или самопроизвольного прерывания беременности во II триместре вследствие мацерации большинства тканей плода возможности цитогенетической диагностики ограничены, для кариотипирования могут быть использованы методы культивирования тканей, а также метод FISH. Обязательным
является |
детальный |
патоморфологический |
анализ |
в |
соответствии |
с протоколомисследования случаев антенатальной гибели плода. |
|
|
|||
10.11.8. Эффективность пренатальной диагностики
Эффективность ПД определяется частотой, с которой удается выявить плоды с тяжелыми ВПР, с хромосомными и моногенными болезнями. Наиболее эффективна в этом отношении, т. е. по числу выявленных ВПР, УЗ-диагностика, она позволяет выявлять до 80% всех врожденных пороков, в том числе практически все, несовместимые с жизнью. Ультразвук особенно эффективен в диагностике ВПР центральной нервной системы. Наибольшие трудности представляет диагностика изолированных пороков сердца, а также дефектов лицевого черепа и дистальных отделов конечностей (15%). Благодаря успехам неонатальной хирургии многие, особенно изолированные, пороки успешно корректируются после рождения. Поэтому при выявлении ВПР у плода рекомендуется консультация хирургов-неонатологов. Однако до принятия решения о постнатальной коррекции любых ВПР необходимо исключить хромосомные болезни с помощью инвазивной ПД.
Эффективность цитогенетической ПД в значительной мере зависит от срока беременности и от показаний, с которыми женщина пришла на диагностику. Так, эффективность ПД в I триместре составляет около 7-8%, во II он обычно снижается до 3- 5%.
10.11.9. Новые направления в пренатальной диагностике
Несмотря на то, что основные методические и организационные проблемы ПД уже успешно решены, данный раздел медицинской генетики продолжает активно развиваться. Неуклонно увеличивается арсенал новых методов и подходов. К перспективным направлениям ПД относятся доимплантационная диагностика и неинвазивная диагностика по клеткам и нуклеиновым кислотам плода в крови матери.
Доимплантационная диагностика
162

Благодаря быстрому развитию методов ВРТ и прецизионных методов анализа генома единичных клеток (методы молекулярной цитогенетики, варианты FISH) ДД все шире входит в практику центров ЭКО. Спектр заболеваний, доступных для этого вида диагностики, в настоящее время насчитывает более 30 нозологий и включает все наиболее частые моногенные и хромосомные болезни. При этом есть все основания считать, что ДД никогда не станет массовой и ее реальный вклад в решение демографической проблемы нашей страны будет очень скромным. Тем не менее, учитывая большую востребованность, нетрудно предвидеть дальнейший рост популярности этой технологии.
Материалом для ДД могут быть полярные тельца или отдельные бластомеры дробящейся яйцеклетки. В зависимости от материала ДД можно подразделить на преконцепционную (анализ полярных телец) и собственно доимплантационную (анализ бластомеров или клеток трофобласта) (схема 10.4).
Схема 10.4. Алгоритм доимплантационной диагностики
Сложности работы с единичными клетками, необходимость наличия первоклассного современного оборудования и высококвалифицированных специалистов существенно лимитирует широкое внедрение этой прогрессивной технологии. Диагностика на изолированных бластомерах позволяет получить точную информацию о генотипе эмбриона. В основном биопсия одного-двух бластомеров осуществляется на стадии 8-10 клеток. Поскольку на ранних стадиях дробления все бластомеры тотипотентны (т. е. взаимозаменяемы), удаление нескольких клеток не сказывается на дальнейшем развитии эмбриона.
Выбор метода молекулярной диагностики определяется спецификой исследуемой мутации и включает как метод ПЦР, так и более сложные ДНК-методы. Они позволяют проводить диагностику всех наиболее распространенных моногенных болезней.
Цитогенетическая ДД проводится на одном-двух бластомерах методом FISH с использованием ДНК-зондов, специфичных к хромосомам 13, 16, 18, 21, 22, X, Y. При гетерозиготном носительстве транслокации одним из родителей для диагностики методом FISH используются ДНК-зонды, специфичные к хромосомам, участвующим в перестройке.
163
Более надежная доимплантационная диагностика может быть проведена на стадии бластоцисты, когда зародыш состоит примерно из 60-100 клеток. При визуализации трофобласта без ущерба для дальнейшего развития можно удалить до 10 клеток трофобласта. Применение этого метода требует, однако, специального дорогостоящего оборудования - лазерной пушки для удаления нескольких клеток трофобласта без повреждения структуры бластоцисты.
Таким образом, единственное и основное преимущество ДД заключается в возможности трансплантации генетически полноценных эмбрионов, т. е. в возможности начать беременность заведомо здоровым плодом.
Диагностика по клеткам и нуклеиновым кислотам плода в крови матери
Любое хирургическое вмешательство при заборе плодного материала неизбежно сопряжено с риском осложнений. И поэтому разработка неинвазивных методов пренатальной диагностики, позволяющих избежать любых осложнений, представляется вполне оправданной. Более перспективным на сегодняшний день представляется предложенный недавно подход, основанный на анализе ДНК в крови матери. Показано, что ДНК из клеток плода (плаценты, плодных оболочек) попадает в плазму материнской крови и может быть обнаружена при помощи молекулярно-генетических методов.
В последние годы достигнуты большие успехи в связи с внедрением новых технологий исследования ДНК - глубокого параллельного секвенирования, позволяющих с высокой достоверностью (около 99%) установить наличие у плода болезни Дауна или трисомии двух других хромосом - 13 (болезнь Патау) и 18 (синдром Эдвардса). В октябре 2011 г. Международная ассоциация по пренатальной диагностике официально разрешила проведение неинвазивной ПД болезни Дауна. Значительные усилия по внедрению данного метода предпринимаются сегодня в России. В настоящее время этот метод уже находится на стадии сертификации. Очевидно, что диагностика по клеткам и нуклеиновым кислотам в крови матери, равно как и доимплантационная диагностика, еще неопределенно долго не станут реальной альтернативой ПД с использованием стандартных инвазивных методов в установленные сроки беременности. И поэтому, высоко оценивая уже существующие достижения доимплантационной и неинвазивной диагностики, совершенствование уже существующих стандартных подходов в сочетании с повышением разрешающей способности молекулярных и цитогенетических методов исследования следует рассматривать как реальную перспективу дальнейшего развития пренатальной диагностики XXI века.
Контрольные вопросы
1.Перечислите методы оценки состояния плода.
2.Какие показатели оценивают при анализе КТГ во время беременности?
3.Какие показатели оценивают при анализе КТГ во время родов?
4.Перечислите основные задачи, которые позволяет решить ультразвуковое исследование при беременности.
5.Назовите сроки выполнения трехкратного УЗИ при беременности.
6.Что такое «биофизический профиль плода»?
7.Кровоток в каких сосудах является наиболее частым объектом допплерометрического исследования при беременности?
8.Опишите показания и технику выполнения амниоскопии.
9.Назовите преимущества определения рН крови плода, уровня лактата в крови плода, пульсоксиметрии и ЭКГ плода для оценки его функционального состояния.
164
РАЗДЕЛ II. ФИЗИОЛОГИЯ РОДОВ. ГЛАВА 11. ГОТОВНОСТЬ ОРГАНИЗМА К РОДАМ
11.1. Причины наступления родов
Роды являются сложным физиологическим процессом, возникающим в результате взаимодействия многих органов и систем организма беременной женщины и состоящим в изгнании жизнеспособного плода и элементов плодного яйца.
До настоящего времени причины наступления родов остаются не вполне ясными, однако общепризнано, что в сложном и надежном механизме, контролирующем начало родов, участвуют многие факторы. Наиболее важную роль играют нейрогуморальные и гормональные системы как материнского организма, так и фетоплацентарного комплекса.
К концу беременности и началу родов у женщины наблюдается преобладание процессов торможения в коре большого мозга и повышение возбудимости подкорковых структур(гипоталамо-гипофизарной системы, структур лимбического комплекса, в первую очередь миндалевидных ядер, и спинного мозга). Усиливаются спинномозговые рефлексы, повышается рефлекторная и мышечная возбудимость матки. Электроэнцефалографические исследования в 1970-е гг. проф. И. И. Яковлева и его сотрудников показали, что к концу беременности у женщин отмечается усиление реакций на интероцептивные раздражители с шейки матки и ослабление (или даже отсутствие) реакций на экстероцептивные раздражители, что свидетельствует о формировании основы родовой доминанты, которая является необходимым условием для своевременного и правильного развертывания родовой деятельности. На фоне подобных изменений нервной системы женщины возрастает роль афферентной импульсации от плода, которая от рецепторов матки по подчревному и тазовым нервам поступает в спинной мозг и далее по спиноталамическому пути в таламус, гипоталамус и проекционные зоны коры большого мозга.
Важную роль в развитии родовой деятельности играют гормональные факторы. В последние 2 нед беременности, и особенно перед родами, происходит повышение уровняэстрогенов и снижение содержания прогестерона. На протяжении беременности прогестерон тормозит спонтанную активность матки. Снижение его продукции перед родами нарушает этот механизм и способствует активации сократительной деятельности миометрия.
Эстрогены через систему нуклеиновых кислот активируют синтез сократительного белка матки (актомиозина), усиливают синтез катехоламинов, активируют холинергическую систему, угнетают активность окситоциназы и моноаминооксидазы, разрушающих серотонин и катехоламины. Изменяя проницаемость клеточной мембраны для ионов кальция, калия, натрия, они меняют электролитные соотношения в мышце матки. Под действием эстрогенов увеличивается количество ионов калия внутри клетки (К+: Na+ = 5 : 3), изменяется мембранный потенциал покоя и увеличивается чувствительность клеток миометрия к раздражению. Таким образом, не вызывая сокращений миометрия, эстрогены как бы сенсибилизируют матку к веществам тономоторного действия.
В настоящее время принято считать, что ключевую роль в развязывании родовой деятельности играют простагландины (ПГЕ2, ПГ2α), синтез которых в децидуальной и амниотической оболочках значительно повышается перед родами.
Считается, что биосинтез простагландинов активируется стероидными гормонами. В этой связи представляет интерес роль плода и фетоплацентарного комплекса в целом в наступлении родов. Повышение уровня эстрогенов, продуцируемых системой мать-
165
плацента-плод, ведет к увеличению содержания простагландинов в матке. В этом процессе не исключается и роль кортизола надпочечников плода. Предполагается влияние и других плодовых факторов, в том числе синтезируемых в почках плода и с мочой поступающих в околоплодные воды, что служит сигналом к высвобождению арахидоновой кислоты, являющейся предшественницей простагландинов. Простагландины индуцируют родовой акт, вызывая деполяризацию мембран клеток миометрия и способствуя высвобождению связанного кальция, вследствие чего происходит сокращение мышцы матки. Кроме того, простагландины стимулируют секрецию окситоцина в задней доле гипофиза у матери и плода и вызывают разрушение прогестерона.
Окситоцин возбуждает α-адренорецепторы, расположенные преимущественно в теле матки, и угнетает β-адренорецепторы; он повышает возбудимость клеточных мембран, подавляет активность холинэстеразы, способствует накоплению ацетилхолина (АХ). АХ и окситоцин, потенцируя действие друг друга, вызывают сокращение матки. Однако существуют сведения о незначительном влиянии окситоцина (или об отсутствии его) на индукцию родового акта. Повышение синтеза окситоцина имеет большое значение для сократительной способности матки во время родов.
Наряду с окситоцином и ацетилхолином большое значение в инициации сократительной деятельности матки принадлежит серотонину, адреналину, норадреналину, гистамину (уровень которых повышается перед родами) и кининовой системе.
Серотонин обеспечивает проницаемость мембран для ионов кальция, вызывает деполяризацию клеточных мембран.
Катехоламины, являясь медиаторами нервной системы, повышают сократительную способность матки, воздействуя на нее через α-адренорецепторы (возбуждая их) и β-адренорецепторы (тормозя их).
Определенная роль в развязывании родовой деятельности принадлежит эпифизу, который продуцирует меланотонин. Меланотонин образуется путем ацетилирования серотонина, выделяется в кровяное русло и обнаруживается в периферических сосудах, нервах, яичниках, гипоталамусе и гипофизе. Циклические изменения секреции меланотонина связаны с более высокой интенсивностью его синтеза ночью и более низкой днем. Между меланотонином и серотонином существуют конкурентные отношения. Экскреция меланотонина за сутки до родов резко снижается. Низкий уровень меланотонина стимулирует повышение продукции окситотических веществ и серотонина, уменьшается тормозящее действие меланотонина на моторную функцию матки.
Большую роль в развитии родовой деятельности играет фетоплацентарный комплекс.
На развитие, а также регуляцию родовой деятельности существенное влияние оказываетгипофизарно-надпочечниковая система плода. Под влиянием активации гипоталамо-гипофизарной системы плода перед началом родов повышается выделение АКТГ передней долей гипофиза плода, который стимулирует синтез дегидроэпиандростерона (ДГЭА) в надпочечниках плода. ДГЭА поступает в печень плода, где происходит его гидроксилирование и образуется 16-ДГЭА. Последний поступает по сосудам пуповины в плаценту и превращается там в эстриол. Эстрогены синтезируются также непосредственно в надпочечниках плода и в его печени, причем в надпочечниках их синтезируется в 1,5-2 раза больше, чем в плаценте.
Перед началом родов увеличивается также количество кортизола, синтезируемого надпочечниками плода. Кортизол поступает оттуда в печень и превращается в ней в предшественники эстрогенов. С током крови последние поступают в плаценту, где
166

превращаются в эстрогены. Есть данные, согласно которым вазопрессин, выделяющийся гипофизом плода, действует аналогично кортикотропному гормону. Выделение вазопрессина сопровождается также высвобождением гипофизом плода окситоцина, который действует подобно окситоцину матери, выделяющемуся в конце беременности в большем количестве.
В мышце матки существуют несколько групп рецепторов: в теле матки - аи β- адренорецепторы; в нижнем сегменте - М-холино- и Д-серотонинорецепторы; в шейке матки - хемо-, механо- и барорецепторы.
Окситоцин, адреналин, норадреналин, простагландины и кинины стимулируют сокращение матки, возбуждая α-адренорецепторы и угнетая β-адренорецепторы. Серотонин, АХ, гистамин усиливают сократительную деятельность матки, возбуждая серотонино-, М-холино- и гистаминорецепторы.
Перед началом родов под влиянием нейрогуморальных изменений в матке преобладает активность α-адренорецепторов. В клетках миометрия снижается мембранный потенциал, увеличивается их возбудимость, усиливается спонтанная активность, повышается чувствительность к контрактильным веществам. Идет накопление энергетических веществ (гликоген, фосфокреатинин, актомиозин, глутатион) и электролитов (кальций, магний, натрий, калий), обеспечивающих сокращение миометрия.
Рис. 11.1. Факторы, стимулирующие развитие родовой деятельности: 1 - гипоталамус матери; 2 - гипофиз матери; 3 - спинной мозг; 4 - дуга спинального рефлекса; 5 - симпатический ганглий; 6 - дорсальный спинальный ганглий; 7 - механо-, баро-, хеморецепторы; 8 - миометрий; 9 - децидуальная ткань; 10 - плацента; 11 - амнион и хорион; 12 - гипофиз плода; 13 - надпочечники плода; 14 - печень плода; 15 - пуповина; 16
-шейка матки; 17 - влагалище; Ом и Оп - окситоцин из гипофиза матери и гипофиза плода; ДГЭА - дегидроэпиандростерон; Эс - эстриол; Э - эстрогены; П - прогестерон; а и в
-адренорецепторы; Э2 - рецепторы эстрогенов; М - М-холинорецепторы; Г - гистаминорецепторы; Д - Д-серотонинорецепторы; ПгЕ2, ПгF2α - рецепторы
простагландинов
167
При снижении мембранного потенциала все клетки миометрия могут генерировать возбуждение, однако в матке существует группа клеток, где это возбуждение возникает в первую очередь и затем распространяется на всю матку. Это так называемый водитель ритма (пейсмейкер), который располагается в дне матки, ближе к правому трубному углу.
Весь комплекс нервных, нейрогуморальных и эндокринных изменений, происходящих в организме перед родами, составляет так называемую родовую доминанту, определяющую наступление и правильное течение родов (рис. 11.1).
11.2. Понятие о готовности организма к родам
В последние 1,5-2 нед беременности заканчивается подготовка организма женщины к предстоящим родам. Эта подготовка охватывает все органы и системы, начиная с центров высшей нервной деятельности и кончая исполнительным органом - маткой. Доминанта беременности сменяется доминантой родов, а матка из плодовместилища превращается в изгоняющий орган.
Готовность организма женщины к родам характеризуется целым рядом признаков, появление которых указывает на возможность начала родов в ближайшее время. Наиболее ярко выраженные изменения происходят в половых органах. В отличие от оценки состояния центральной нервной системы или гормонального статуса, требующей привлечения специальных, как правило, сложных методов исследования, диагностика состояния полового аппарата осуществляется с помощью обычных клинических методов обследования беременной и несложных тестов. К ним относятся определение «зрелости» шейки матки, окситоциновый тест, маммарный тест, цитологическое исследование влагалищных мазков.
11.3. Методы оценки готовности к родам
«Зрелость» шейки матки может быть достаточно точно определена при влагалищном исследовании. Процесс «созревания» обусловлен следующими механизмами, достаточно хорошо изученными. Сочетанное морфологическое, биохимическое и гистохимическое изучение тканей шейки матки в сопоставлении с данными клинического определения готовности шейки матки к родам показали, что во время беременности в шейке матки происходит постепенное частичное замещение мышечной ткани соединительной. Наблюдаются изменения в самой соединительной ткани шейки: образуются «молодые» коллагеновые волокна, которые чрезвычайно гидрофильны и поэтому более гибки, чем коллагеновые волокна вне беременности. Часть коллагеновых волокон рассасывается и замещается основным веществом, главным компонентом которого является кислый мукополисахарид хондроитинсульфат. По мере прогрессирования беременности он постепенно деполимеризуется, что приводит к повышению гидрофильности тканей и продольному расщеплению коллагеновых волокон на коллагеновые фибриллы. Клинически это проявляется разрыхлением и укорочением шейки матки, зиянием просвета цервикального канала.
Процесс частичного рассасывания коллагеновых волокон и изменения состава основного вещества начинается с области наружного зева и постепенно распространяется к внутреннему зеву. Именно с этим связано то, что размягчение внутреннего зева в процессе «созревания» шейки матки происходит в последнюю очередь. Ускорение процессов «созревания» шейки матки отмечено у беременных после введения эстрогенных гормонов и простагландинов.
При пальпаторной оценке состояния шейки матки определяют ее консистенцию, степень ее укорочения, степень проходимости шеечного канала, расположение шейки
168
матки в полости малого таза, состояние нижнего сегмента матки при пальпации через влагалищные своды, изменение формы шеечного канала и соотношение длины влагалищной части шейки матки и длины шеечного канала.
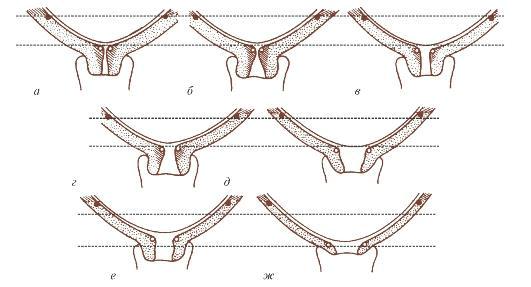
По совокупности этих признаков (классификация Г. Г. Хечинашвили) различают четыре разновидности состояния шейки матки: «незрелая», «созревающая», «неполностью созревшая» и «зрелая» (табл. 11.1, рис. 11.2).
Рис. 11.2. Изменения состояния и консистенции шейки и нижнего сегмента матки при поздних сроках беременности: а, б - шейка при беременности 32-34 нед размягчена по периферии, но участок плотноватой ткани по ходу канала еще сохранен, наружный зев у первородящих (а) пропускает кончик пальца, у повторнородящих (б) канал проходим до внутреннего зева для одного пальца: в, г - шейка при беременности 36-38 нед почти полностью размягчена, в области внутреннего зева обнаруживается участок плотноватой ткани: у первородящих (в) канал проходим за внутренний зев для одного пальца и имеет цилиндрическую форму, и у повторнородящих (г) канал свободно проходим за внутренний зев для одного пальца и имеет форму усеченного конуса, основание которого обращено книзу; д, е - шейка при доношенной беременности размягчена полностью как у первородящих (д), так и у повторнородящих (е), канал свободно проходим за внутренний зев для одного пальца и более; у первородящих канал имеет форму усеченного конуса с основанием, обращенным кверху, у повторнородящих - цилиндрическую форму; ж - шейка непосредственно перед началом родов у перво- и повторнородящих женщин резко укорочена, истончена, канал проходим более чем для одного пальца, в области внутреннего зева он плавно переходит в нижний сегмент матки
Таблица 11.1. Зрелость шейки матки (по Г. Г. Хечинашвили)
|
Степень зрелости шейки матки |
|
|
|
|
||
Характеристика |
|
|
|
|
|
|
|
|
|
|
|
«неполностью |
|
|
|
признака |
«незрелая» |
|
«созревшая» |
|
|
«зрелая» |
|
|
|
|
созревшая» |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Размягчена |
не |
Размягчена |
|
|
|
Плотная |
или |
почти |
|
|
||
|
полностью, |
|
|
|
|||
Консистенция |
размягчена |
|
|
полностью, |
за |
Размягчена |
|
|
определяется |
|
|||||
шейки матки |
только |
по |
|
исключением |
|
полностью |
|
плотноватая ткань |
по |
|
|||||
|
периферии |
|
области |
|
|
||
|
|
ходу шеечного канала |
|
|
|||
|
|
|
внутреннего |
|
|
||
169

|
|
|
|
|
|
|
|
|
|
|
|
зева |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Влагалищная |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
Влагалищная |
|
часть |
|
шейки |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
матки |
|
резко |
|||||
|
|
Влагалищная |
|
|
|
|
|
|
|
часть |
шейки |
|
||||||||
|
|
Влагалищная |
часть |
укорочена |
(2 |
см |
||||||||||||||
|
|
часть |
|
|
матки |
|
|
|
||||||||||||
Длина |
|
|
|
шейки |
матки |
слегка |
|
|
|
и |
|
менее), |
||||||||
|
сохранена |
или |
укорочена |
|
(ее |
|
||||||||||||||
влагалищной |
укорочена (длина ее от |
|
шеечный |
|
канал |
|||||||||||||||
слегка |
|
|
длина от 3 до 2 |
|
||||||||||||||||
части |
шейки |
|
|
4 до 3 см), шеечный |
соответствует по |
|||||||||||||||
матки |
и |
укорочена, |
|
канал |
|
длиннее |
см); |
|
шеечный |
длине |
|
|
|
|||||||
шеечного канала |
иногда |
очень |
влагалищной |
части |
канал |
на |
1 |
см |
влагалищной |
|
||||||||||
длинная |
(4 |
см |
длиннее |
|
|
|
||||||||||||||
|
|
и более) |
|
|
более чем на 1 см |
|
|
влагалищной |
|
части шейки или |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
длиннее |
|
ее |
не |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
части |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
более чем на 0,5 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
см |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
У |
первородящих |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
наружный |
|
зев |
Шеечный |
канал |
|
|
|
|
|||||||
|
|
|
|
|
пропускает |
|
кончик |
Шеечный |
канал |
|||||||||||
|
|
|
|
|
|
проходим |
|
для |
||||||||||||
|
|
|
|
|
пальца (реже проходим |
|
свободно |
|
|
|||||||||||
|
|
|
|
|
одного |
пальца |
|
|
||||||||||||
|
|
|
|
|
для одного |
пальца |
до |
проходим |
|
для |
||||||||||
Степень |
|
Наружный |
зев |
за |
внутренний |
|
||||||||||||||
|
внутреннего |
зева), |
|
у |
одного пальца за |
|||||||||||||||
проходимости |
закрыт |
|
или |
повторнородящих |
|
|
зев, |
|
|
|
нет |
внутренний |
зев, |
|||||||
шеечного канала |
пропускает |
|
|
|
плавного |
|
|
|||||||||||||
|
проходим для |
одного |
|
|
не |
изогнут, |
||||||||||||||
и его форма |
кончик пальца |
перехода |
|
|
||||||||||||||||
пальца до внутреннего |
|
|
плавно |
|
|
|
||||||||||||||
|
|
|
|
|
зева. Шеечный |
канал |
шеечного |
|
|
переходит |
|
в |
||||||||
|
|
|
|
|
канала в нижний |
|
||||||||||||||
|
|
|
|
|
изогнут, |
|
имеется |
нижний сегмент |
||||||||||||
|
|
|
|
|
|
сегмент |
|
|
||||||||||||
|
|
|
|
|
резкий |
переход |
его |
|
в |
|
|
|
|
|
|
|||||
|
|
|
|
|
нижний сегмент |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Толщина стенок |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
влагалищной |
2 см |
|
|
1,5 см |
|
|
|
|
|
1 см |
|
|
|
|
0,5 см |
|
|
|
||
части |
шейки |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
матки |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
Предлежащая |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
часть |
|
через |
Через |
|
своды |
|||
|
|
Предлежащая |
Предлежащая |
частьсводы |
|
|
|
отчетливо |
|
|
||||||||||
Состояние |
часть |
через |
через |
|
|
сводыпальпируется |
пальпируется |
|
||||||||||||
нижнего |
|
своды |
|
|
пальпируется |
|
|
|
довольно |
|
|
предлежащая |
|
|||||||
сегмента матки |
определяется |
недостаточно |
|
|
|
отчетливо, |
|
но |
часть |
|
плода, |
|||||||||
|
|
неотчетливо |
отчетливо |
|
|
|
|
ориентиры |
|
|
наориентиры |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
ней |
определитьопределяются |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
нельзя |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Окончание табл. 11.1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
Степень зрелости шейки матки |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Характеристика |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
«неполностью |
|
|
|
|
|
||||||
признака |
|
«незрелая» |
|
|
«созревшая» |
|
|
«зрелая» |
|
|
|
|||||||||
|
|
|
|
|
созревшая» |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|||||||||||||
Расположение |
Расположена |
|
вОтклонена |
от |
Располагается |
|
Располагается |
|||||||||||||
шейки в полостистороне |
|
|
|
отпроводной |
оси |
ближе |
|
|
|
к |
строго |
|
|
по |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
170 |
