
- •Расчет физико-химических свойств
- •Содержание
- •Введение
- •1. Метод аскадского
- •1.1. Сущность метода инкрементов
- •1.2. Расчет Ван-дер-ваальсовых объемов
- •Значения межмолекулярных радиусов ряда атомов
- •Значения длин связи между некоторыми атомами
- •(А) – полистирола, (б) – полидиметилсилоксана
- •2. Расчет основных физико-химических свойств полимеров
- •2.1 Характерные температуры полимеров
- •Температура стеклования
- •Температура плавления
- •Температура деструкции
- •2.2. Оптические свойства полимера Показатель преломления
- •Коэффициент оптической чувствительности по напряжению
- •2.3. Диэлектрическая проницаемость полимеров
- •2.4. Растворимость полимеров Плотность энергии когезии полимеров и параметр растворимости Гильдебранда
- •Критерий растворимости
- •2.5. Теплоемкость
- •3. Заключение
- •4. Задание для курсовой работы
- •Список литературы
- •Приложение 3.1 Значение параметров δi и γi различных атомов и типов межмолекулярного взаимодействия для расчета температуры плавления по формуле (8)
- •Приложение 3.2
- •Приложение 5.1 Атомные рефракции ряда атомов в органических соединениях по Эйзенлору для расчета коэффициента преломления
- •Приложение 5.2
- •Приложение 7 Величины ихарактеризующие вклады каждого атома и типа межмолекулярного взаимодействия в теплоемкость.
- •Приложение 8 Индивидуальное задание студентам для выполнения курсовой работы
- •450078, Г. Уфа, ул. Чернышевского, 145, к. 227; тел. (347) 278-69-85.
Температура плавления
Температура плавления (Tm) определяется как температура, при которой полимер переходит из кристаллического состояния в вязкотекучее состояние. Микрокристаллические полимеры вследствие их структурных особенностей не обладают четкой температурой плавления [5]. Как следствие, температура плавления является физической характеристикой полимера, которая трудно поддается расчету на основании строения полимерного звена [2]. Существует два возможных подхода для расчета данной физической характеристики, один из которых основан на соотношении температуры стеклования (Tg)и температуры плавления (Tm). При этом следует отметить, что по правилу БименаTg/ Tm2/3. Уравнение, связывающее температуру стеклования с температурой плавления, получено на основании экспериментальных данных [1, 2]:
|
|
(8) |
где
![]()
![]() (ki– парциальный коэффициент упаковкиi-атома);γi– инкременты, учитывающие вклад сильных
межмолекулярных взаимодействий;
(ki– парциальный коэффициент упаковкиi-атома);γi– инкременты, учитывающие вклад сильных
межмолекулярных взаимодействий;![]() .
Значенияδiиγiпредставлены в приложении 3.1. Расчеты,
проведенные по формуле (8), дают хорошее
совпадение с экспериментом. Однако
температура плавления сополимеров не
может быть описана простым соотношением,
полученным на основе уравнения (8).
.
Значенияδiиγiпредставлены в приложении 3.1. Расчеты,
проведенные по формуле (8), дают хорошее
совпадение с экспериментом. Однако
температура плавления сополимеров не
может быть описана простым соотношением,
полученным на основе уравнения (8).
Другой поход основан на рассмотрении повторяющегося звена полимера как набора ангармонических осцилляторов. Согласно выводам, приставленным в работах [1, 2], температуру плавления (Tm) полимера можно определить как:
|
|
(9) |
Значение Kiопределяется числом атомов образующих повторяющееся звено. Но так как сочетание некоторых групп атомов приводит к диполь-дипольному взаимодействию, водородным связям и т.д., то последние можно учесть путем добавления к энергиям дисперсионных взаимодействийDiтой доли энергии сильного межмолекулярного взаимодействия, которая обусловлена вкладомi-го атома. Тогда:
|
|
(10) |
где
![]() –
вклад атомаi-го типа
в диполь-дипольное взаимодействие;
–
вклад атомаi-го типа
в диполь-дипольное взаимодействие;![]() –
вклад атомаi-го типа
в водородную связь и т.д. Расчеты,
проведенные по уравнению (9) показали,
что ряда полимеров достаточно знать
параметрыDH,
–
вклад атомаi-го типа
в водородную связь и т.д. Расчеты,
проведенные по уравнению (9) показали,
что ряда полимеров достаточно знать
параметрыDH,
![]() ,DOи
,DOи![]() (приложение 3.2) для удовлетворительного
расчета температур плавления, исходя
из химического строения повторяющегося
звена. Следует отметить, что, во-первых,
формула (9) применяется только для
полимеров содержащих атомы водорода,
кислорода и углерода; а во-вторых,
несмотря на хорошую сходимость
экспериментальных и расчетных данных,
данный метод расчетаTmимеет ограниченное применение.
(приложение 3.2) для удовлетворительного
расчета температур плавления, исходя
из химического строения повторяющегося
звена. Следует отметить, что, во-первых,
формула (9) применяется только для
полимеров содержащих атомы водорода,
кислорода и углерода; а во-вторых,
несмотря на хорошую сходимость
экспериментальных и расчетных данных,
данный метод расчетаTmимеет ограниченное применение.
В работах [1, 2, 4] приведены таблицы расчетных значений температур плавления, вычисленных по формулам (8) и (9), ряда полимеров в сравнении с экспериментальными данными.
Температура деструкции
Согласно [5] деструкция высокомолекулярных соединений это расщепление макромолекул на низкомолекулярные вещества. При нагревании полимера происходит изменение его объема, причем это изменение складывается из двух частей: увеличение свободного объема и изменение длин связей. Анализ этих изменений привел к следующей зависимости температуры начала интенсивной термической деструкции (Td) от параметров химического строения:
|
|
(10) |
где
![]() – парциальный объем расширенияi-го
атома, возникающего за счет изменения
длин химических связей. При этом:
– парциальный объем расширенияi-го
атома, возникающего за счет изменения
длин химических связей. При этом:
|
|
(11) |
где d0– равновесное расстояние между химическими атомами;E– энергия диссоциации химических связей. С учетом уравнений (10) и (11) температура термодеструкции (Td) определяется из соотношения:
|
|
(12) |
где параметр
![]() – параметр, характерный для каждого
атома и типа межмолекулярного
взаимодействия и зависящий от энергии
химических связей распадающихся в
процессе деструкции. При этом:
– параметр, характерный для каждого
атома и типа межмолекулярного
взаимодействия и зависящий от энергии
химических связей распадающихся в
процессе деструкции. При этом:
|
|
|
В случае распада по C―Н связямd0= 1,08 Ǻ,E= 395 кДж/моль,a= 0,266 Ǻ-1.
Значения
![]() приведены
в приложении 4.
приведены
в приложении 4.
Поскольку атомы входят в состав полярных групп, обладающих специфическим межмолекулярным взаимодействием, то вклад их в термостойкость отличен от вклада, вносимого теми же атомами, обладающими лишь обычным Ван-дер-ваальсовым взаимодействием. Обычно в полимерах имеются следующие полярные группы:

При расчете Tdпо уравнению (12) учет межмолекулярных
взаимодействий проводится следующим
образом. Если атом не входит в состав
полярной группы, то его вклад обозначается![]() и
умножается на соответствующий
Ван-дер-ваальсовый объем. Если же атом
входит в состав полярной группы, то его
вклад обозначается
и
умножается на соответствующий
Ван-дер-ваальсовый объем. Если же атом
входит в состав полярной группы, то его
вклад обозначается![]() или
или![]() (h– водородная связь,d– диполь-дипольное
взаимодействие), и только
(h– водородная связь,d– диполь-дипольное
взаимодействие), и только![]() или
или![]() умножается на соответствующий
Ван-дер-ваальсовый объем, т.е. не
учитывается вклад данного атома в
Ван-дер-ваальсовое взаимодействие, как
существенно более слабое.
умножается на соответствующий
Ван-дер-ваальсовый объем, т.е. не
учитывается вклад данного атома в
Ван-дер-ваальсовое взаимодействие, как
существенно более слабое.
Примеры расчета величин Tdдля представителей различных классов полимеров приведены в работах [1, 2, 4].

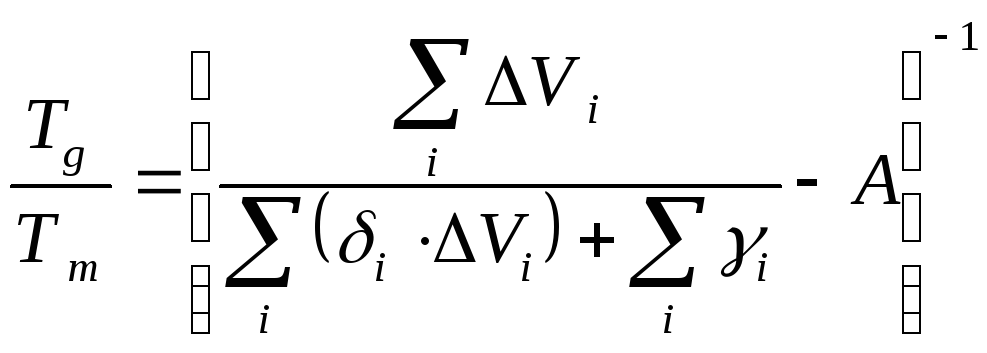 ,
,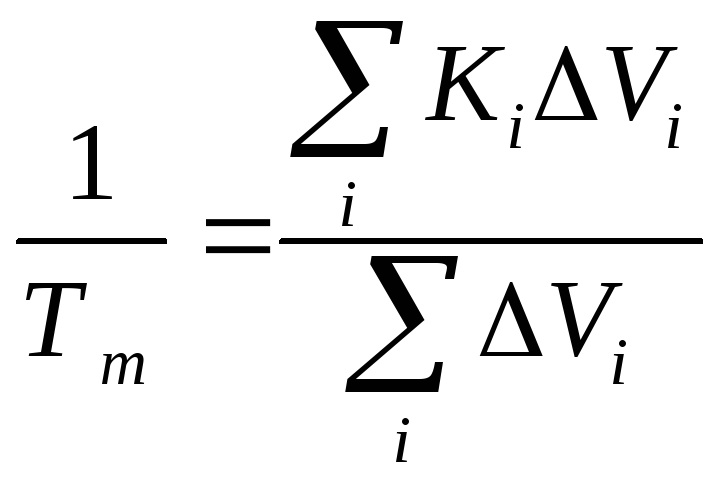 .
.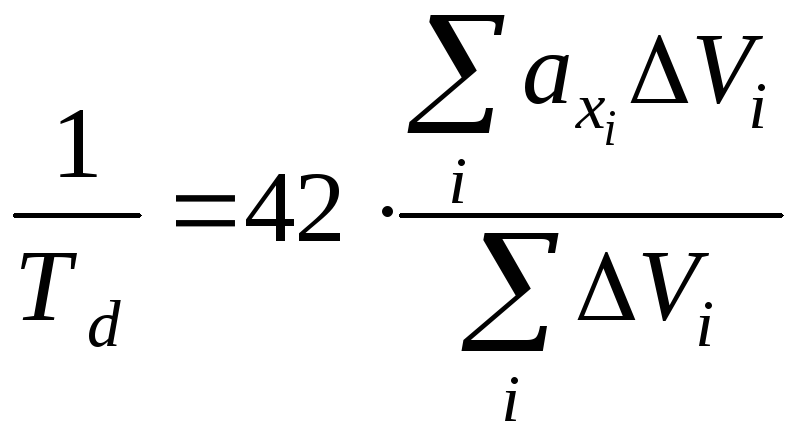 ,
,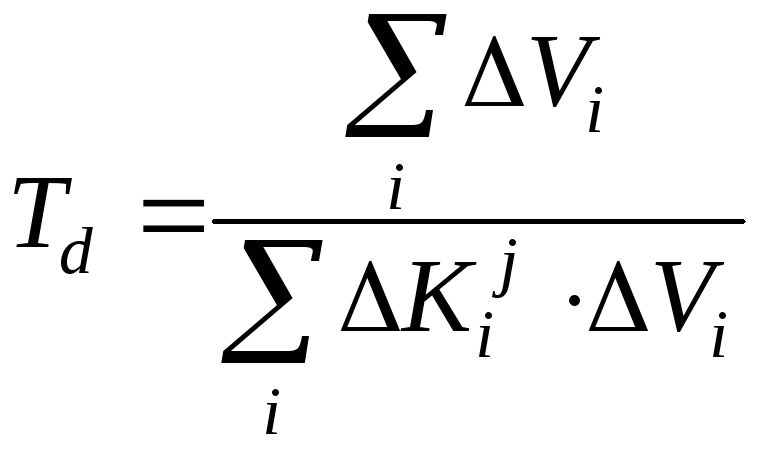 ,
,