- •Практическая работа № 1 Обработка стали в ковше синтетическим шлаком
- •Термодинамика процесса рафинирования стали жидким синтетическим шлаком
- •Межфазные свойства расплавов
- •Кинетика процессов рафинирования металла синтетическим шлаком
- •Рафинирование расплавов от примесей
- •Решение типовых задач
- •Задачи для решения
- •Варианты заданий:
- •Варианты заданий:
- •Варианты заданий:
- •Варианты заданий:
- •Практическая работа 2
- •2.2. Пример расчёта мощности вакуумной системы при обработке стали в агрегате vd и vd - ов (ковшевое вакуумирование)
- •I этап - создание рабочего разряжения в камере
- •2.3. Задание к расчету
- •Технические характеристики вакуумных пароэжекторных насосов оао«Северсталь»
- •Плотности газов
- •Основные размеры сталеразливочных ковшей
- •Варианты заданий
- •Литература
- •Практическая работа 3
- •3.2. Расчет времени коагуляции и удаления жидких включений
- •3.2. Расчет времени коагуляции и удаления твёрдых включений
- •3.3. Задание к расчету
- •Значение диссипации энергии и параметры процесса удаления оксидных включений при обработке стали на различных установках
- •Литература
- •Изменение температуры металла при легировании
- •4.1. Общие сведения
- •4.2. Примеры расчетов
- •4.3. Задание к расчету
- •Варианты заданий
- •Литература
Литература
Поволоцкий Д.Я., Кудрин В.А., Вишкарев А.Ф. Внепечная обработка стали. М: МИСиС, 1995.
Кнюппель Г. . Раскисление и вакуумная обработка стали. Ч.II. Основы и технология ковшевой металлургии: Пер. с нем. М.: Металлургия, 1984, - 414с.
Дорохов В.И.: Известия АН. Металлы, 1970, №5, с.51-55.
Практическая работа 4
Изменение температуры металла при легировании
4.1. Общие сведения
Температура стали при выпуске в ковш изменяется не только за счет потерь тепла теплоизлучением или теплопроводностью, но и за счет присадки легирующих элементов.
Легирующие элементы используются либо в чистом виде, либо в виде сплавов, большей частью в виде сплавов с железом (ферросплавов). При присадке легирующих материалов следует учитывать следующие изменения энтальпии стали, отнесенные к единице массы.
Нагрев и плавление присадок, происходящие с затратой тепла
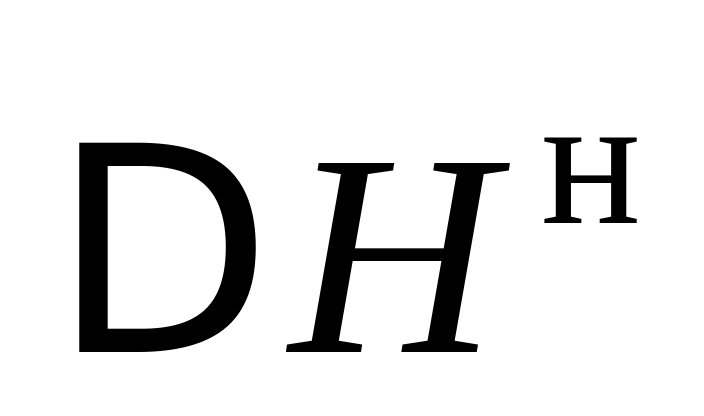 .
.Разложение интерметаллических соединений, имеющихся в сплавах, с подводом тепла
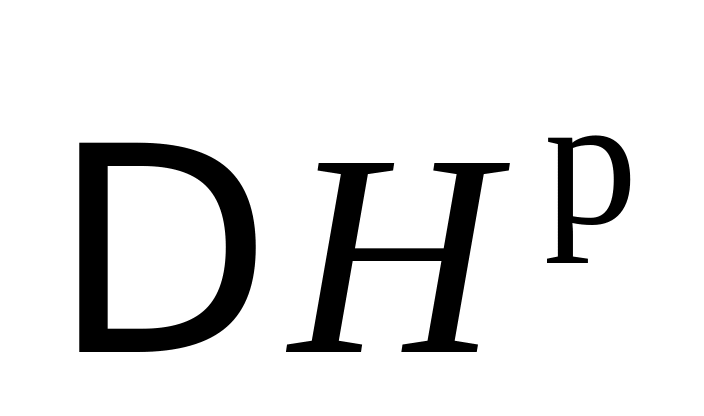 .
.Смешение расплавленной присадки с жидкой сталью, при этом теплота смешения
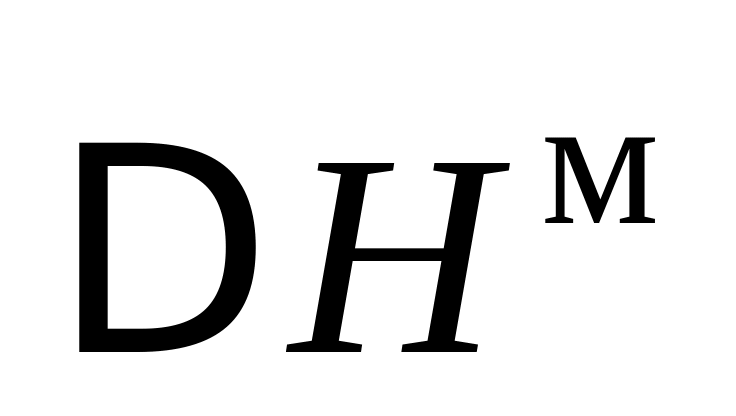 в случае образования идеального раствора
равна нулю; если образующийся раствор
не является идеальным, то может быть
как выделение (
<
0),
так и
поглощение (
>
0) тепла при смешении.
в случае образования идеального раствора
равна нулю; если образующийся раствор
не является идеальным, то может быть
как выделение (
<
0),
так и
поглощение (
>
0) тепла при смешении.Взаимодействие между легирующей присадкой и кислородом, растворенным в стали, с выделением тепла реакции
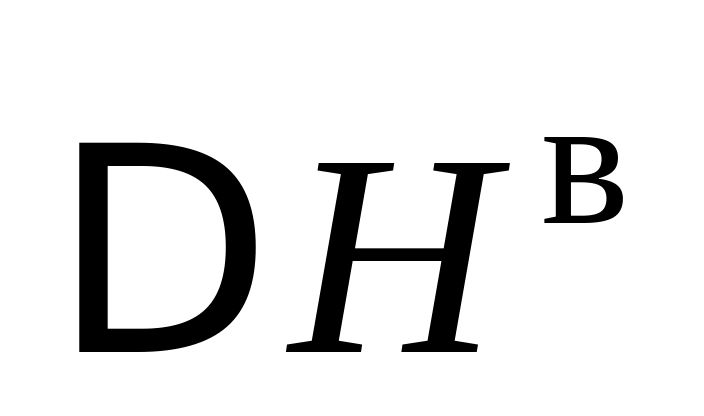 .
.
Если в стальной расплав вводится х % сплава, а с есть удельная теплоемкость стали, то изменение температуры расплавленной стали при легировании будет равно:
![]() ,
(4.1)
,
(4.1)
Значения теплот нагрева и плавления , смешения , разложения приведены в таблице 4.1.
Теплота смешения интерметаллических соединений равна теплоте образования с обратным знаком. Для обычно интересующих нас соединений теплота образования при комнатных температурах известна. Поэтому, зная концентрацию интерметаллических соединений в сплавах, можно рассчитать снижение температуры стали, вызванное затратой тепла на разложение этих соединений.
Теплоту смешения обычно используемых легирующих элементов с железом можно заимствовать из известных публикаций. Если же табличные данные для какогото элемента отсутствуют, то ее можно приближенно рассчитать по известному коэффициенту активности, допуская, что раствор является регулярным. Для бинарной системы используется соотношение:
![]() ,
(4.2)
,
(4.2)
где γ1 и γ2 – коэффициенты активности растворителя (1), и растворенного вещества (2); при этом за стандартное состояние выбирается чистое вещество, а концентрация выражается в молярных долях; N1 и N2 – молярные доли растворителя и растворенного вещества соответственно.
Коэффициенты активности растворителя и растворенного вещества связаны между собой уравнением Гибса-Дюгема:
![]() .
.
Это позволяет определить коэффициент активности одного компонента, если известен другой.
Теплоту реакции можно рассчитать по известным термодинамическим величинам.
4.2. Примеры расчетов
1.
Проведем
расчет на примере марганца.
Для нагрева марганца с 25 до 1600 °С и его
расплавления необходимое тепло
![]() составляет 81140
Дж/моль =
составляет 81140
Дж/моль =
![]() Дж/г.
Теплота смешения
марганца со сталью равна
=
5024 Дж/моль =
Дж/г.
Теплота смешения
марганца со сталью равна
=
5024 Дж/моль =![]() Дж/г.
Дж/г.
Теплотой реакции при 1600 °С можно пренебречь, поскольку равновесное с марганцем содержание кислорода в железе при невысоких концентрациях марганца, как правило, выше, чем фактическое содержание кислорода в стали. В соответствии с уравнением (4.1) имеем:
![]() .
.
Удельная
теплоемкость стали при 1600 °С равна 43,1
![]() ,
или 43,1/55,85
= 0,772 Дж/(гּК).
Таким образом, при введении в стальной
расплав 1 % Мn
произойдет понижение температуры на
,
или 43,1/55,85
= 0,772 Дж/(гּК).
Таким образом, при введении в стальной
расплав 1 % Мn
произойдет понижение температуры на
ΔU = 1568,3ּ1 : (100ּ0,772) = 20 °С.
При использовании ферромарганца, содержащего, например, 75 % Мn, необходимо еще учесть затраты тепла на нагрев и расплавление железа. При введении 1 % Мn ферромарганец вносит 0,33 % Fe. Для нагрева железа с 25 до 1600 °С и его расплавления требуется, по данным [1], 72724 Дж/моль или 72724/55,85 = 1308,5 Дж/г. Где 55,85 – атомная масса Fe. Для 0,33 % Fe затраты тепла составят 1308,5ּ0,33 = 431,8 Дж. Теплота смешения 75 % ферромарганца составляет [1] 76,6 Дж/г. Поэтому снижение температуры стали при введении 1 % Мn за счет присадок 75 % ферромарганца cоставит:
![]() °С.
°С.
В
расчетах в соответствии с диаграммой
состояния Fe-Мn
пренебрегли теплотой
разложения
![]() .
.
Предварительный подогрев 75 % ферромарганца, например до 800 °C снижает необходимое тепло подогрева до = 971,3 Дж/г и соответственно уменьшает снижение температуры стали до
![]() °С.
°С.
2. Во втором примере рассмотрим присадку кремния в стальной расплав при 1600 °С. Теплота нагрева и растворения кремния составляет ΔНн = 91272 Дж/моль = -91272/28,09 = 3249 Дж/г. Теплота смешения кремния с жидким железом равна в среднем ΔНм = -121417 Дж/моль = -121417/28 09 = - 4322 Дж/г. Тогда при введении 1 % Si
![]() °С,
°С,
т.е. температура стали повышается на 14 °С.
При использовании 90 % ферросилиция следует принять во внимание, что ~ 20 % Si находится в виде интерметаллического соединения FeSi2 с теплотой образования 715,9 Дж/г FeSi2 (при стандартных условиях). Отсюда теплота разложения равна 715,9ּ02ּ09 = 128,9 Дж. Кроме того, необходимо учесть тепло на нагрев и расплавление железа ферросилиция. Это тепло при введении в сталь 1 % Si, при этом ферросилиций вносит 0,11 % Fe, составит 1308,5ּ0,11 = 144 Дж. Таким образом при добавке в сталь 1 % Si за счет 90 %-ного ферросилиция изменение температуры стали (нагрев) составит
![]() °С.
°С.
Дополнительно предположим, что в жидкой стали растворено 0,01 % кислорода, с которым кремний будет реагировать. Тепловой эффект реакции можно рассчитать из уравнения раскисления:
lg ([% Si] ּ [% О]2) = -31040 / Т + 12,0
или
2,303 RT lg ([% Si] ּ [% О]2) = -142000 + 54,94 Т.
Отсюда ΔНв равно -594526 Дж/моль SiO2 или -594526/3,2 = = -18579 Дж/г О2.
 При
содержании в стали 1 % Si
в металле при 1600 °С, исходя из константы
равновесия [% Si]
[% О]2
=
3ּ10-5,
остаточное содержание
кислорода
равно
При
содержании в стали 1 % Si
в металле при 1600 °С, исходя из константы
равновесия [% Si]
[% О]2
=
3ּ10-5,
остаточное содержание
кислорода
равно
![]()
![]() ;
т.е. за
время раскисления удалится 0,01 – 0,0055 =
0,0045 % кислорода. Отсюда изменение
(повышение)
температуры стали за счет теплоты
реакции составит:
;
т.е. за
время раскисления удалится 0,01 – 0,0055 =
0,0045 % кислорода. Отсюда изменение
(повышение)
температуры стали за счет теплоты
реакции составит:
![]() °C.
°C.
Если же исходное содержание кислорода в стали – 0,05 % и конечное – 0,0445 %, т.е. когда количество удаленного за период раскисления кислорода составит 0,05 – 0,0055 = 0,0445 %, изменение температуры стали (нагрев) достигнет
![]() °С.
°С.
Следовательно сталь дополнительно нагреется на 11 °С. Общий нагрев стали для случая использования металлического Si составит 25 °С.
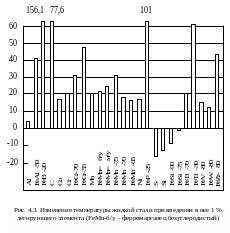
Снижение температуры стали за счет теплоты разложения при использовании 90 % ферросилиция и введении 1 % Si составляет 144 / (100ּ0,772) = = 2 °С, что очень мало. Однако в зависимости от типа сплава, как видно из рис. 4.1, снижение температуры стали за счет теплоты разложения может быть значительным и составлять, например, при использовании 50 %-ного ферроалюминия 20 °С.
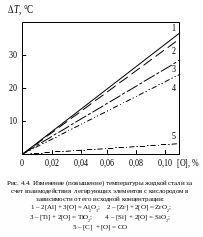
Из работы [1] заимствованы и рис. 4.2-4.4. На рис. 4.2. представлена зависимость изменения температуры жидкой стали от количества присаженных элементов для раскисления в чистом виде и в форме различных ферросплавов. На рис. 4.3. показано изменение температуры жидкой стали при введении в нее 1 % легирующих элементов в чистом виде или в виде обычных промышленных ферросплавов.
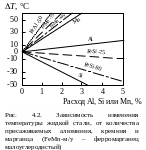 Результаты,
представленные на рис. 4.1-4.3, не учитывают
теплоту реакции легирующего
элемента с кислородом. Это пренебрежение,
как показано при расчетах с кремнием,
допустимо, если содержание кислорода
в стали низко (например, менее 0,01
%), что имеет место при выплавке сталей
с повышенным содержанием углерода (>
0,3 %) или в конце вакуумной обработки
стали. В противном случае экзотермические
реакции раскисления ведут к повышению
температуры стали, что следует из рис.
4.4.
Результаты,
представленные на рис. 4.1-4.3, не учитывают
теплоту реакции легирующего
элемента с кислородом. Это пренебрежение,
как показано при расчетах с кремнием,
допустимо, если содержание кислорода
в стали низко (например, менее 0,01
%), что имеет место при выплавке сталей
с повышенным содержанием углерода (>
0,3 %) или в конце вакуумной обработки
стали. В противном случае экзотермические
реакции раскисления ведут к повышению
температуры стали, что следует из рис.
4.4.
Приведенный выше материал позволяет проводить оценку изменения температуры жидкой стали, которое следует ожидать при ее раскислении и легировании. Он указывает также пределы, до которых возможно производить присадку легирующих элементов в ковш, если сталь в дальнейшем не подогревается. Так, при производстве, например, трансформаторной стали, содержащей 4 % Si, с использованием 90 % ферросилиция повышение температуры стали с учетом теплоты реакции составит (см. рис. 4.2.) 4ּ10 + 10 = 50 °С. Наоборот, присадка 3 % Сr в виде 70 % феррохрома приведет к охлаждению стали на 3ּ30 = 90 °С. В этом случае необходимо предусмотреть предварительный перегрев стали.