
- •I. Физколлоидная химия
- •1. Физическая химия
- •1.1. Вода
- •1.1.1. Вода как уникальная молекула жизни
- •1.1.3. Буферные растворы
- •1.2. Биоэнергетика клетки
- •1.3. Термохимия
- •1.4. Химическая кинетика и катализ
- •2. Коллоидная химия
- •2.1. Классификация дисперсных систем
- •2.2. Классификация дисперсных систем по агрегатному состоянию дисперсной фазы
- •2.2. Поверхностные явления
- •2.3. Адсорбция
- •2.4. Коллоидные растворы (золи)
- •2.4.1. Характеристика коллоидных растворов
- •2.4.2. Растворы высокомолекулярных соединений
- •II. Биологическая химия
- •3. Белки
- •3.1. Общая характеристика белков
- •3.3. Методы выделения, фракционирования и очистки белков
- •3.3.1. Методы выделения белков
- •3.4. Физико-химические свойства белков
- •3.5. Аминокислоты
- •3.6. Структура белковой молекулы
- •I'm 1.8. Денатурация и ренатурация рибонукле- азы (по Анфинсену):
- •3.7. Классификация белков
- •3.7.1. Простые белки
- •3.7.2. Сложные белки
- •4. Нуклеиновые кислоты
- •4.1. Общая характеристика нуклеиновых кислот
- •4.2. Нуклеотиды и нуклеозиды
- •4.3. Дезоксирибонуклеиновая кислота
- •4.4. Рибонуклеиновые кислоты
- •5. Углеводы 5.1. Общая характеристика углеводов
- •5.2. Моносахариды
- •5.3. Олигосахариды
- •5.4. Полисахариды (глюканы)
- •6. Липиды
- •6.1. Общая характеристика липидов
- •6.2. Простые липиды
- •6.3. Сложные липиды
- •6.4. Двойной липидный слой клеточных мембран
- •Контрольные вопросы и задания
- •7. Витамины
- •7.1. Общая характеристика витаминов
- •7.2. Классификация и номенклатура витаминов
- •7.2.1. Жирорастворимые витамины
- •7.2.2. Водорастворимые витамины
- •8. Ферменты 8.1. Общая характеристика ферментов
- •8.3. Общие свойства ферментов
- •8.4. Активирование и ингибирование ферментов
- •8.2. Участие ионов металлов в активировании ферментов
- •8.5. Классификация и номенклатура ферментов
- •III класс. Гидролазы. Они разрывают внутримолекулярные связи путем присоединения
- •8.6. Применение ферментов
- •9. Гормоны
- •9.1. Уровни регуляции гормонов
- •9.2. Гормоны, выделяемые железами внутренней секреции
- •9.3. Гормоны местного действия
- •11. Обмен углеводов
- •11.1. Переваривание углеводов в пищеварительном тракте
- •11.2. Катаболизм глюкозы
- •11.3. Цикл трикарбоновых кислот
- •11.4. Пентозофосфатный путь окисления глюкозо-6-фосфата
- •11.5. Биосинтез углеводов
- •11.6. Регуляция обмена углеводов
- •12. Обмен липидов
- •12.1. Переваривание липидов в пищеварительном тракте
- •12.2. Промежуточный обмен липидов
- •2. Если синтезируется много сн3—со—КоА, а энергии для синтеза жира недостаточно, то образуется активированная ацетоуксусная кислота:
- •12.3. Биосинтез липидов
- •12.4. Метаболизм стеринов и стеридов
- •13. Обмен белков
- •13.2. Биологическая ценность белков
- •13.3. Особенности переваривания белков у моногастричных животных
- •13.4. Особенности переваривания белков у жвачных
- •13.5. Метаболизм белков в тканях
- •13.6. Особенности обмена отдельных аминокислот
- •13.7. Биосинтез белка
- •14. Обмен нуклеиновых кислот
- •14.1. Переваривание нуклеиновых кислот в пищеварительном тракте
- •14.2. Промежуточный обмен нуклеиновых кислот (распад нуклеиновых кислот в тканях)
- •14.3. Биосинтез нуклеиновых кислот
- •14.4. Рекомбинантные молекулы и проблемы генной
- •15. Обмен воды и солей
- •15.1. Содержание и роль воды в организме
- •15.2. Электролиты тканей
- •15.3. Потребность организма в минеральных веществах, их поступление и выделение
- •16. Взаимосвязь обмена белков, жиров и углеводов
- •17. Биохимия крови
- •18. Биохимия нервной ткани
- •18.1. Химический состав нервной ткани
- •18.2. Обмен веществ в нервной ткани
- •18.3. Химизм передачи нервного импульса
- •19. Биохимия мышечной ткани
- •19.1. Морфология и биохимический состав мышечной ткани
- •19.2. Механизм сокращения мышцы
- •19.3. Окоченение мышц
- •20. Биохимия молока и молокообразования
- •21. Биохимия почек и мочи
- •22. Биохимия кожи и шерсти
- •23. Биохимия яйца
- •Приложение
2.2. Поверхностные явления
Поверхностные явления в коллоидах играют первостепенную роль, так как, являясь микрогетерогенными системами, коллоиды характеризуются колоссальной поверхностью раздела между частицами дисперсной фазы и дисперсионной среды. Наличие сильно развитой поверхности в коллоидных растворах объясняет многие физико-химические особенности этих систем. Поэтому можно сказать, что коллоидная химия — это физическая химия дисперсных систем и поверхностных явлений.
2.3. Адсорбция
Концентрирование вещества, равномерно распределенного в одной из фаз дисперсной системы, на границе раздела фаз называется адсорбцией.
Адсорбция обусловлена наличием адсорбционных сил, имеющих различную природу. Различают межмолекулярные (ван-дер-ваальсовы) и химические (ионные, ковалентные) силы.
Иногда адсорбция, начавшись на поверхности, распространяется вглубь частицы. Такой процесс называют абсорбцией; если такое поглощение сопровождается химическим взаимодействием, то процесс носит название хемосорбции.
Вещество, способное адсорбировать на своей поверхности другое вещество или ионы, называется адсорбентом. Адсорбируемое нещество называется адсорбтивом.
Явления адсорбции, абсорбции и хемосорбции объединены общим понятием сорбции.
Процесс адсорбции обратим. Частицы в адсорбционных слоях совершают колебательные движения, то приближаясь к адсорбенту, то удаляясь от него. Некоторые из них могут выходить за пределы действия сил притяжения адсорбента. В этом случае наблюдается обратный процесс — десорбция.
Со временем система приходит в состояние адсорбционного равновесия:
Адсорбция![]() Десорбция.
Десорбция.
Адсорбция носит избирательный характер. Так, например, активированный уголь хорошо поглощает хлор, но не адсорбирует оксид углерода.
Процесс адсорбции экзотермичен и, следовательно, в соответствии с принципом Ле-Шателье, с повышением температуры адсорбция уменьшается и равновесие сдвигается в сторону процесса десорбции.
Все растворимые вещества по их способности адсорбироваться на границе раздела фаз делятся на две группы: поверхностно-активные (ПАВ) вещества и поверхностно-неактивные. Характерной особенностью ПАВ является то, что молекулы их содержат дне части: полярную гидрофильную (растворимую в воде) и неполярную гидрофобную (в воде нерастворимую). При растворении таких веществ в воде они погружают свои гидрофильные группы в моду, а гидрофобная часть располагается выше уровня воды, т. е. как бы торчит из воды (рис. 2.1).
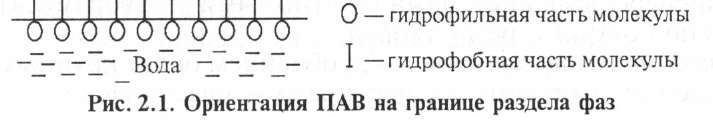
Если же поверхностно-активное вещество равномерно распределено в одной из двух несмешивающихся жидкостей, то оно концентрируется на границе раздела этих двух фаз (рис. 2.2).
Обычно углеводородный радикал гидрофобный, а функциональные группы —ОН, —СООН, —NH2 и т. д. — гидрофильные. Чем длиннее углеводородный радикал, тем меньше растворимость его в воде, но тем выше становится его способность к адсорбции. Эта закономерность получила название правила Трау- бе—Дюкло. Это правило применимо к разбавленным растворам.
Процессы адсорбции происходят и в живых организмах. Роль твердого тела играют мембраны и коллоидные частицы. Так, вещества, образующиеся после переваривания в желудочно-кишечном тракте белков, углеводов и т. д. (это соответственно аминокислоты, глюкоза и т. д.), попадают в кровь и адсорбируются из крови на внешней мембране клеток. Только после этого процесса клетка поглощает эти питательные вещества (служащие либо источником энергии, либо строительным материалом клеток).
Одно из главных свойств адсорбции — ее избирательность. На способности адсорбентов избирательно поглощать растворенные вещества основаны хроматографические методы анализа, позволяющие разделять сложные смеси на отдельные фракции. Впервые этот метод использовал русский ботаник М. С. Цвет (1903) для разделения зеленого вещества растений — хлорофилла — на составные части. Хроматографию широко применяют при разделении и очистке лекарственных веществ, витаминов, аминокислот, ионов, углеводородов нефтяных фракций и др.
В последние годы широкое распространение получили методы ионообменной хроматографии.
