
- •I. Физколлоидная химия
- •1. Физическая химия
- •1.1. Вода
- •1.1.1. Вода как уникальная молекула жизни
- •1.1.3. Буферные растворы
- •1.2. Биоэнергетика клетки
- •1.3. Термохимия
- •1.4. Химическая кинетика и катализ
- •2. Коллоидная химия
- •2.1. Классификация дисперсных систем
- •2.2. Классификация дисперсных систем по агрегатному состоянию дисперсной фазы
- •2.2. Поверхностные явления
- •2.3. Адсорбция
- •2.4. Коллоидные растворы (золи)
- •2.4.1. Характеристика коллоидных растворов
- •2.4.2. Растворы высокомолекулярных соединений
- •II. Биологическая химия
- •3. Белки
- •3.1. Общая характеристика белков
- •3.3. Методы выделения, фракционирования и очистки белков
- •3.3.1. Методы выделения белков
- •3.4. Физико-химические свойства белков
- •3.5. Аминокислоты
- •3.6. Структура белковой молекулы
- •I'm 1.8. Денатурация и ренатурация рибонукле- азы (по Анфинсену):
- •3.7. Классификация белков
- •3.7.1. Простые белки
- •3.7.2. Сложные белки
- •4. Нуклеиновые кислоты
- •4.1. Общая характеристика нуклеиновых кислот
- •4.2. Нуклеотиды и нуклеозиды
- •4.3. Дезоксирибонуклеиновая кислота
- •4.4. Рибонуклеиновые кислоты
- •5. Углеводы 5.1. Общая характеристика углеводов
- •5.2. Моносахариды
- •5.3. Олигосахариды
- •5.4. Полисахариды (глюканы)
- •6. Липиды
- •6.1. Общая характеристика липидов
- •6.2. Простые липиды
- •6.3. Сложные липиды
- •6.4. Двойной липидный слой клеточных мембран
- •Контрольные вопросы и задания
- •7. Витамины
- •7.1. Общая характеристика витаминов
- •7.2. Классификация и номенклатура витаминов
- •7.2.1. Жирорастворимые витамины
- •7.2.2. Водорастворимые витамины
- •8. Ферменты 8.1. Общая характеристика ферментов
- •8.3. Общие свойства ферментов
- •8.4. Активирование и ингибирование ферментов
- •8.2. Участие ионов металлов в активировании ферментов
- •8.5. Классификация и номенклатура ферментов
- •III класс. Гидролазы. Они разрывают внутримолекулярные связи путем присоединения
- •8.6. Применение ферментов
- •9. Гормоны
- •9.1. Уровни регуляции гормонов
- •9.2. Гормоны, выделяемые железами внутренней секреции
- •9.3. Гормоны местного действия
- •11. Обмен углеводов
- •11.1. Переваривание углеводов в пищеварительном тракте
- •11.2. Катаболизм глюкозы
- •11.3. Цикл трикарбоновых кислот
- •11.4. Пентозофосфатный путь окисления глюкозо-6-фосфата
- •11.5. Биосинтез углеводов
- •11.6. Регуляция обмена углеводов
- •12. Обмен липидов
- •12.1. Переваривание липидов в пищеварительном тракте
- •12.2. Промежуточный обмен липидов
- •2. Если синтезируется много сн3—со—КоА, а энергии для синтеза жира недостаточно, то образуется активированная ацетоуксусная кислота:
- •12.3. Биосинтез липидов
- •12.4. Метаболизм стеринов и стеридов
- •13. Обмен белков
- •13.2. Биологическая ценность белков
- •13.3. Особенности переваривания белков у моногастричных животных
- •13.4. Особенности переваривания белков у жвачных
- •13.5. Метаболизм белков в тканях
- •13.6. Особенности обмена отдельных аминокислот
- •13.7. Биосинтез белка
- •14. Обмен нуклеиновых кислот
- •14.1. Переваривание нуклеиновых кислот в пищеварительном тракте
- •14.2. Промежуточный обмен нуклеиновых кислот (распад нуклеиновых кислот в тканях)
- •14.3. Биосинтез нуклеиновых кислот
- •14.4. Рекомбинантные молекулы и проблемы генной
- •15. Обмен воды и солей
- •15.1. Содержание и роль воды в организме
- •15.2. Электролиты тканей
- •15.3. Потребность организма в минеральных веществах, их поступление и выделение
- •16. Взаимосвязь обмена белков, жиров и углеводов
- •17. Биохимия крови
- •18. Биохимия нервной ткани
- •18.1. Химический состав нервной ткани
- •18.2. Обмен веществ в нервной ткани
- •18.3. Химизм передачи нервного импульса
- •19. Биохимия мышечной ткани
- •19.1. Морфология и биохимический состав мышечной ткани
- •19.2. Механизм сокращения мышцы
- •19.3. Окоченение мышц
- •20. Биохимия молока и молокообразования
- •21. Биохимия почек и мочи
- •22. Биохимия кожи и шерсти
- •23. Биохимия яйца
- •Приложение
8.5. Классификация и номенклатура ферментов
Рациональная номенклатура ферментов составлена путем прибавления к латинскому корню названия субстрата, на который действует фермент, или к названию процесса, катализируемого ферментом, окончания «-аза».
Например, фермент, воздействующий на крахмал (amylum), называется амилаза; на мочевину (urea) — уреаза; на фенолы — фенолаза и т. д.
Кроме рационального названия сохранились ранее появившиеся термины: «пепсин», «трипсин».
В 1961 г. принята новая международная классификация, в основу которой принят тип катализируемой реакции. В настоящее время известно около 3000 различных ферментов. Классификацию проводят по типу их действия. Различают шесть классов ферментов:
оксидоредуктазы — окислительно-восстановительные ферменты; катализируют биологическое окисление;
трансферазы — катализируют реакции переноса различных химических групп от одной молекулы (донора) к другой молекуле (акцептору);
гидролазы — осуществляют химические превращения веществ с участием молекулы воды;
л и а з ы — отщепляют от субстратов ту или иную группу негидролитическим путем;
изомеразы — осуществляют изомерные превращения соединений;
лигазы (синтетазы) — катализируют реакции синтеза, сопровождающиеся отщеплением фосфорной кислоты от АТФ или другого трифосфата.
I класс. Оксидоредуктазы. Это ферменты окислительно-восста- новительных реакций, лежащих в основе биологического окисления. Название ферментов составлено по следующей форме: название субстрата (донора), от которого отщепляются атомы водорода (электроны) + название акцептора, на который переносятся атомы водорода + термин «оксидоредуктаза», например лактат: НАД- оксидоредуктаза.
Различают следующие подклассы оксиредуктаз: аэробные дегидрогеназы, анаэробные дегидрогеназы, электронтранспортазы, пероксидаза и каталаза.
Аэробные дегидрогеназы переносят электроны и протоны водорода с окисляемого субстрата на кислород:

К ним относятся ферменты оксидазы.
Анаэробные дегидрогеназы переносят электроны и протоны водорода с окисляемого субстрата на другой субстрат. К ним относятся пиридинзависимые и флавинзависимые дегидрогеназы.
Например, окисление молочной кислоты происходит под действием лактатдегидрогеназы, при этом НАД восстанавливается в НАДН2:
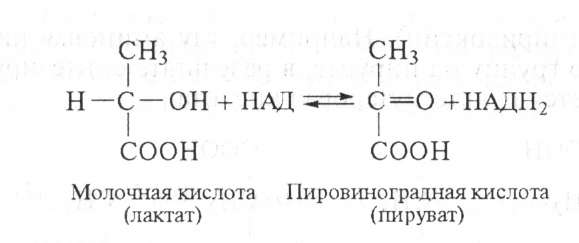
Окисление янтарной кислоты происходит под действием сук- цинатдегидрогеназы, при этом ФАД восстанавливается в ФАДН2:
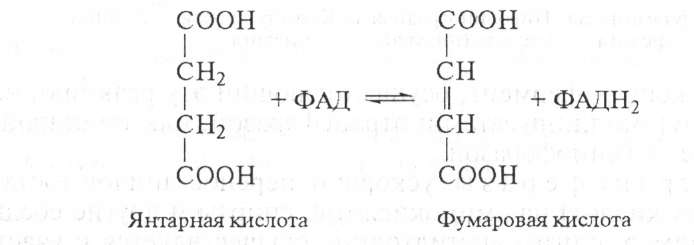
Электронтранспортазы — переносчики электронов. К ним относятся цитохромные ферменты, цитохромоксидазы дыхательной цепи митохондрий.
Пероксидаза и каталаза: пероксидаза катализирует окисление субстрата пероксидом водорода. Например, под действием пероксидазы сероводород окисляется с участием перокси- да водорода:
![]()
Каталаза в организме животных разрушает пероксид водорода на воду и молекулярный кислород:
![]()
Каталаза обезвреживает действие пероксида и служит источником молекулярного кислорода в тканях.
II класс. Трансферазы. Катализируют реакции переноса атомов и групп атомов, включают следующие подклассы: аминоферазы, ацилтрансферазы, фосфотрансферазы, метилферазы, глюкозил- трансферазы, алкилтрансферазы.
Глутаминовая
Пировиноградная а-Кетоглутаровая
Алании кислота кислота(пируват) кислота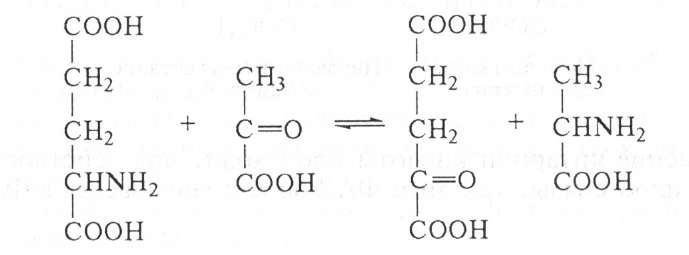
Пиридоксин — фермент, осуществляющий эту реакцию, называется 1-глутамил:пируватаминотрансферазой, или по старой номенклатуре — аминоферазой.
Ацилтрансферазы ускоряют перенос ацилов (остатков карбоновых кислот) на аминокислоты, спирты и другие соединения. Например, синтез ацетилхолина осуществляется с участием фермента холинацетилтрансферазы:
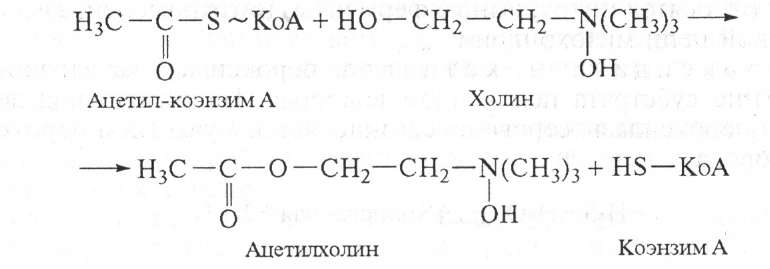
Фосфотрансферазы — ферменты, ускоряющие реакцию переноса остатка фосфорной кислоты. Донором фосфатных остатков чаще всего служит АТФ. Например, гексокиназа ускоряет перенос остатка фосфорной кислоты на глюкозу:
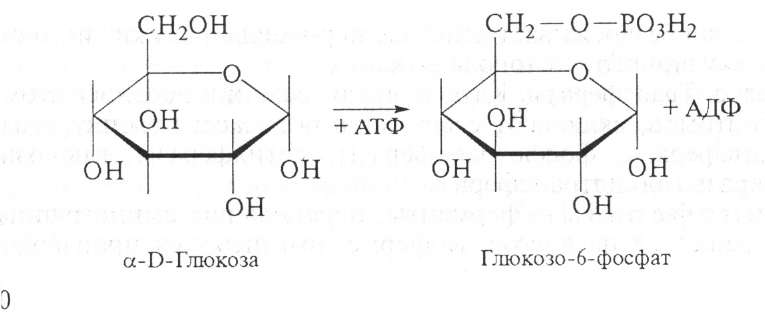
Метилферазы — ферменты, переносящие метальную группу с одного соединения на другое. Например, при синтезе креатина донором метальной группы служит метионин.
