
- •Орловский государственный технический университет
- •302030, Г. Орел, ул. Московская, 65.
- •Содержание
- •Введение
- •Лабораторная работа №1 Методы определения восстанавливающих сахаров
- •Общие сведения
- •Практическая часть
- •1.3.1 Опыт 1. Определение глюкозы в растительном сыре по Фелингу
- •1.3.1.1 Методика выполнения работы:
- •1.3.1.2 Оформление работы
- •1.3.2 Опыт 2. Рефрактометрическое определение молочного сахара
- •1.3.2.1 Методика выполнения работы
- •1.3.2.2 Оформление работы
- •1.4 Контрольные вопросы
- •Лабораторная работа №2 Определение содержания крахмала в зерне
- •2.2 Общие сведения
- •2.3.2.1 Методика выполнения работы
- •2.3.2.2 Оформление работы
- •2.4 Контрольные вопросы
- •Лабораторная работа №3 Выделение растворимого пектина и определение количества пектина по пектату кальция
- •3.2 Общие сведения
- •3.3 Практическая часть
- •3.3.1 Методика выполнения работы
- •3.3.2 Оформление работы
- •3.4 Контрольные вопросы
- •Лабораторная работа №4 Определение качественных показателей жира
- •4.2 Общие сведения
- •4.3 Практическая часть
- •4.3.1 Опыт 1. Определение показателя преломления масла
- •4.3.1.1 Методика выполнения работы
- •4.3.1.2 Оформление работы
- •4.3.2 Опыт 2. Определение перекисного числа жира
- •4.3.2.1 Методика выполнения работы
- •4.3.2.2 Оформление результатов
- •4.3.3 Опыт 3. Определение содержания жира в пищевых продуктах рефрактометрическим методом
- •4.3.3.1 Методика выполнения работы
- •4.3.3.2 Оформление результатов
- •4.4 Контрольные вопросы
- •Лабораторная работа № 5 Изучение физико-химических свойств белков
- •5.2. Общие сведения
- •5.3 Практическая часть
- •5.3.1 Опыт 1. Цветные реакции на белки
- •Биуретовая реакция (реакция Пиотровского)
- •Окрашенный биуретовый комплекс
- •Ксантопротеиновая реакция (реакция Мульдера)
- •5.3.1.1 Методика выполнения работы
- •5.3.1.2 Оформление результатов опыта
- •5.3.2 Опыт 2. Реакции осаждения белков
- •5.3.2.1 Методика выполнения работы
- •5.3.2.2 Оформление результатов опыта
- •5.3.3 Опыт 3. Определение изоэлектрической точки желатина
- •5.3.3.1 Методика выполнения работы
- •5.3.3.2 Оформление результатов опыта
- •5.4 Контрольные вопросы
- •Лабораторная работа №6 Методы количественного определения белка
- •6.2 Общие сведения
- •6.3 Практическая часть
- •6.3.1 Опыт 1. Определение белка по методу Лоури
- •6.3.1.1 Методика выполнения работы
- •6.3.1.2 Оформление результатов
- •6.3.2 Опыт 2. Определение содержания белков методом формольного титрования
- •6.3.2.1 Методика выполнения работы
- •6.3.2.2 Оформление результатов опыта
- •6.4 Контрольные вопросы
- •Лабораторная работа №7 Определение общего азота по Несслеру
- •7.2 Общие сведения
- •7.3 Практическая часть
- •Построение калибровочной кривой для определения аммонийного азота по Несслеру
- •7.3.2 Оформление результатов опыта
- •7.4 Контрольные вопросы
- •Лабораторная работа №8 Получение нуклеопротеида из дрожжей и его гидролиз
- •8.2 Общие сведения
- •8.3 Практическая часть
- •8.3.1 Методика выполнения работы
- •8.3.2 Оформление результатов опыта
- •8.4 Контрольные вопросы
- •Лабораторная работа №9 Определение активности гидролитических ферментов
- •9.2 Общие сведения
- •9.3 Практическая часть
- •9.3.1 Опыт 1. Определение амилазной активности слюны.
- •9.3.1.1 Методика выполнения работы
- •9.3.1.2 Оформление результатов опыта
- •9.3.2 Опыт 2. Определение активности β-фруктофуранозидазы
- •9.3.2.1 Методика выполнения работы
- •9.3.2.2 Оформление результатов опыта
- •9.4 Контрольные вопросы
- •Лабораторная работа №10 Определение активности каталазы
- •10.2 Общие сведения
- •10.3 Практическая часть
- •10.3.1 Опыт 1. Определение активности каталазы в свежем растительном материале.
- •10.3.1.1 Методика выполнения работы
- •10.3.1.2 Оформление результатов опыта
- •10.3.2 Опыт 2. Определение активности каталазы в масле
- •10.3.2.1 Методика выполнения работы
- •10.3.2.2 Оформление результатов опыта
- •10.4 Контрольные вопросы
- •Лабораторная работа №11 Определение активности дегидрогеназы
- •11.2 Общие сведения
- •11.3 Практическая часть
- •11.3.1 Опыт 1. Восстановление метиленовой сини дегидрогеназой дрожжей
- •11.3.1.1 Методика выполнения работы
- •11.3.1.2 Оформление результатов опыта
- •11.3.2 Опыт 2. Окисление формальдегида дегидрогеназой молока
- •11.3.2.1 Методика выполнения работы
- •11.3.2.2 Оформление результатов опыта
- •11.4 Контрольные вопросы
- •Лабораторная работа №12 Определение активности полифенолоксидазы
- •12.2 Общие сведения
- •12.3 Практическая часть
- •12.3.1 Опыт 1. Определение активности полифенолоксидазы
- •12.3.1.1 Методика выполнения работы
- •12.3.1.2 Оформление результатов опыта
- •12.3.2 Опыт 2. Ингибиторы полифенолоксидазы
- •12.3.2.1 Методика проведения работы
- •12.3.2.2 Оформление результатов опыта
- •12.4 Контрольные вопросы
- •Лабораторная работа №13 Определение содержания витамина с
- •13.2 Общие сведения
- •13.3 Практическая часть
- •13.3.2 Оформление результатов опыта
- •13.4 Контрольные вопросы
- •Лабораторная работа №14 Определение содержания β-каротина
- •14.2 Общие сведения
- •14.3 Практическая часть Калориметрический метод определения содержания β -каротина
- •14.3.1 Методика выполнения работы
- •14.3.2 Оформление результатов опыта
- •14.4 Контрольные вопросы
- •Лабораторная работа №15 Определение витаминов а и е методом оф вжх
- •15.2 Общие сведения
- •15.3 Практическая часть
- •15.3.1 Методика выполнения работы
- •15.3.2 Оформление результатов опыта
- •15.4 Контрольные вопросы
- •Лабораторная работа №16 Определение содержания минеральных веществ
- •16.2 Общие сведения
- •16.3 Практическая часть
- •16.3.1 Опыт 1. Определение фосфора
- •16.3.1.1 Методика выполнения работы
- •16.3.1.2 Оформление результатов опыта
- •16.3.2 Опыт 2. Определение кальция комплексонометрическим методом
- •16.3.2.1 Методика выполнения работы
- •16.3.2.2 Оформление результатов опыта
- •16.4 Контрольные вопросы
- •Лабораторная работа №17 Исследование продуктов, выделяемых дрожжами при спиртовом брожении
- •17.2 Общие сведения
- •17.3 Практическая часть
- •17.3 Методика выполнения работы
- •17.3.2 Оформление результатов опыта
- •17.4 Контрольные вопросы
- •Литература
Практическая часть
1.3.1 Опыт 1. Определение глюкозы в растительном сыре по Фелингу
В основе метода лежит реакция Троммера, то есть способность солей меди(II) в определенных условиях количественно окислять глюкозу.
В реакции Троммера происходит образование как альдоновых кислот, так и гидроксида меди(II), что указывает на отсутствие количественной связи между глюкозой и гемиоксидом меди. Однако, если к реакционной смеси добавить сегнетову соль, то образуется комплекс, в котором медь реагирует с глюкозой в стехиометрическом соотношении:
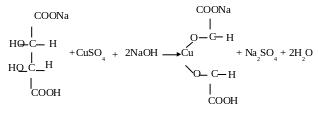

Количество закиси меди (Сu2O), эквивалентное окисленной глюкозе, определяется йодометрическим методом:
C u2O
+I2
CuO + CuI2
u2O
+I2
CuO + CuI2
Эта реакция в присутствии солей щавелевой или винной кислот протекает практически до конца.
Избыточное количество йода, которое не прореагировало с гемиоксидом меди, можно определить титрованием тиосульфатом натрия (индикатор – раствор крахмала):
2 Na2S2O3 + I2 2NaI +Na2S4O6
Приборы и реактивы: мерные колбы на 500 мл; конические колбы на 250, 50 мл; стеклянные палочки; пипетки; водяная баня; бюретки для титрования; фарфоровая ступка с пестиком; воронка; фильтр; 0,2%-ный раствор глюкозы; реактив Фелинга (раствор I: 200 г сегнетовой соли и 150 г NaOH растворяют в 1 л дистиллированной воды; раствор II: 40 г перекристаллизованного сульфата меди растворяют в 1 л дистиллированной воды; перед работой растворы I и II смешивают); насыщенный раствор щавелевой кислоты; 0,05 М раствор йода; 0,05 М раствор тиосульфата натрия; 1%-ный раствор крахмала; мел; 30%-ный раствор сульфата цинка.
1.3.1.1 Методика выполнения работы:
25 г растительного сырья (овощей, фруктов) измельчают и тщательно растирают в фарфоровой ступке с дистиллированной водой, затем смесь переносят количественно водой в коническую колбу на 250 мл, заливают 150-200 мл горячей дистиллированной водой и нагревают 1 ч на водяной бане при 75-800 С. После охлаждения смесь переносят в мерную колбу на 500 мл, доводят до метки дистиллированной воды и фильтруют.
При анализе кислых продуктов (яблоки, лимоны, виноград и др.) органические кислоты могут разрушить сахар, поэтому перед нагреванием на бане в колбу добавляют мел.
При анализе продуктов, не имеющих кислую реакцию (морковь, капуста, картофель и др.), мел не добавляют.
Для осаждения примесей посторонних веществ (белков и др.) к фильтрату добавляют 1,5 мл 30%-ного раствора сульфата цинка (или 5 мл 10% раствора ацетата свинца, или 5 мл 4%-ного раствора фосфорномолибденовой кислоты). Смесь фильтруют.
В две колбы на 50 мл помещают 10 мл фелинговой жидкости. В одну из колб добавляют 10 мл исследуемого раствора, содержащего глюкозу, а в другую 10 мл дистиллированной воды. Содержимое обеих колб нагревают до кипения, кипятят 5 минут и охлаждают.
После этого в обе колбы наливают по 10 мл насыщенного раствора щавелевой кислоты, по 10 мл раствора йода и после перемешивания стеклянной палочкой отстаивают в течение 5 минут. Затем в обе колбы вносят по 5 капель раствора крахмала и титруют раствором тиосульфата до перехода образовавшейся темно-синей окраски в голубую.
Массовая концентрация глюкозы в исследуемом растворе расчитывается по формуле:
С=(В-А)*f*a*v0/v1
где С – массовая концентрация глюкозы, мг/мл;
А и В – объемы раствора тиосульфата натрия, затраченного на титрование пробы и контроля, мл;
f – коэффициент поправки на титр 0,05 М раствора тиосульфата натрия;
а – масса глюкозы (3,52 мг), эквивалентная 1мл 0,05 М раствора тиосульфата натрия;
v0 – общий объем пробы, мл;
v1 – объем исследуемого раствора, взятого для анализа, мл.
