
- •1. Фотометрический анализ (молекулярная абсорбционная спектроскопия). Теоретические основы
- •1.1. Методы фотометрического анализа
- •1.2. Основной закон светопоглощения (закон Бугера-Ламберта-Бера)
- •1.3. Спектр светопоглощения (спектральная характеристика вещества)
- •1.4. Отклонения от основного закона светопоглощения
- •1.5. Закон аддитивности светопоглощения
- •1.6. Качественный спектрофотометрический анализ
- •1.7. Количественный анализ по светопоглощению
- •1.7.1. Подчинение основному закону светопоглощения
- •1.7.2. Определение концентрации вещества в растворе с помощью градуировочного графика
- •1.7.3. Определение концентрации веществ в смеси
- •1.8. Приборы для измерения поглощения растворов. Принципиальные схемы и основные элементы
- •1.9. Спектрофотометрическое титрование
- •Необходимые реактивы и принадлежности
- •Порядок выполнения работы
- •Вопросы
- •Необходимые реактивы, приборы
- •Необходимые реактивы, приборы
- •Необходимые релжтиеы, приборы
- •Порядок работы на колориметре фотоэлектрическом; концентрационном кфк-2мп
- •Вопросы
- •Необходимые реактивы, приборы
- •Методика определения
- •Вопросы
- •Необходимые реактив, . Приборы
- •Методика онределения
- •Порядок работы на приборе лмф-69
- •Вопросы
- •2. Эмиссионный спектральный анализ
- •2.1. Теоретические основы эмиссионной спектроскопии
- •2.2. Качественный спектральный анализ
- •2.3. Количественный спектральный анализ
- •2.4. Источники возбужнения
- •2.5. Пламенная фотометрия
- •2.6. Применение эмиссионного спектрального анализа
- •Необходимые реактивы, приборы, посуда
- •Вопросы
- •3. Люминесцентный анализ
- •3.1.Теоретические основы метода
- •3.2. Спектры поглощения и спектры люминесценции
- •3.3. Энергетический и квантовый выходы люминесценции
- •3.4. Интенсивность люминесценции
- •3.5. Качественный анализ
- •3.6. Количественный анализ
- •3.7. Применение люминесцентного метода для анализа пищевых продуктов и с/х сырья
- •3.8. Аппаратура люминесцентного анализа
- •Аппаратура ы реактивы
- •Выполнение работы
- •Работа 2. Определение свободного и связанного витамина в2 в пищевых продуктах
- •Необходимые реактивы, приборы
- •Вопросы
- •4. Хроматография
- •4.1. Основные принципы и классификация хроматографических методов анализа
- •4.2. Характеристика хроматографических методов анализа
- •4.2.1. Адсорбционная хроматография (жидкостно-адсорбционная, жидкостная твердoфазная хроматография)
- •4.2.2. Ионообменная хроматоарафия (жидкостная твердофазная хроматография (жтх))
- •4.2.3. Распределительная хроматография (жидкость-жидкостная хроматография жжх))
- •4.2.4. Осадочная хроматография
- •4.2.5. Газовая хроматография
- •4.2.6. Жидкостная высокоскоростная (высокоэффективная) хроматография
- •4.2.7. Гель-хроматография
- •4.2.8. Молекулярный ситовой анализ
- •Вопросы
- •Вопросы
- •Работа 2. Определение углеводов методом тонкослойной хроматографии
- •Работа 3. Изучение свойств ионообменных смол
- •Работа 4. Концентрирование ионов меди (II) из разбавленных растворов методом ионообменной хроматографии
- •Необходимые реактивы, приборы
- •Работа 5. Отделение железа от меди и ее качественное определение
- •Работа 6. Определение никеля по величине зоны хроматограммы
- •Работа 7. Определение спиртов методом газо-жидкостной хроматографии на лабораторном хроматографе
- •Вопросы
- •Работа 8. Идентификация и количестенное определение веществ в газо-жидкостной хроматографии (гжх) по хроматограммам свидетелей и таблицам
- •Работа 9. Определение содержания влаги в спиртах методом внутреннего стандарта
- •Литература
4.2. Характеристика хроматографических методов анализа
4.2.1. Адсорбционная хроматография (жидкостно-адсорбционная, жидкостная твердoфазная хроматография)
Разделение компонентов смеси основано на их различной адсорбционной способности. Адсорбция - поглощение поверхностью твердого тела или поглощение на границе раздела жидкость-жидкость или жидкость-газ.
Общая скорость адсорбции складывается из скорости адсорбции и скорости десорбции. Каждая молекула или нон бссчисленное количество раз сорбируется и десорбируется, перемещаясь с потоком жидкости (или газа) в колонке.
При постоянной температуре адсорбция увеличивается с ростом концентрации раствора или давления газа. Зависимость количества поглощенного вещества от концентрация растора или давленая газа при постоянной температуре называют изотермой адсорбции. Типичная изотерма адсорбции приведена на рис. 4.5. Математически эта зависимость может быть выражсна уравнением Лэнгмюра:
![]()
где n - количество адсорбированного вещества при равновесии;
n∞ - максимальное количество вещества, которое может быть адсорбировано на данном адсорбенте ;
В - постоянная;
С - концентрация.
Такой вид изотермы адсорбции отвечает мономолекулярному слою, для полимолекулярного слоя она может быть вогнутой или S-образной.
В качестве адсорбентов применяют вещества с развитой поверхностью различной степени дисперсности или волокнистые (целлюлоза, вата). От величины зерен или волокон адсорбента и от плотности его упаковки зависит скорость фильтрации раствора через колонку.
Адсорбенты должны удовлетворять следующим требованиям:
- быть химически инертными к компонентам анализируемой смеси и растворителю;
- должны иметь достаточную адсорбционную способность и больлшую активную поверхность;
- должны быть однородными и не подвергаться дальнейшему диспергированию в колонке;
- должны быть стандартными, при отсутствии таковых должны готовиться по единой методике из одного и того же сырья (оксиды магния и алюминия, приготовленные по различныим методикам, обладают различной адсорбционной способностью).
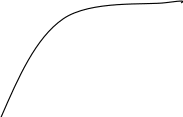
n
C
Рис. 4.4. Изотерма адсорбции
Очень ответственной операцией является заполнение хроматографической колонки адсорбенеом - зависит четкость разделения исследуемых компонентов, т.е. четкость полученных хроматограмм.
В адсорбционной хроматографии чаще всего используется проявительный (элюэнтный) анализ.
Наиболее распространенными адсорбентами являются: органические - сахароза, инулин, молочный сахар, целлюлоза, крахмал; неорганические - оксиды алюминия, кальция, цинка, магния, карбонат кальция, силикагель, активированный уголь, природные минералы - глины.
Растворители в адсорбционной хроматографии должны быть химически инертны как к растворяемому вещесгву, так и к адсорбенту. В качестве растворителей применяют воду, спирты, ацетон, эфиры, бензол, толуол и д.р.
Хроматограммы могут быть внутренними и внешними.
Внутренняя хроматограмма. Непосредственно на колонке можно проводить качественный и количественный анализ визуально по окраске зон адсорбента. Если зоны компонентов не окрашены, хроматограмму можно “проявить”. В качестве проявителя используют различные реагенты, образующие с сорбированными в колонке компонентами окрашенные соединения. В ряде случаев используют способность некоторых веществ люминесцировать под действием ультрафиолетовык лучей. для кодичественного анализа требуется иметь дополнительные хроматограммы растворов “свидетелей” с точно извесгной их концентрацией.
Внешняя хроматограмма. Качественный и количественный анализ может быть осуществлен непрерывным анализом вытекающего из колонки раствора или последовательным отбором отдельных фракпкй и их анализом (коллектор фракций).
