
- •1. Фотометрический анализ (молекулярная абсорбционная спектроскопия). Теоретические основы
- •1.1. Методы фотометрического анализа
- •1.2. Основной закон светопоглощения (закон Бугера-Ламберта-Бера)
- •1.3. Спектр светопоглощения (спектральная характеристика вещества)
- •1.4. Отклонения от основного закона светопоглощения
- •1.5. Закон аддитивности светопоглощения
- •1.6. Качественный спектрофотометрический анализ
- •1.7. Количественный анализ по светопоглощению
- •1.7.1. Подчинение основному закону светопоглощения
- •1.7.2. Определение концентрации вещества в растворе с помощью градуировочного графика
- •1.7.3. Определение концентрации веществ в смеси
- •1.8. Приборы для измерения поглощения растворов. Принципиальные схемы и основные элементы
- •1.9. Спектрофотометрическое титрование
- •Необходимые реактивы и принадлежности
- •Порядок выполнения работы
- •Вопросы
- •Необходимые реактивы, приборы
- •Необходимые реактивы, приборы
- •Необходимые релжтиеы, приборы
- •Порядок работы на колориметре фотоэлектрическом; концентрационном кфк-2мп
- •Вопросы
- •Необходимые реактивы, приборы
- •Методика определения
- •Вопросы
- •Необходимые реактив, . Приборы
- •Методика онределения
- •Порядок работы на приборе лмф-69
- •Вопросы
- •2. Эмиссионный спектральный анализ
- •2.1. Теоретические основы эмиссионной спектроскопии
- •2.2. Качественный спектральный анализ
- •2.3. Количественный спектральный анализ
- •2.4. Источники возбужнения
- •2.5. Пламенная фотометрия
- •2.6. Применение эмиссионного спектрального анализа
- •Необходимые реактивы, приборы, посуда
- •Вопросы
- •3. Люминесцентный анализ
- •3.1.Теоретические основы метода
- •3.2. Спектры поглощения и спектры люминесценции
- •3.3. Энергетический и квантовый выходы люминесценции
- •3.4. Интенсивность люминесценции
- •3.5. Качественный анализ
- •3.6. Количественный анализ
- •3.7. Применение люминесцентного метода для анализа пищевых продуктов и с/х сырья
- •3.8. Аппаратура люминесцентного анализа
- •Аппаратура ы реактивы
- •Выполнение работы
- •Работа 2. Определение свободного и связанного витамина в2 в пищевых продуктах
- •Необходимые реактивы, приборы
- •Вопросы
- •4. Хроматография
- •4.1. Основные принципы и классификация хроматографических методов анализа
- •4.2. Характеристика хроматографических методов анализа
- •4.2.1. Адсорбционная хроматография (жидкостно-адсорбционная, жидкостная твердoфазная хроматография)
- •4.2.2. Ионообменная хроматоарафия (жидкостная твердофазная хроматография (жтх))
- •4.2.3. Распределительная хроматография (жидкость-жидкостная хроматография жжх))
- •4.2.4. Осадочная хроматография
- •4.2.5. Газовая хроматография
- •4.2.6. Жидкостная высокоскоростная (высокоэффективная) хроматография
- •4.2.7. Гель-хроматография
- •4.2.8. Молекулярный ситовой анализ
- •Вопросы
- •Вопросы
- •Работа 2. Определение углеводов методом тонкослойной хроматографии
- •Работа 3. Изучение свойств ионообменных смол
- •Работа 4. Концентрирование ионов меди (II) из разбавленных растворов методом ионообменной хроматографии
- •Необходимые реактивы, приборы
- •Работа 5. Отделение железа от меди и ее качественное определение
- •Работа 6. Определение никеля по величине зоны хроматограммы
- •Работа 7. Определение спиртов методом газо-жидкостной хроматографии на лабораторном хроматографе
- •Вопросы
- •Работа 8. Идентификация и количестенное определение веществ в газо-жидкостной хроматографии (гжх) по хроматограммам свидетелей и таблицам
- •Работа 9. Определение содержания влаги в спиртах методом внутреннего стандарта
- •Литература
Работа 2. Определение свободного и связанного витамина в2 в пищевых продуктах
В настоящее время известно З формы, в которых витамин В2 (рибофлавин) присутствует в природных источниках: свободный рибофлавин и его нуклеотидные формы в виде фосфорнокислых эфиров, связанных с белком (флавин - мононуклеотид, флавин - аденин - динуклеотид).
Современные методы определения рибофлавина основаны на его способности флуоресцировать. Связанные с белком формы не флуоресцируют. Согласно литературным данным для освобождения рибофлавина из его динуклеотида и для разрыва связи с белком применяют кислотный гидролиз с последующей обработкой ферментными препаратами или трихлоруксусной кислотой (ССI3СООН).
Необходимые реактивы, приборы
Флуориметр ЭФ-ЗМА или другой марки
.Рибофлавин, чда.
Гидрокарбонат натрия NaHCO3.
Тиосульфат натрия Na2S2O3.
Серная кислота, 0,5 М раствор.
Гидроксид натрия, 40 % раствор.
Трихлоруксусная кислота, 20 % раствор.
Универсальная индикаторная бумага.
Мерные колбы вместимостью 100 мл - З шт.
Конические колбы вместимостью 100 мл - 2 шт.
Складчатый фильтр.
Воронка диаметром 5-7 см.
Водяная баня.
Ход определения
На аналитических весах отбирают пробу измельченного комбикорма (5,0000 г), переносят в мерную колбу, добавляют 50 мл 0.5 М серной кислоты и кипятят 30 мин на водяной бане. Объем жидкости доводят горячей дистиллированной водой до метки и фильтруют через складчатый фильтр в коническую колбу. Мерную колбу (на 100 мл) ополаскивают 3,5 мл дистиллированной воды и переносят жидкость на тот же фильтр. Фильтрат перемешивают, отбирают 30 мл в коническую колбу, добавляют 30 мл раствора трихлоруксусной кислоты, кипятят 10 мин на водной бане.
Колбу охлаждают струей водопроводной воды, доводят рН жидкости до 4,0-4,5 добавлением 40 %-ного раствора гидроксида натрия, значение рН контролируют с помощью универсальной индикаторной бумаги. Жидкость вновь фильтруют. Фильтрат переносят в кювету флуориметра и снимают показания прибора. флуоресценцию исследуемого раствора сравнивают с флуоресценцией стандартного раствора витамина В2 (см. приготовление стандартного раствора в работе 1). Стрелку прибора устанавливают на 60 делений. После измерения флуоресценции в каждую кювету к стандартному и анализируемому растворам добавляют по 0,1 г гидрокарбоната и тиосульфата натрия для тушения люминесценции и снова измеряют интенсивность флуоресценции. При этом флуоресценция стандартного раствора полностью исчезает, в анализируемом растворе остается слабая флуоресценция, обусловленная примесями; интенсивность флуоресценции примесей учитывают при вычислениях.
Содержание рибофлавина в комбикормах (м, г/т) рассчитывают по формуле:
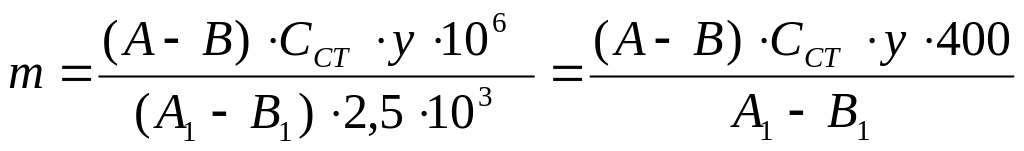 ,
,
где А и В - показания флуориметра для исследуемого раствора до и после тушения флуоресценции;
А1 иВ1 - показания флуориметра для стандартного раствора до и после тушения флуоресценции;
106 - коэффициент пересчета на 1 т продукта
2,5 - 0,5 пробы анализируемого продукта;
103 - коэффициент пересчета миллиграммовых количеств рибофлавина на граммы;
Сст - концентрация стандартного раствора, мг/мл;
у - вместимость мерной колбы, мл.
