
- •Глава 1 общие вопросы аэрогазодинамики
- •Аэродинамика и ее задачи
- •Исторический экскурс
- •Основные методы и постулаты аэрогазодинамики
- •Гипотеза сплошности среды. Идеальная и реальная жидкости
- •Уравнение состояния
- •Основные свойства жидкостей и газов
- •Сжимаемость
- •Влияние температуры на вязкость
- •Коэффициенты теплопроводности некоторых веществ
- •Параметры состояния газа
- •Критерии вязкости и сжимаемости
- •Полная аэродинамическая сила и момент
- •Системы координат, применяющиеся в аэродинамике
- •Компоненты аэродинамической силы и момента в связанной и скоростной системах координат. Угол атаки и угол скольжения
- •Международная стандартная атмосфера
- •Контрольные вопросы и задания
Коэффициенты теплопроводности некоторых веществ
Вещество |
, Вт/м/К |
Вещество |
, Вт/м/К |
Серебро |
458 |
Кирпич изоляционный |
0,14 |
Медь |
384 |
Асбест листовой |
0,12 |
Алюминий |
204 |
Шлаковая вата |
0,07 |
Латунь |
85 |
Аммиак |
0,570 |
Чугун |
63 |
Вода |
0,547 |
Накипь котельная |
1,3…3,1 |
Воздух |
0,024 |
Бетон |
1,28 |
Углекислый газ |
0,017 |
К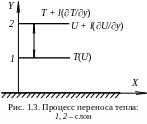 оэффициент
,
как и
,
зависит от вида газа и температуры. При
увеличении температуры
растет. При высоких температурах
коэффициент теплопроводности реального
газа
оэффициент
,
как и
,
зависит от вида газа и температуры. При
увеличении температуры
растет. При высоких температурах
коэффициент теплопроводности реального
газа
![]() .
.
Рассмотрим
процесс переноса тепла с точки зрения
молекулярно-кинети-ческой теории (рис.
1.3). Количество тепла, переносимое
единицей массы, равно
![]() ,
где U
– внутренняя энергия единицы массы
газа.
,
где U
– внутренняя энергия единицы массы
газа.
Масса
молекул, пересекающих при своем движении
поверхность с единичной площадью, равна
![]() ,
где
,
где
![]() – собственная скорость молекул, т. е.
через единичную площадку в единицу
времени переносится энергия (количество
тепла), равная
– собственная скорость молекул, т. е.
через единичную площадку в единицу
времени переносится энергия (количество
тепла), равная
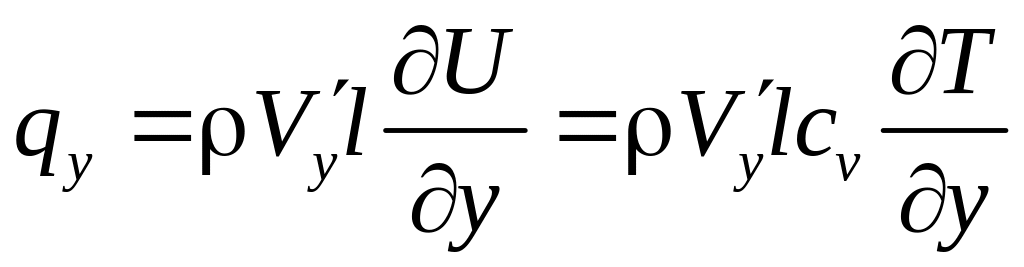 ,
(1.6)
,
(1.6)
так
как
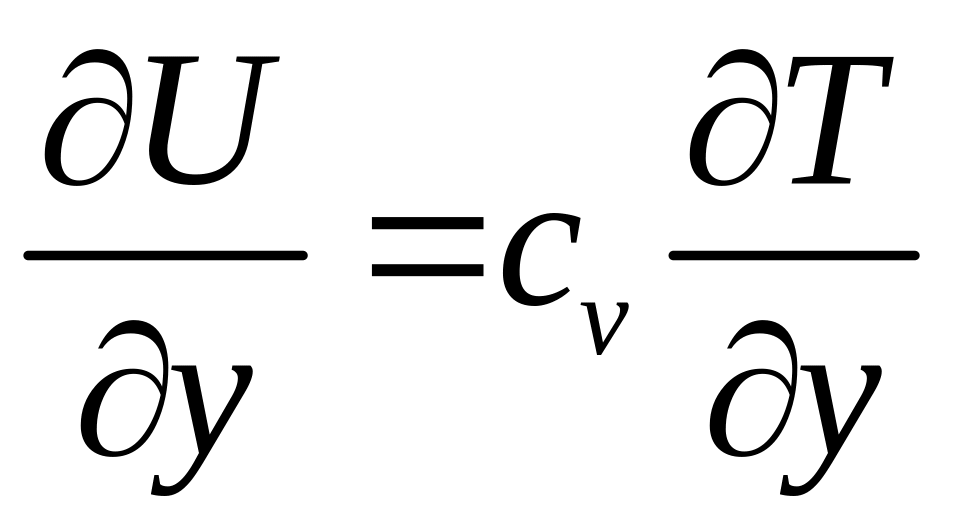 .
Сравнивая формулы (1.5) и (1.6), можно сделать
вывод, что
.
Сравнивая формулы (1.5) и (1.6), можно сделать
вывод, что
![]() .
Таким образом, коэффициент
пропорционален скорости хаотического
движения молекул, являющейся функцией
температуры газа, поэтому
.
Таким образом, коэффициент
пропорционален скорости хаотического
движения молекул, являющейся функцией
температуры газа, поэтому
![]() .
.
При температурах до 2 000 К коэффициент теплопроводности можно определить через коэффициент динамической вязкости по следующей формуле:
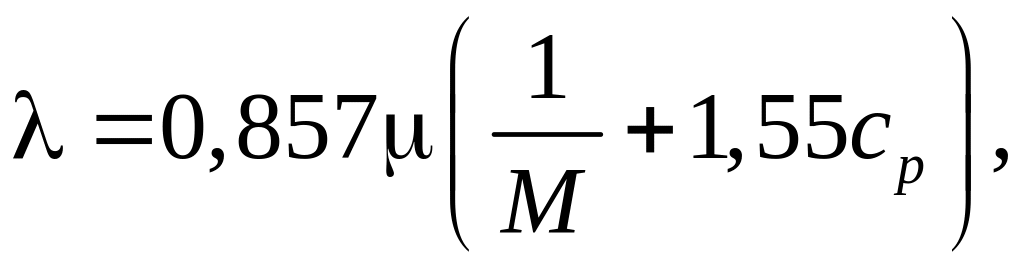
где
![]() – молекулярный вес данного сорта газа.
– молекулярный вес данного сорта газа.
Параметры состояния газа
Вспомним
объединенный газовый закон
![]() (
(![]() ),
или уравнение Менделеева–Клапейрона
– уравнение состояния идеального газа:
),
или уравнение Менделеева–Клапейрона
– уравнение состояния идеального газа:
![]() или
или
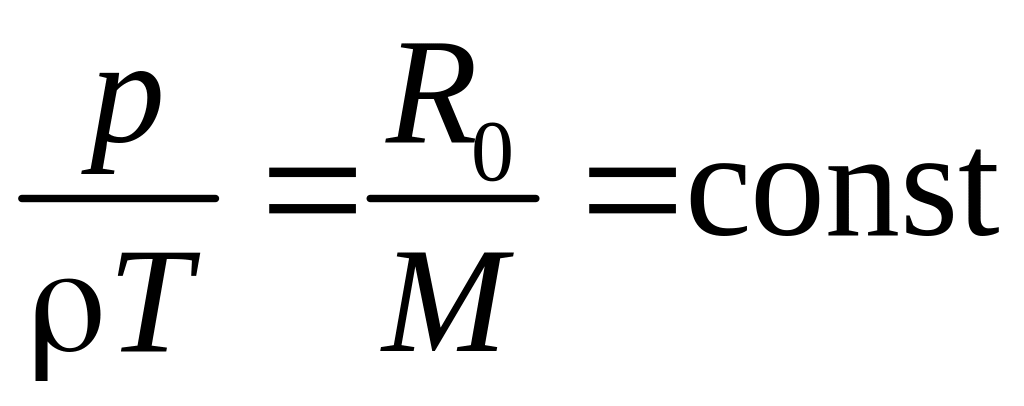 .
.
Важнейшими
характеристиками состояния газа являются
давление
,
плотность
и температура
![]() .
.
В общем случае при движении газа эти параметры меняются при переходе от точки к точке и зависят от времени. Для термодинамически совершенного газа , , связаны указанным уравнением Клапейрона. Во многих реальных практических случаях эта связь выражается более сложно. Для реальных газов нельзя пренебрегать собственным объемом молекул и силами взаимодействия между ними. Эти факторы сказываются тем сильнее, чем выше давление.
Таким образом, для неустановившегося движения параметры состояния газа являются функциями координат и времени:
![]() ,
,
![]() ,
,
![]()
Давление. Если скорость движения жидкости V = 0, то касательные напряжения отсутствуют и в жидкости имеются только напряжения сжатия – аэродинамическое давление.
Выделим
в жидкости бесконечно малый тетраэдр
(рис. 1.4), в котором
![]() есть плоскости граней тетраэдра,
перпендикулярных к осям
есть плоскости граней тетраэдра,
перпендикулярных к осям
![]()
![]() – давление на этих гранях;
– давление на этих гранях;
![]() и
и
![]() – давление и плоскость наклонной грани,
взятой произвольно.
– давление и плоскость наклонной грани,
взятой произвольно.
С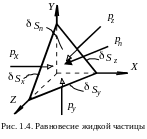 илы,
действующие на рассматриваемый объем
жидкости, разделяются на поверхностные
– силы давления на грани
илы,
действующие на рассматриваемый объем
жидкости, разделяются на поверхностные
– силы давления на грани
![]() и объемные – массовая сила
и объемные – массовая сила
![]() .
.
Так
как объем тетраэдра
![]() есть
величина третьего порядка малости, а
есть
величина третьего порядка малости, а
![]() – второго порядка, то при стягивании
тетраэдра в точку массовой силой можно
пренебречь.
– второго порядка, то при стягивании
тетраэдра в точку массовой силой можно
пренебречь.
Уравнение
равновесия тетраэдра в проекции на ось
ОX
запишется
как
![]() ,
или
,
или
![]() .
Поскольку
.
Поскольку
![]() ,
то
,
то
![]() .
Аналогичные результаты получаются для
проекций на оси OY
и OZ.
.
Аналогичные результаты получаются для
проекций на оси OY
и OZ.
Следовательно,
так как координатные плоскости выбраны
произвольно, то
![]()
Д авление
в любой точке покоящейся жидкости
остается постоянным для всех площадок,
проходящих через эту точку, т. е. не
зависит от ориентации площадки, на
которую оно действует.
авление
в любой точке покоящейся жидкости
остается постоянным для всех площадок,
проходящих через эту точку, т. е. не
зависит от ориентации площадки, на
которую оно действует.
Единицы
измерения давления следующие: в системе
СИ 1 Па = 1
![]() ;
в технической системе 1 ат =
;
в технической системе 1 ат =
![]() Па.
Па.
Плотность.
Массовая плотность характеризует
распределение массы в среде. Для среды,
сплошь заполняющей пространство,
плотность есть функция координат точки.
Массовая плотность жидкости или газа
определяется как
![]() .
.
Для
прерывистой среды этот предел мог бы и
не существовать. При величине
,
сравнимой с молекулярными размерами,
непрерывное изменение
привело бы к прерывистому изменению
![]() .
Приняв гипотезу сплошности среды, можно
быть уверенным, что предел существует
всегда.
.
Приняв гипотезу сплошности среды, можно
быть уверенным, что предел существует
всегда.
Единица
измерения плотности –
![]() .
Например, при нормальных условиях (
.
Например, при нормальных условиях (![]() )
плотность воды равна
)
плотность воды равна
![]() а
плотность воздуха
а
плотность воздуха
![]() Для газов плотность является функцией
давления и температуры,
Для газов плотность является функцией
давления и температуры,
![]() ,
а для несжимаемых жидкостей
– только температуры,
,
а для несжимаемых жидкостей
– только температуры,
![]() .
.
Непосредственное
измерение плотности движущейся сжимаемой
среды затруднено, поэтому
обычно определяют косвенным путем. Так
для совершенных газов плотность
определяют с помощью уравнения
Менделеева–Клапейрона, для изотермических
процессов (![]() )
– по уравнению
)
– по уравнению
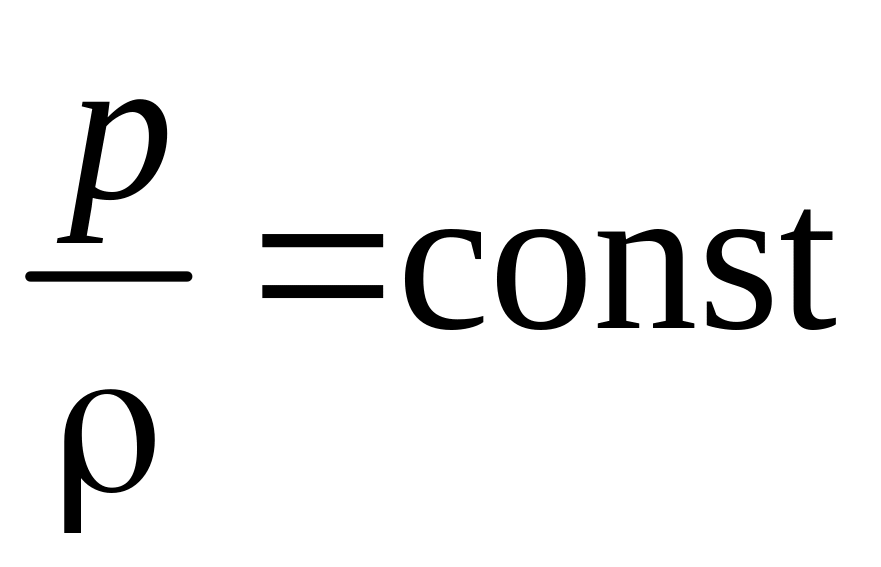 ,
для адиабатических процессов – по
уравнению
,
для адиабатических процессов – по
уравнению
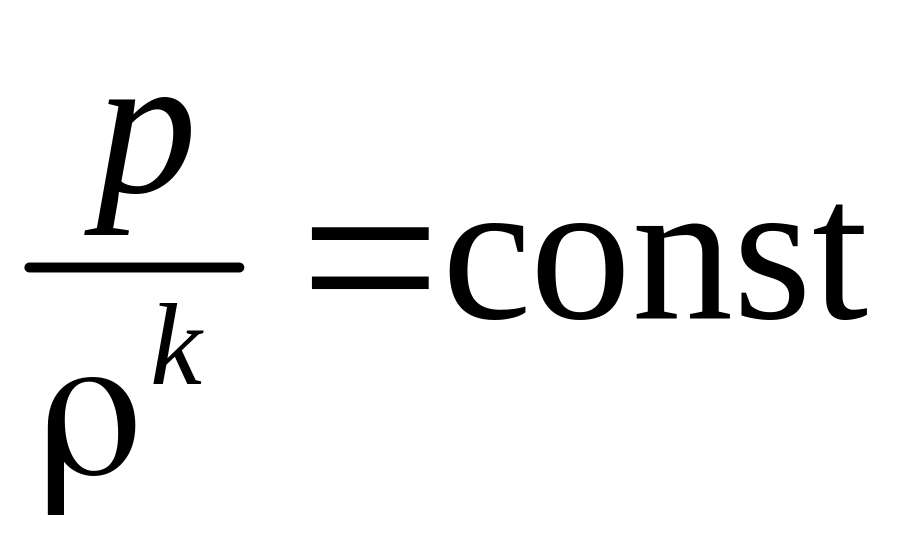 ,
где
,
где
![]() – показатель адиабаты, величина которого
зависит от молекулярного строения
данного сорта газа; для двухатомных
газов k
= 1,4.
– показатель адиабаты, величина которого
зависит от молекулярного строения
данного сорта газа; для двухатомных
газов k
= 1,4.
Температура. Температура есть мера внутренней энергии жидкости или газа и вообще любого тела. По величине температуры судят о степени нагретости, т. е. о тепловом состоянии тела. При наличии теплопроводности температура различных частей тела от точки к точке меняется непрерывно. Непрерывность изменения температуры возможна только в сплошных средах. Если же элементарный объем сравним с молекулярными размерами, то – прерывистая функция (в межмолекулярном объеме температура равна нулю). Поскольку скорость хаотического движения молекул зависит от температуры, то является мерой кинетической составляющей внутренней энергии.
Если
![]() ,
то мы имеем дело с неустановившимся
(нестационарным) полем температур, если
,
то мы имеем дело с неустановившимся
(нестационарным) полем температур, если
![]() ,
то поле температур стационарное
(установившееся).
,
то поле температур стационарное
(установившееся).
В
настоящее время на равных правах
существуют и применяются температурные
шкалы Цельсия и Кельвина. Единица
измерения температуры по шкале Цельсия
– градус
![]() ,
по шкале Кельвина – К (Кельвин). Переход
от шкалы Цельсия к шкале Кельвина
осуществляется следующим образом:
,
по шкале Кельвина – К (Кельвин). Переход
от шкалы Цельсия к шкале Кельвина
осуществляется следующим образом:
![]() (К).
(К).
