
- •Глава 1 общие вопросы аэрогазодинамики
- •Аэродинамика и ее задачи
- •Исторический экскурс
- •Основные методы и постулаты аэрогазодинамики
- •Гипотеза сплошности среды. Идеальная и реальная жидкости
- •Уравнение состояния
- •Основные свойства жидкостей и газов
- •Сжимаемость
- •Влияние температуры на вязкость
- •Коэффициенты теплопроводности некоторых веществ
- •Параметры состояния газа
- •Критерии вязкости и сжимаемости
- •Полная аэродинамическая сила и момент
- •Системы координат, применяющиеся в аэродинамике
- •Компоненты аэродинамической силы и момента в связанной и скоростной системах координат. Угол атаки и угол скольжения
- •Международная стандартная атмосфера
- •Контрольные вопросы и задания
Уравнение состояния
Уравнение состояния для несжимаемой жидкости имеет вид
![]() .
.
В реальной действительности все жидкости хотя и в малой мере, но сжимаемы, и уравнение состояния имеет более сложную форму. Для идеальных (термодинамически совершенных) газов уравнением состояния является уравнение Менделеева–Клапейрона:
![]()
или
уравнение Клапейрона
![]() ,
в котором
,
в котором
![]() – газовая постоянная для данного сорта
газа, где
– газовая постоянная для данного сорта
газа, где
![]() – универсальная газовая постоянная,
= 8,314 Дж/моль/К; М
–
молекулярная масса данного сорта газа,
кг/моль. Для смеси газов молекулярная
масса зависит от относительной
концентрации
– универсальная газовая постоянная,
= 8,314 Дж/моль/К; М
–
молекулярная масса данного сорта газа,
кг/моль. Для смеси газов молекулярная
масса зависит от относительной
концентрации
![]() отдельных компонентов.
отдельных компонентов.
Для реальных газов используют уравнения состояния, полученные или эмпирически, или теоретически, или на некоторых частных предположениях относительно внутренней структуры газа. Наиболее известно для реальных газов уравнение состояния Ван-дер-Ваальса:
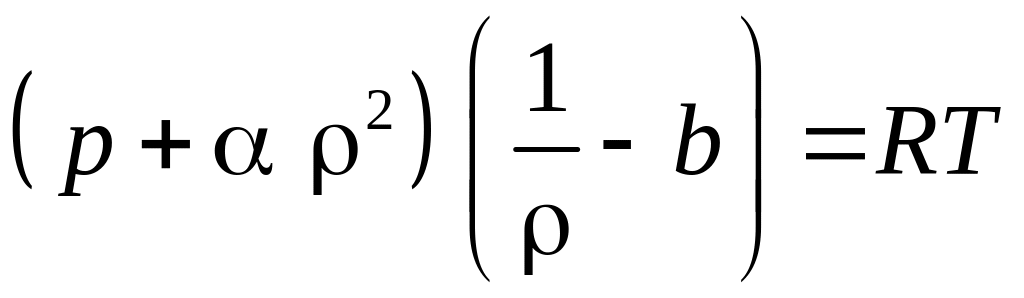 ,
,
где
коэффициент
![]() характеризует силы взаимодействия
между молекулами; b
– собственный объем молекул. Коэффициенты
и b
зависят от температуры.
характеризует силы взаимодействия
между молекулами; b
– собственный объем молекул. Коэффициенты
и b
зависят от температуры.
Для пара чаще всего используют уравнение состояния Молье:
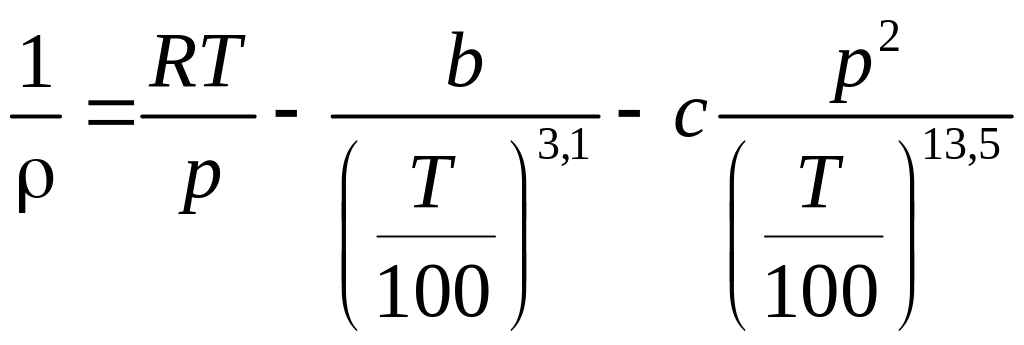 ,
,
где
b
и с
– постоянные. В зависимости от вида
уравнения состояния выражения для
внутренней энергии
![]() газа и его теплосодержания имеют разную
форму.
газа и его теплосодержания имеют разную
форму.
Основные свойства жидкостей и газов
Рассмотрим ряд общих для всех жидкостей и газов механических свойств, которые отличают их от твердых тел.
Механические связи между частицами жидкостей и газов весьма слабы, поэтому их частицы обладают очень большой подвижностью и в связи с этим текучестью – одним из основных свойств жидкостей и газов, о котором уже говорилось. Рассмотрим другие свойства.
Сжимаемость
Жидкости и газы способны в широких пределах деформироваться, изменяя не только свою форму, но и свой объем.
Способность жидкостей и газов изменять свой объем под действием сжимающих усилий называется сжимаемостью. Сжимаемость газов существенно выше, чем у жидкостей. Количественно оценить сжимаемость позволяет коэффициент сжимаемости.
Выделим
объем
![]() жидкости или газа. Пусть он находится
под давлением
жидкости или газа. Пусть он находится
под давлением
![]() .
Если изменить величину давления на
.
Если изменить величину давления на
![]() ,
то объем изменится на величину
,
то объем изменится на величину
![]() и относительное изменение объема
(объемная относительная деформация)
будет равно
и относительное изменение объема
(объемная относительная деформация)
будет равно
![]() .
Величину этой деформации, приходящейся
на единицу изменения давления, называют
коэффициентом
сжимаемости:
.
Величину этой деформации, приходящейся
на единицу изменения давления, называют
коэффициентом
сжимаемости:
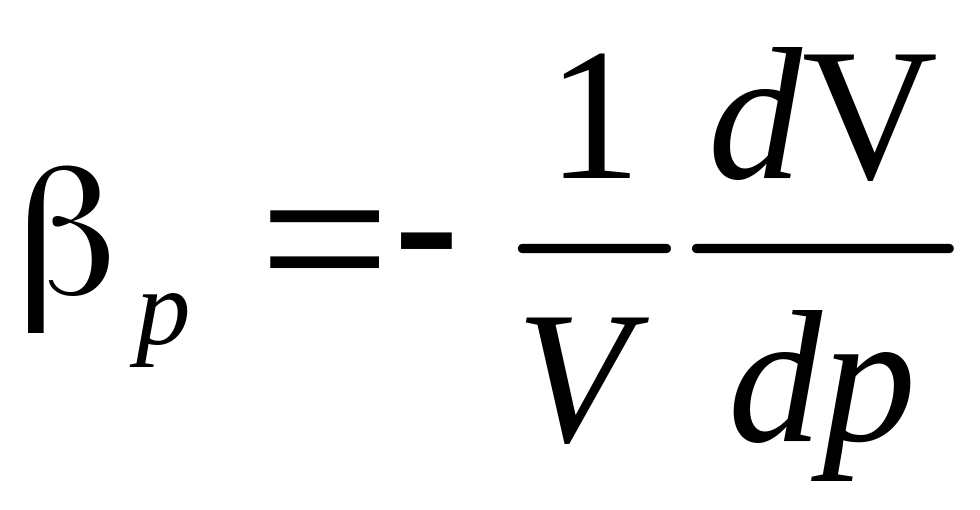
![]() ,
,
отсюда
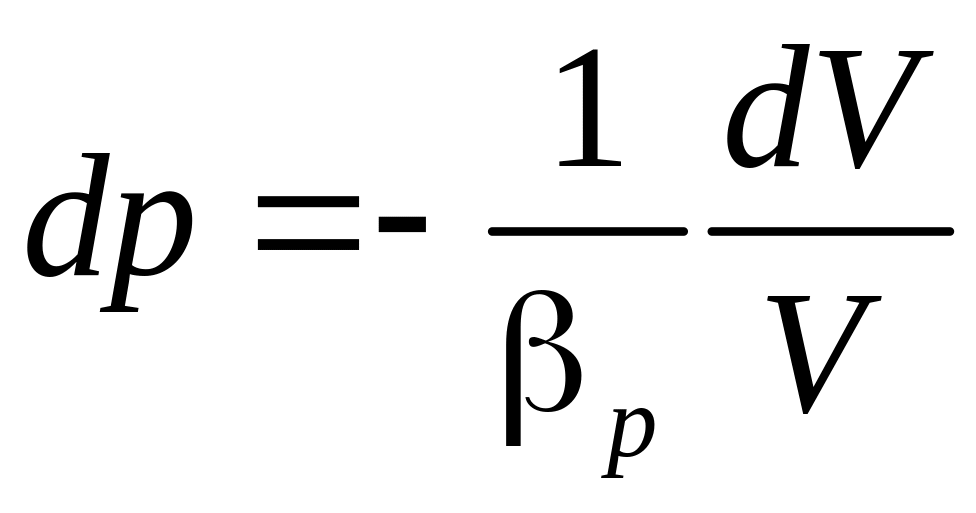 .
.
Знак
«минус» показывает, что при сжатии
величина объема уменьшается. Из выражения
видно, что
![]() есть объемный модуль упругости
есть объемный модуль упругости
![]() данной жидкости или газа, т. е. коэффициент
пропорциональности в законе Гука:
данной жидкости или газа, т. е. коэффициент
пропорциональности в законе Гука:
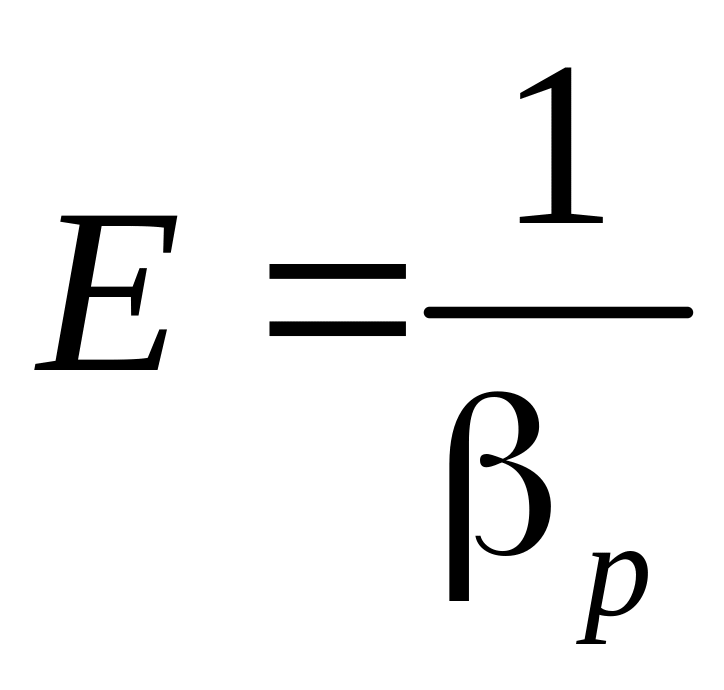
![]() ,
,
тогда
![]() .
.
Коэффициент
сжимаемости
![]() для жидкостей и газов не является
постоянной величиной:
для жидкостей и газов не является
постоянной величиной:
![]() Для газов
Для газов
![]() ,
т. е. модуль упругости
пропорционален давлению p.
,
т. е. модуль упругости
пропорционален давлению p.
Сжимаемость капельных жидкостей гораздо меньше, чем сжимаемость газов. Так при нормальных условиях для воды она в 13 900 раз ниже, чем для воздуха. Поэтому при решении многих задач механики капельные жидкости можно считать несжимаемыми. Так как законы движения для жидкостей и газов во многом одинаковы, то обычно жидкости и газы объединяют под общим названием «жидкости», различая их по сжимаемости: несжимаемые (капельные жидкости) и сжимаемые (газы).
Усилия, которые возникают в жидкостях и газах при сжатии, могут достигать огромных величин. Однако ни жидкость и ни газ не выдерживают сколь-нибудь значительных растягивающих усилий. При растяжении даже малыми усилиями в них возникают пустоты, разрывы. Поэтому будем считать, что при отсутствии разрывов и пустот отсутствуют и растягивающие усилия.
Все
жидкости изменяют свой объем и при
изменении температуры. Изменение объема
характеризует коэффициент
теплового расширения
![]() ,
равный объемной относительной деформации,
приходящейся на единицу изменения
температуры:
,
равный объемной относительной деформации,
приходящейся на единицу изменения
температуры:
![]()
![]() .
.
В
общем случае
![]() .
При малых изменениях температуры можно
считать
.
При малых изменениях температуры можно
считать
![]() и
и
![]() ,
где
,
где
![]() – объем жидкости при температуре
– объем жидкости при температуре
![]() .
.
Наряду с коэффициентом сжимаемости и модулем упругости сжимаемость может быть охарактеризована другими параметрами, с которыми мы ознакомимся ниже.
Вязкость
Все жидкости и газы обладают в той или иной мере вязкостью.
Вязкостью называется способность жидкостей и газов сопротивляться усилиям, касательным к поверхности выделенного объема, т. е. усилиям сдвига.
К жидкостям с малой вязкостью относятся вода, воздух и другие газы. Жидкости с большой вязкостью – это глицерин, минеральное масло и др.
У капельных жидкостей вязкость – это свойство, обратное текучести. Она представляет собой проявление механических связей между частицами (сил сцепления). Под действием этих связей молекулы колеблются относительно своих средних по времени положений. Так как кинетическая энергия колеблющейся молекулы увеличивается с ростом температуры, то усиливается и ее колебательное движение. Вследствие этого механические связи ослабевают, и вязкость жидкости уменьшается. И наоборот, вязкость жидкости будет резко расти с приближением температуры к точке замерзания.
Физическое происхождение вязкости у газов иное. Кинетическая теория учит, что молекулы газов совершают беспорядочное тепловое движение. Молекулы движутся равномерно и прямолинейно до столкновения с другими молекулами. Когда молекулы из какого-либо слоя движущейся жидкости попадают в другой, с иной скоростью движения, то в результате столкновения они обмениваются количествами движения и тем самым изменяют скорость течения газа.
Таким образом, диффузия молекул, сопровождаемая переносом количества движения из одного слоя в другой, является причиной возникновения силы, касательной к слоям (силы трения).
Как известно из кинетической теории газов, с ростом температуры растет скорость теплового движения молекул, увеличивается перенос количества движения и, следовательно, увеличивается вязкость газов.
К асательные
усилия в жидкостях и газах, по сравнению
с нормальными к поверхности сжимающими
усилиями, обычно весьма малы (иногда
меньше почти в тысячу раз). Это позволяет
при решении многих задач, связанных с
определением нормальных усилий (расчет
распределения нагрузок по поверхности
ЛА, аэродинамического момента),
пренебрегать касательными усилиями и
вязкостью, т. е. перейти к идеальной
жидкости.
асательные
усилия в жидкостях и газах, по сравнению
с нормальными к поверхности сжимающими
усилиями, обычно весьма малы (иногда
меньше почти в тысячу раз). Это позволяет
при решении многих задач, связанных с
определением нормальных усилий (расчет
распределения нагрузок по поверхности
ЛА, аэродинамического момента),
пренебрегать касательными усилиями и
вязкостью, т. е. перейти к идеальной
жидкости.
Выделим
на поверхности
![]() рассматриваемого объема жидкости
элементарную площадку
рассматриваемого объема жидкости
элементарную площадку
![]() (рис. 1.1). Пусть на нее действует
поверхностная сила
(рис. 1.1). Пусть на нее действует
поверхностная сила
![]() (сила, действие которой распределено
по поверхности рассматриваемого объема).
Тогда напряжение поверхностных сил в
данной точке равно
(сила, действие которой распределено
по поверхности рассматриваемого объема).
Тогда напряжение поверхностных сил в
данной точке равно
![]() .
.
Составляющие поверхностных напряжений следующие: нормальная – аэродинамическое давление p и касательная – напряжение трения .
Н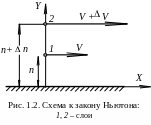 апряжение
трения возникает только тогда, когда
одни частицы жидкости движутся
относительно других или относительно
граничных поверхностей.
апряжение
трения возникает только тогда, когда
одни частицы жидкости движутся
относительно других или относительно
граничных поверхностей.
Рассмотрим
простейший случай, когда все частицы
жидкости движутся параллельно какой-либо
плоскости (рис. 1.2).
Относительная скорость направленного
движения частиц в слое 2
по отношению к слою 1
равна
.
Чем больше разность скоростей, тем
больше силы трения между слоями. То есть
касательное напряжение
![]() ,
или в пределе при
,
или в пределе при
![]() имеем следующее:
имеем следующее:
![]()
![]() , (1.1)
, (1.1)
где
![]() – коэффициент пропорциональности,
который называют коэффициентом
динамической вязкости,
Н
·
с/м2.
– коэффициент пропорциональности,
который называют коэффициентом
динамической вязкости,
Н
·
с/м2.
Выражение (1.1) представляет собой закон Ньютона для касательных напряжений при ламинарном течении.
Из
кинетической теории газов известно,
что
![]() ,
где
,
где
![]() – плотность;
– плотность;
![]() – средняя скорость движения молекул;
– средняя скорость движения молекул;
![]() – длина свободного пробега молекул,
пропорциональная
– длина свободного пробега молекул,
пропорциональная
![]() .
.
С
ростом температуры растет и средняя
скорость движения молекул, вследствие
чего коэффициент динамической вязкости
также будет расти. Величина давления
(в очень широком диапазоне изменения)
практически не влияет на величину
.
Так увеличение давления приводит к
росту плотности газа и одновременному
уменьшению длины свободного пробега
молекул. То есть влияние давления на
величину
взаимно компенсируется, и можно считать,
что
![]() .
.
Влияние температуры на вязкость капельных жидкостей и газов имеет разный характер (табл. 1.1).
Таблица 1.1
