
- •Химическая термодинамика Пример решения вариант № 5
- •Величину ∆g для заданной температуры.
- •Величину Кр для заданной температуры.
- •Пример решения вариант №11
- •Величину ∆g для заданной температуры.
- •Величину Кр для заданной температуры.
- •Химическая кинетика
- •Химическая кинетика
- •Пример решения вариант №29
- •Химическая кинетика
- •Химическая кинетика
- •Пример решения вариант №10
- •Домашнее задание №2 диаграммы плавкости
- •Диаграммы плавкости Пример решения вариант №5
- •Растворы электролитов
- •Растворы электролитов Пример решения вариант №7
- •Растворы неэлектролитов
- •(Задача №2)
- •Равновесие в растворах электролитов (Задача №2) Пример решения вариант № 3
- •Экстракция
- •Экстракция Пример решения вариант №1
- •Решение:
- •Электропроводность
- •Электропроводность Пример решения вариант №12
- •Пример решения вариант №13
- •Пример решения вариант №15
- •Домашнее задание №3 поверхностные явления. Адсорбция (задача №1)
- •Поверхностные явления. Адсорбция (задача №1) Пример решения вариант №3
- •Пример решения вариант №19
- •Поверхностные явления. Адсорбция (задача №2)
- •Поверхностные явления. Адсорбция (задача №2) Пример решения вариант №9
- •Гальванические элементы (задача №1)
- •Гальванические элементы (задача №1) Пример решения №1
- •Пример решения №2
- •Пример решения №3
- •Гальванические элементы (задача №2)
- •Гальванические элементы (задача №2) Пример решения вариант №6
Диаграммы плавкости Пример решения вариант №5
Задание:
1)На основании данных о температуре начала кристаллизации двухкомпонентной системы постройте диаграмму фазового состояния (диаграмму плавкости) А-В (таблица 1).
2)Обозначить точками:
I – жидкий расплав, содержащий а % вещества А, при температуре Т1.
II – расплав, содержащий а % вещества А, находящийся в равновесии с кристаллами химического соединения.
III – систему состоящий из твердого вещества А в равновесии с расплавом, содержащим б % вещества А.
IV – равновесие фаз одинакового состава.
V – равновесие 3 фаз.
3)Определите составы химических соединений.
4)Определить качественные и количественные составы эвтектики.
5)Начертите схематически все типы кривых охлаждения, возможные в данной системе; укажите каким составам на диаграмме эти кривые соответствуют.
6)В каком физическом состоянии находятся системы, содержащие в ,г, д % вещества А при температуре Т1? Что произойдет с этими системами, если их охладить до Т2?
7)Определите число фаз и вариантность системы при эвтектической температуре и содержании А:
а) 95 моль %
б)5 моль %
8)При какой температуре начнет отвердевать расплав, содержащий в% вещества А? При какой температуре он отвердевает полностью? Каков состав первых выпавших кристаллов?
9)При какой температуре начнет плавиться расплав, содержащий г% вещества А? При какой температуре он расславится полностью? Каков состав первых капель раствора?
10)Какой компонент и в каком количестве (кг) выкристаллизуется, если 2 кг расплава, содержащего а моль % вещества А, охладить от Т1 до Т=1000К (таблица 2).
Таблица 1.
Система |
Состав А, моль % |
Т начала кристаллизации |
Состав А, моль % |
Т начала кристаллизации |
А – MgSO4 В – Cs2SO4 |
0 10 20 30 40 45 47 50 |
1292 1241 1193 1116 1013 953 969 999 |
55 60 63 65 70 80 90 100 |
1018 1083 1098 1113 1163 1238 1323 1397 |
Таблица 2.
Т1, К |
а |
б |
в |
г |
д |
Т2, К |
1173 |
55 |
90 |
10 |
40 |
72 |
1023 |
Решение:
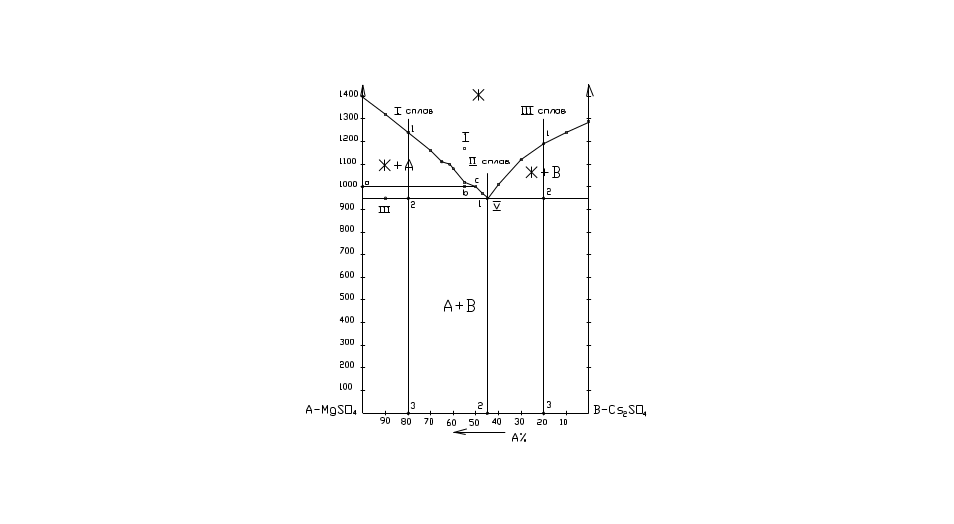
5) а) Кривая охлаждения для состава 80% MgSO4 и 20% Cs2SO4:
 0-1
– охлаждение жидкого сплава MgSO4
и Cs2SO4.
0-1
– охлаждение жидкого сплава MgSO4
и Cs2SO4.
1-2 – выделение кристаллов MgSO4.
2-2’ – совместное выделение кристаллов MgSO4 и Cs2SO4 – кристаллизация эвтектики.
2’-3 – охлаждение закристаллизовавшегося сплава MgSO4 и Cs2SO4.
б) Кривая охлаждения для состава 45% MgSO4 и 55% Cs2SO4:
0-1 – охлаждение жидкого сплава MgSO4 и Cs2SO4.
1-1’ – совместное выделение кристаллов MgSO4 и Cs2SO4 – кристаллизация эвтектики.
1’-2 – охлаждение закристаллизовавшегося сплава MgSO4 и Cs2SO4.
в) Кривая охлаждения для состава 20% MgSO4 и 80% Cs2SO4:
0-1 – охлаждение жидкого сплава MgSO4 и Cs2SO4.
1-2 – выделение кристаллов Cs2SO4.
2-2’ – совместное выделение кристаллов MgSO4 и Cs2SO4 – кристаллизация эвтектики.
2’-3 – охлаждение закристаллизовавшегося сплава MgSO4 и Cs2SO4.
6)Система, содержащая 10% вещества MgSO4 при температуре 1173 К – это смесь жидкого сплава MgSO4 и Cs2SO4 и твёрдых кристаллов Cs2SO4. Если эту систему охладить до 1023 К, то в этой системе будет больше твёрдых кристаллов Cs2SO4 (произойдет выделение кристаллов Cs2SO4).
Система, содержащая 40% вещества MgSO4 при температуре 1173 К – это жидкий расплав MgSO4 и Cs2SO4. Если эту систему охладить до 1023 К, то система просто охладится (Т2 < Т1).
Система, содержащая 72% вещества MgSO4 при температуре 1173 К – это состояние равновесия между жидким расплавом MgSO4 и Cs2SO4 и смесью жидкого расплава MgSO4 и Cs2SO4 и твердых кристаллов MgSO4. Если эту систему охладить до 1023 К, то начнёт происходить выделение кристаллов MgSO4 и система будет представлять собой смесь жидкого расплава MgSO4 и Cs2SO4 и твердых кристаллов MgSO4.
7) а) Число фаз – 3.
С = 2 + 1 – 3 = 0.
б) Число фаз – 3.
С = 2 + 1 – 3 = 0.
8) Расплав, содержащий 10% вещества MgSO4, начнёт отвердевать при Т = 1241 К, а отвердеет полностью при Т = 953 К. Состав первых выпавших кристаллов – чистые кристаллы Cs2SO4.
9) Расплав, содержащий 40% вещества MgSO4, начнёт плавиться при Т = 953 К, а расплавится полностью при Т = 1013 К. Состав первых капель раствора – жидкий расплав MgSO4 и Cs2SO4.
10) Пусть: abc = 100% = 2 кг.
![]()
