
- •Химическая термодинамика Пример решения вариант № 5
- •Величину ∆g для заданной температуры.
- •Величину Кр для заданной температуры.
- •Пример решения вариант №11
- •Величину ∆g для заданной температуры.
- •Величину Кр для заданной температуры.
- •Химическая кинетика
- •Химическая кинетика
- •Пример решения вариант №29
- •Химическая кинетика
- •Химическая кинетика
- •Пример решения вариант №10
- •Домашнее задание №2 диаграммы плавкости
- •Диаграммы плавкости Пример решения вариант №5
- •Растворы электролитов
- •Растворы электролитов Пример решения вариант №7
- •Растворы неэлектролитов
- •(Задача №2)
- •Равновесие в растворах электролитов (Задача №2) Пример решения вариант № 3
- •Экстракция
- •Экстракция Пример решения вариант №1
- •Решение:
- •Электропроводность
- •Электропроводность Пример решения вариант №12
- •Пример решения вариант №13
- •Пример решения вариант №15
- •Домашнее задание №3 поверхностные явления. Адсорбция (задача №1)
- •Поверхностные явления. Адсорбция (задача №1) Пример решения вариант №3
- •Пример решения вариант №19
- •Поверхностные явления. Адсорбция (задача №2)
- •Поверхностные явления. Адсорбция (задача №2) Пример решения вариант №9
- •Гальванические элементы (задача №1)
- •Гальванические элементы (задача №1) Пример решения №1
- •Пример решения №2
- •Пример решения №3
- •Гальванические элементы (задача №2)
- •Гальванические элементы (задача №2) Пример решения вариант №6
ПРИЛОЖЕНИЕ №6
Государственное образовательное учреждение высшего профессионального образования
«Московский государственный технический университет имени Н.Э. Баумана»
(МГТУ им. Н.Э. Баумана)
ПРИМЕРЫ ДОМАШНИХ ЗАДАНИЙ
Физическая химия
Автор: Логинова А.Ю., Герасимова Н.С.
ФН6-КФ кафедра «Химия»
ДОМАШНЕЕ ЗАДАНИЕ №1
ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
Для следующих реакций определить:
Величину ∆G для заданной температуры.
Величину Кр для заданной температуры.
Построить график функциональной зависимости ∆G = f(Т).
Построить график для уравнения lnKp =
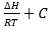 и
определить по нему ∆H
и C.
и
определить по нему ∆H
и C.
1. CO+H2O(Г)=CO2+H2 T=298K, 500K, 700K, 900K;
2. CO+O2+N2=CO2+N2O T=298K, 400K, 500K, 600K;
3. 2CO=CO2+Cалмаз T=298K, 350K, 400K, 450K;
4. 3CO+N2+3H2O=2NH3+3CO2 T=298K, 350K, 400K, 450K;
5. 2CO+N2+2O2=2CO2+2NO T=298K, 350K, 400K, 450K;
6. 2CO+GeO2=Ge+2CO2 T=298K, 400K, 600K, 800K;
7. CO+PtCl2+H2O(г)=CO2+Pt+2HCl T=298K, 350K, 400K, 450K;
8. 2H2+GeO2=2H2O(г)+Ge T=298K, 600K, 800K, 1000K;
9. 2H2+SiO2=2H2O(г)+Si T=298K, 600K, 800K, 1000K;
10. 2H2+SiCl4=Si+4HCl T=298K, 400K, 500K, 600K;
11. CO2+Zn=ZnO+CO T=298K, 500K, 700K, 900K;
12. 3H2O(г)+2Fe=H2+ Fe2O3 T=298K, 350K, 500K, 700K;
13. 2H2O+2C=CH4+CO2 T=298K, 500K, 700K, 900K;
14. 3Fe2O3(т)+H2=2Fe3O4(т)+CO2(г) T=298K, 400K, 500K, 700K;
15. 3Fe2O3(т)+CO(г)= 2Fe3O4(т)+CO2(г) T=298K, 350K, 450K, 550K;
16. Fe2O3(т)+3H2(г)=2Fe(т)+3H2O(г) T=298K, 400K, 500K, 600K;
17. Fe2O3(т)+3CO(г)=2Fe(т)+3CO2(г) T=298K, 350K, 400K, 450K;
18. Fe3O4(т)+4H2(г)=3Fe(т)+4H2O(г) T=298K, 350K, 500K, 700K;
19. Fe3O4(т)+4CO(г)=3Fe(т)+4CO2(г) T=298K, 400K, 600K, 800K;
20. CO2+H2(г)=CO(г)+H2O|(г) T=298K, 600K, 800K, 900K.
Химическая термодинамика Пример решения вариант № 5
Для следующих реакций определить:
Величину ∆g для заданной температуры.
Величину Кр для заданной температуры.
Построить график функциональной зависимости ∆G = f(Т).
Построить график для уравнения lnKp =
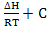 и
определить по нему ∆H
и C.
и
определить по нему ∆H
и C.
Дано:
2CO+N2+2O2=2CO2+2NO
Т1=298К, Т2=350К, Т3=400К, Т4=450К.
Таблица №1.
|
∆Н |
∆S
298,
|
a |
b·103 |
c·10-5 |
N2 |
0 |
191,5 |
27,87 |
4,27 |
- |
O2 |
0 |
205,03 |
31,46 |
3,39 |
-3,77 |
CO |
-110,5 |
197,4 |
28,41 |
4,10 |
-0,46 |
CO2 |
-393,51 |
213,6 |
44,14 |
9,04 |
-8,53 |
NO |
90,37 |
210,62 |
29,58 |
3,85 |
-0,59 |
∆Н298=2∆Hf (CO2)+ 2∆Hf (NO)- 2∆Hf (CO)=-787,82+180,74+221=-385,28 кДж/моль
∆a=∑aпр - ∑аисх = 2·44,14+2·29,58-2·28,41-27,87-2·31,46=-0,17
∆b=6,53·10-3
∆c=-9,78·105
∆cp=-0,17+6,53·10-3T-9,78·105T-2
∆H350=∆H298+![]() =
-385280-0,17(350-298)+
=
-385280-0,17(350-298)+![]() *10-3(3502-2982)+9,87*105(
*10-3(3502-2982)+9,87*105(![]() )=-385280-8,84+110,02-487,59=
-385666 Дж/моль=
-385,67 кДж/моль
)=-385280-8,84+110,02-487,59=
-385666 Дж/моль=
-385,67 кДж/моль
∆H400= -385,9 кДж/моль
∆H450= -386,1 кДж/моль
∆S298= -147,92 Дж/моль·К
∆S350=∆S298+![]() =
-147,92-0,17ln(350/298)+6,53·10-3(350-298)+
=
-147,92-0,17ln(350/298)+6,53·10-3(350-298)+![]() =
-147,92-0,03+0,34-1,51= -149,12 Дж/моль·К
=
-147,92-0,03+0,34-1,51= -149,12 Дж/моль·К
∆S400= -149,75 Дж/моль·К
∆S450= -150,09 Дж/моль·К
∆G298=∆H298-T∆S298= -385280+44080= -342200 Дж/моль = -342,2 кДж/моль
∆G350= -385666+52192= -333474 Дж/моль = -333,5 кДж/моль
∆G400= -385900+59900= -326000 Дж/моль = -326 кДж/моль
∆G450= -386100+67540,5= -318559,5 Дж/моль = -318,6 кДж/моль
![]()
![]()
![]()
![]()
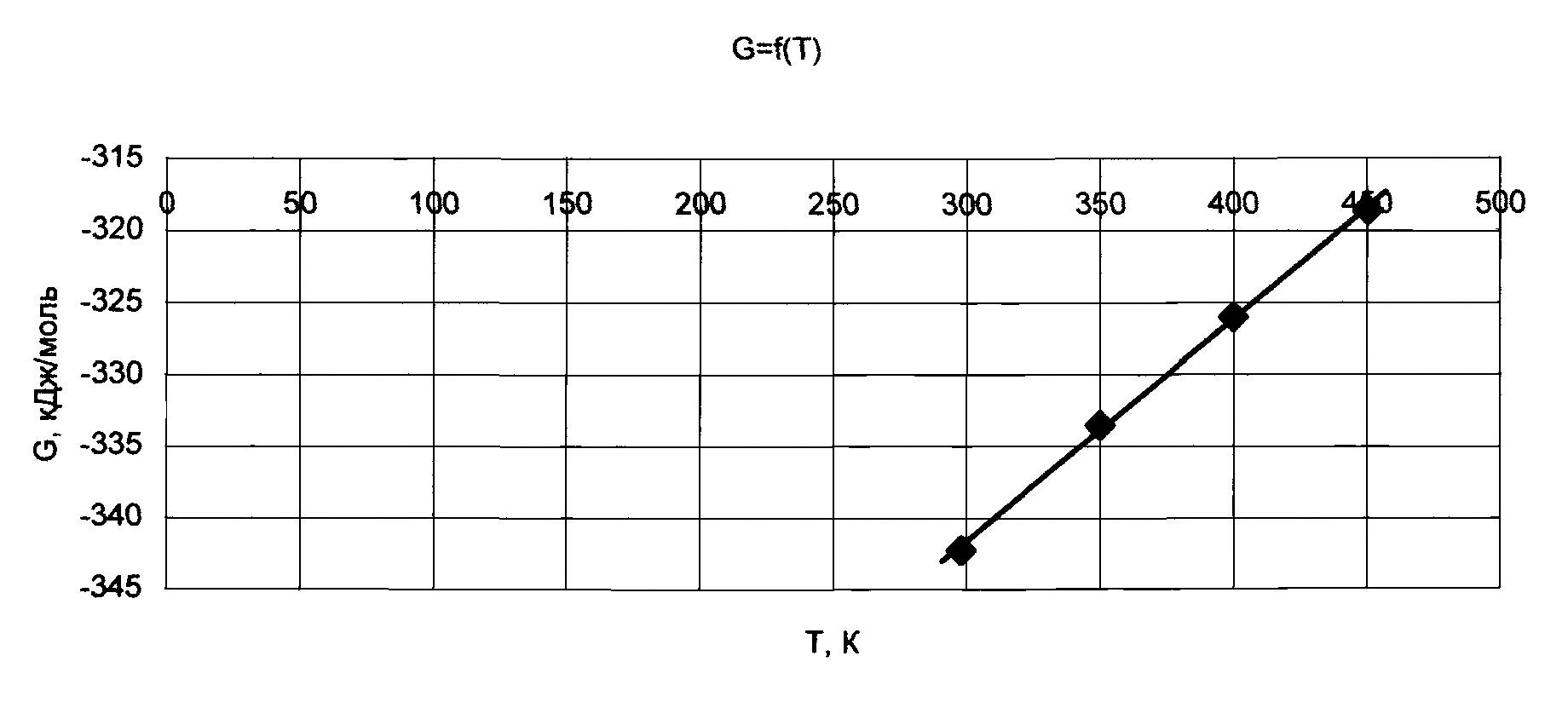
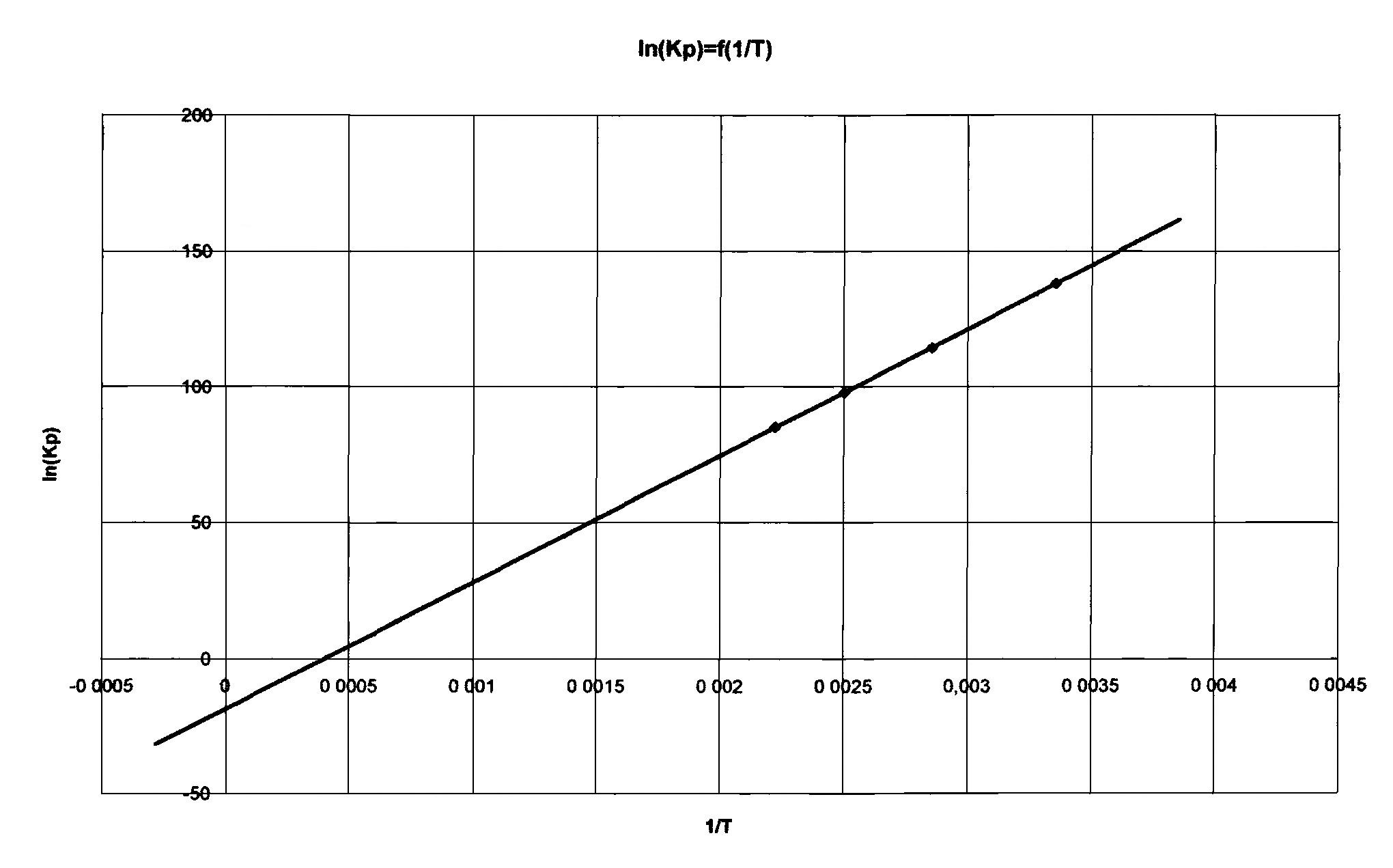
С= -19
![]()
Пример решения вариант №11
Задание.
Для следующих реакций определить:
Величину ∆g для заданной температуры.
Величину Кр для заданной температуры.
Построить график функциональной зависимости ∆G = f(Т).
Построить график для уравнения lnKp = и определить по нему ∆H и C.
Дано:
CO2+Zn=ZnO+CO
T1=298 K; T2=500 K; T3=700 K; T4=900 K.
Таблица №1.
|
∆Н |
∆S
298,
|
a |
b·10-3 |
c’·105 |
CO2 |
-393,51 |
213,6 |
44,14 |
9,04 |
-8,53 |
CO |
-110,5 |
197,4 |
28,41 |
4,10 |
-0,46 |
ZnO |
-394 |
43,5 |
48,99 |
5,10 |
-9,12 |
Zn |
0 |
41,59 |
22,38 |
10,04 |
----- |
Решение:
∆Н 298 х.р. = ∆Н 298(ZnO) + ∆Н 298(CO) - ∆Н 298(CO2) -∆Н 298(Zn)
∆Н 298 х.р. = -394*103 – 110,5*103 + 393,51*103 – 0 = -65,99 .
∆Н
Т
= ∆Н
298
х.р. +
![]() = ∆Н
298
х.р. +
= ∆Н
298
х.р. +
![]() =∆Н
298
х.р. +
=∆Н
298
х.р. +
![]() .
.
![]() 48,99 + 28,41 - 44,14 - 22,38 = 10,88
48,99 + 28,41 - 44,14 - 22,38 = 10,88
![]() (5,1 + 4,1 - 9,04 - 10,04)·10-3
= -9,88·10-3
(5,1 + 4,1 - 9,04 - 10,04)·10-3
= -9,88·10-3
![]() (-9,12 - 0,46 + 8,53)*105
= -1,05*105
(-9,12 - 0,46 + 8,53)*105
= -1,05*105

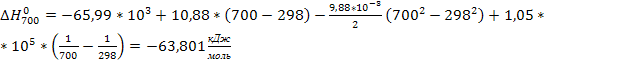
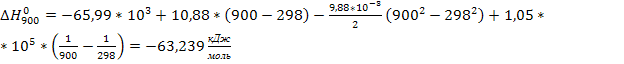
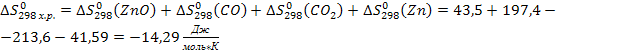
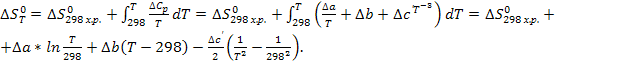

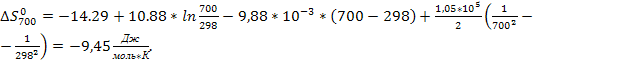
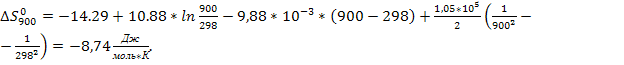
![]()
![]()
![]()
![]()
![]()
2)![]()
![]()
![]()
![]()
![]()
График функциональной зависимости
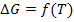

Таблица №2
-
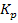
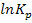

6,7·1010
298
24,93
3,36·10-3
1,54·106
500
14,25
2·10-3
1,86·104
700
9,83
1,43·10-3
1,64·103
900
7,40
1,11·10-3
![]()
![]() .
.
![]()
