- •Белорусский государственный медицинский университет
- •Биологическая химия
- •Содержание
- •Предисловие
- •Структура и функции белков и пептидов. Сложные белки
- •Классификация белков
- •I. Функциональная (по функции, выполняемой в организме)
- •II. По форме молекулы
- •III. По степени сложности молекулы
- •Функции пептидов
- •I. По строению радикала
- •II. По кислотно-основным свойствам
- •III. По полярности
- •Свойства аминокислот
- •Амфотерность
- •С тереоизомерия
- •Спектральные свойства
- •Уровни структурной организации белковых молекул
- •Сложные белки
- •Методы исследования структуры белков и пептидов
- •Этапы исследования первичной структуры белков и пептидов
- •Методы разделения белков Отделение белков от низкомолекулярных примесей
- •Разделение белков по молекулярной массе
- •Выделение индивидуальных белков
- •Анализ гомологичных белков
- •Установление ак-последовательности белка
- •I. Определение n-концевой ак
- •Фибриллярные структурные белки
- •Фибриллярные адгезивные белки
- •Введение в энзимологию. Свойства ферментов
- •Классификация и номенклатура ферментов
- •Строение фермента
- •Единицы измерения активности
- •В лияние температуры
- •В лияние рН
- •Влияние концентрации субстрата
- •Регуляция активности ферментов Принципы регуляции химических процессов в клетке
- •Влияние ингибиторов
- •Ковалентная модификация структуры фермента
- •Примеры использования ингибиторов в медицинской практике
- •Множественные формы ферментов
- •Медицинские аспекты энзимологии
- •Причины гиперферментемий
- •Применение ферментов в медицине
- •2 Стороны метаболизма
- •Общая схема катаболизма пищевых веществ атф и адениловая система клетки
- •Окислительное декарбоксилирование пирувата
- •Последовательность реакций, катализируемых пируватдегидрогеназным комплексом
- •Регуляция пируватдегидрогеназного комплекса
- •Лимоннокислый цикл Кребса, цикл трикарбоновых кислот (цтк)
- •Функции цикла Кребса
- •Регуляция цтк
- •Тканевое дыхание, окислительное фосфорилирование
- •Комплексы дыхательной цепи
- •Пути утилизации кислорода клеткой
- •Переваривание, всасывание, поступление в клетку углеводов. Метаболизм гликогена
- •Переваривание углеводов
- •Всасывание углеводов
- •Транспорт глюкозы в клетки
- •Превращение глюкозы в клетках
- •Метаболизм гликогена
- •Синтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •Гликолиз. Аэробное окисление глюкозы. Глюконеогенез гликолиз
- •Патогенетическая взаимосвязь углеводов пищи и кариеса
- •Аэробное окисление глюкозы
- •Глюконеогенез
- •Пентозофосфатный путь. ГлюкуроновЫй путь пентозофосфатный путь
- •ГлюкуроновЫй путь
- •Переваривание липидов в желудочно-кишечном тракте, система их доставки в клетки к лассификация липидов по химическому строению
- •Переваривание и всасывание
- •Ресинтез липидов в клетках слизистой тонкого кишечника:
- •Депонирование и мобилизация липидов из жировых депо, внутриклеточный обмен жирных кислот
- •Внутриклеточный метаболизм жирных кислот
- •Окисление жирных кислот в пероксисомах
- •Синтез жирных кислот
- •Происхождение ненасыщенных жирных кислот в клетках
- •Синтез и нарушения обмена холестерола, метаболизм кетоновых тел
- •Синтез холестерола de novo
- •Регуляция синтеза холестерола
- •Роль нарушений обмена холестерола в развитии атеросклероза
- •Факторы, связанные с низким или высоким уровнем хс лпвп
- •Образование и утилизация кетоновых тел
- •Система свёртывания крови
- •Свёртывающая (гемокоагуляционная) система крови
- •Антикоагулянтная система
- •Фибринолитическая система
- •Оценка состояния обмена белков, протеолиз азотистый баланс
- •Протеолиз, свойства протеаз. Ограниченный и тотальный протеолиз
- •Переваривание белков в желудочно-кишечном тракте
- •Транспорт аминокислот в клетки
- •Внутриклеточный обмен аминокислот общие пути катаболизма аминокислот Реакции переаминирования
- •Реакции дезаминирования
- •Пути обезвреживания аммиака в организме — синтез глутамина и мочевины.
- •Химия нуклеопротеинов Нуклеиновые кислоты — биополимеры, мономерами которых являются нуклеотиды.
- •Строение рнк
- •Биосинтез нуклеотидов
- •Фосфорибозиламин
- •Инозинмонофосфат
- •ДТмф дУмф умф
- •Образование дезоксирибонуклеотидов
- •Биосинтез днк
- •Биосинтез рнк
- •Структура рнк-полимеразы прокариот
- •R Аминоацил-тРнк
- •Гормоны. Общий механизм действия гормонов
- •Механизм действия гормонов, взаимодействующих
- •Механизм действия гормонов, взаимодействующих с 1-тмс-рецепторами
- •Механизм действия гормонов, взаимодействующих с внутриклеточными (r)
- •Гормоны — производные белков, пептидов и аминокислот гормоны гипоталамуса
- •Гормоны аденогипофиза Это гормоны белково-пептидной природы.
- •Гормоны задней доли гипофиза
- •Гормоны поджелудочной железы
- •2. Окисление и изомеризация прегненолона в прогестерон. Прегненолон является предшественником всех стероидных гормонов.
- •Половые гормоны
- •Биохимия питания. Макро- и микроэлементы
- •Макроэлементы
- •Концентрация электролитов вне и внутри клетки существенно различается: натрий и кальций преобладают во внеклеточном пространстве, калий и магний — внутри клетки. Кальций
- •Кальцитонин
- •Паратирин (паратгормон)
- •Витамин д (кальциферол), антирахитический
- •Микроэлементы Железо
- •Биохимия питания. Витамины и другие незаменимые факторы питания. Синдром недостаточного питания
- •Витамины
- •Биохимия соединительных тканей и органов полости рта (костная, хрящевая ткани; зубы)
- •Неколлагеновые белки костной ткани и их роль в процессах минерализации
- •Химический состав тканей зуба и кости (весовые %)
- •Биохимия ротовой жидкости
- •Функции ротовой жидкости
- •1. Защитная.
- •Белки ротовой жидкости и их роль
- •Ферменты ротовой жидкости и их роль
- •Поверхностные образования на эмали
- •Фтор (f) и его роль в организме
- •Биохимия печени
- •Функции печени
- •Миофибриллярные (сократительные) белки
- •Молекулярный механизм мышечного сокращения
- •Источники энергии мышечного сокращения
- •Механизмы энергообеспечения мышечного сокращения
Пути обезвреживания аммиака в организме — синтез глутамина и мочевины.
1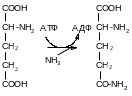 .
Синтез глутамина. Реакция
катализируется глутаминсинтетазой:
.
Синтез глутамина. Реакция
катализируется глутаминсинтетазой:
Распределение и субклеточная локализация. Реакция протекает в цитозоле клеток всех тканей, но особенно выражена в мозге, где аммиак наиболее токсичен, и мышцах, где обмен белков мышц сопровождается образованием значительных количеств аммиака.
Функции глутамина:
a) во всех тканях глутамин является донором азота для синтеза важных молекул, в частности, для пуринового и пиримидинового синтеза;
б) является нетоксичной формой транспорта аммиака из разных тканей к клеткам печени, где он превращается в мочевину;
в) в кишечнике служит источником энергии для энтероцитов;
г) в почках участвует в поддержании кислотно-щелочного равновесия. Гидролиз амидной группы в боковой цепи глутамина глутаминазой позволяет связывать протоны. Это особенно важно в условиях метаболического ацидоза.
2. Синтез мочевины. Печень — единственный орган, клетки которого содержат все ферменты синтеза мочевины и, следовательно, являются главным местом ее синтеза. Участвуют митохондриальные ферменты и ферменты цитозоля.
Суммарная реакция синтеза мочевины:
Аспартат + NH3 + CO2 + 3АТФ
3 H2O + мочевина + фумарат + 2АДФ + АМФ + 2Фн + пирофосфат.
Энергетический баланс. 3 молекулы АТФ расходуется на синтез каждой молекулы мочевины.
1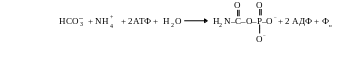 .
Синтез
карбамоилфосфата
(происходит в митохондриях):
.
Синтез
карбамоилфосфата
(происходит в митохондриях):
2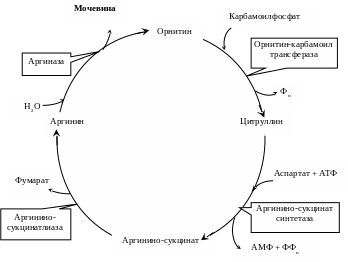 .
Орнитиновый
цикл мочевинообразования:
.
Орнитиновый
цикл мочевинообразования:
Реакции декарбоксилирования
Синтез серотонина:
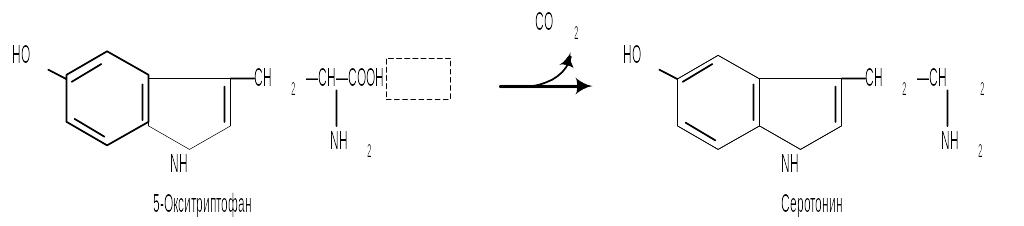
Биологическая роль серотонина:
1. Центральное действие (ЦНС) — повышение аппетита, регуляция памяти, настроения, поведения, функций сердечно-сосудистой и эндокринной систем.
2. Периферическое действие — активирует перистальтику, повышает агрегацию тромбоцитов, проницаемость мелких сосудов, оказывает радиопротекторное действие.
Синтез гистамина:
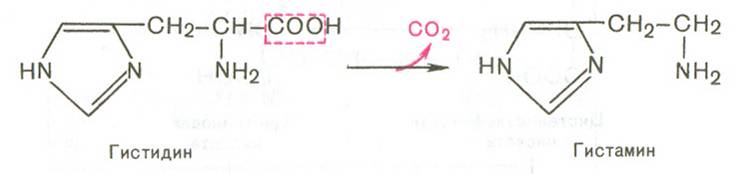
Биологическая роль гистамина: повышает тонус гладкой мускулатуры, расширяет капилляры, снижает АД, повышает секрецию желудка и выделение желчи, участвует в развитии воспаления и развитии боли.
Синтез γ-аминомасляной кислоты (ГАМК):
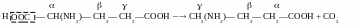
Биологическая роль ГАМК: медиатор торможения.
Синтез дофамина, норадреналина и адреналина:
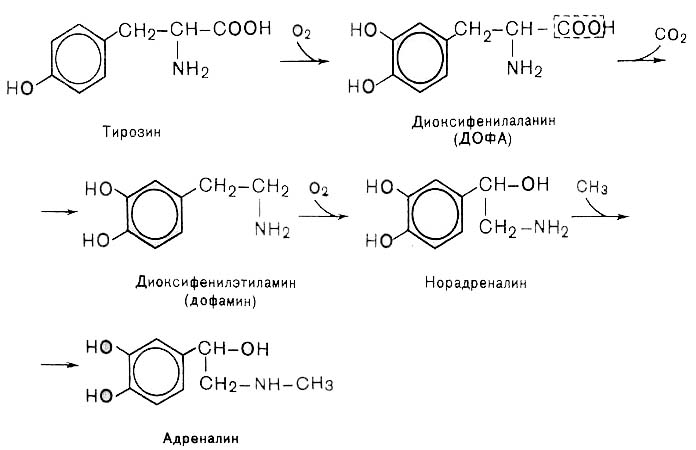
Биологическая роль катехоламинов: увеличивают потребление кислорода клетками, органами и организмом; повышают активность ферментов цикла Кребса, дыхательной цепи; стимулируют синтез АТФ; повышают АД.
Химия нуклеопротеинов Нуклеиновые кислоты — биополимеры, мономерами которых являются нуклеотиды.
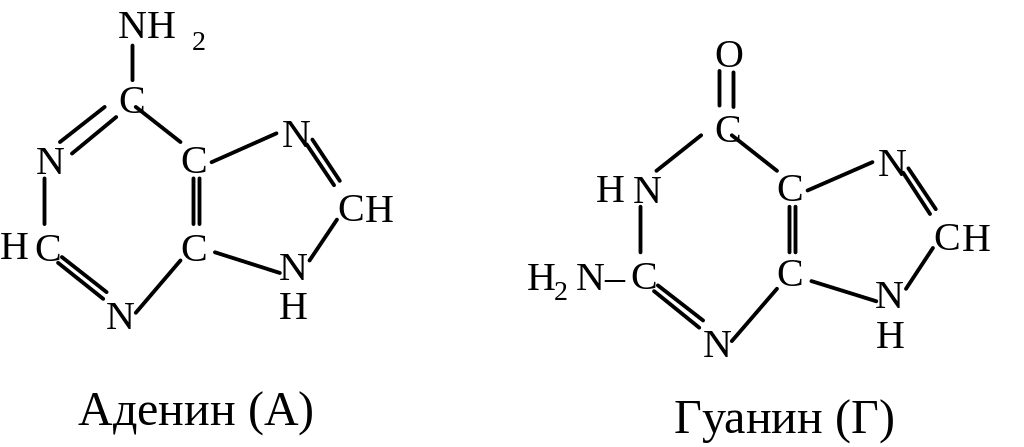
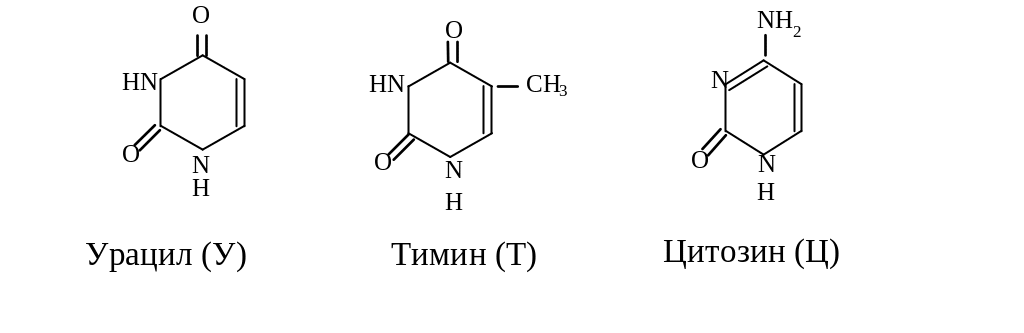
Азотистые основания (АО): Пуриновые |
|
Пиримидиновые |
|
Свойства АО: гидрофобность, копланарность, поглощение УФ при 260 нм.
Нуклеозид = АО + пентоза (рибоза или дезоксирибоза). Пентоза присоединяется N-гликозидной связью.
Свойства нуклеозидов: гидрофильность.
Нумерация атомов: в АО нумеруют 1, 2, 3 и т. д., в пентозе — 1/, 2/, 3/, и т. д.
Нуклеотид = нуклеозид + 1–4 остатка H3PO4.
Свойства нуклеотидов: кислотность, отрицательный заряд.
Номенклатура:
АЗОТИСТОЕ ОСНОВАНИЕ |
НУКЛЕОЗИД (+ рибоза) |
НУКЛЕОТИД (+ фосфат) |
Пурины АДЕНИН
ГУАНИН
ГИПОКСАНТИН |
АДЕНОЗИН*
ГУАНОЗИН
ИНОЗИН |
АДЕНОЗИН монофосфат (АМФ)*; дифосфат (АДФ); трифосфат (АТФ). ГУАНОЗИН монофосфат (ГМФ), …
ИНОЗИН монофосфат (ИМФ), … |
Пиримидины УРАЦИЛ
ЦИТОЗИН
ТИМИН |
УРИДИН
ЦИТИДИН
ТИМИДИН (+дезоксирибоза) |
УРИДИН монофосфат (УМФ), …
ЦИТИДИН монофосфат (ЦМФ), …
ТИМИДИН монофосфат (ТМФ), … |
* — если сахар дезоксирибоза — дезоксиАДЕНОЗИН, дАМФ.
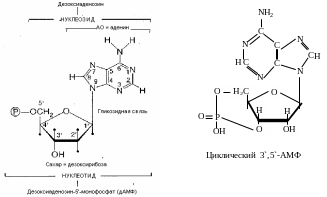
Биологическая роль нуклеотидов:
являются универсальными источниками энергии в клетке (АТФ, ГТФ);
являются активаторами и переносчиками мономеров в клетке (например, УДФ-глюкоза, ЦДФ-холин);
являются аллостерическими регуляторами активности ферментов;
входят в состав коферментов (НАД+, НАДФ+, ФАД, КоА- SH);
циклические мононуклеотиды (цАМФ, цГМФ) являются вторичными посредниками действия гормонов и других сигналов на клетку;
являются мономерами в составе нуклеиновых кислот.
СТРОЕНИЕ ДНК
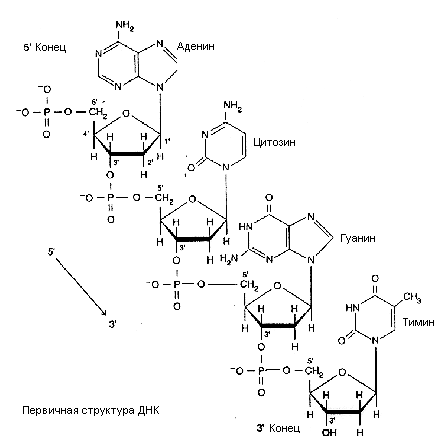 В
ДНК входят 4 типа АО: А, Т, Г, Ц; сахар
дезоксирибоза. Связь между нуклеотидами
образуется с участием 3/-ОН-группы
одного нуклеотида и 5/-остатком
фосфорной кислоты другого
(3/–5/-фосфодиэфирная
связь). В результате молекула полинуклеотида
приобретает направленность — у нее
есть 3/-конец
и 5/-конец.
В
ДНК входят 4 типа АО: А, Т, Г, Ц; сахар
дезоксирибоза. Связь между нуклеотидами
образуется с участием 3/-ОН-группы
одного нуклеотида и 5/-остатком
фосфорной кислоты другого
(3/–5/-фосфодиэфирная
связь). В результате молекула полинуклеотида
приобретает направленность — у нее
есть 3/-конец
и 5/-конец.
Под первичной структурой ДНК понимают последовательность нуклеотидов в одной полинуклеотидной цепи.
В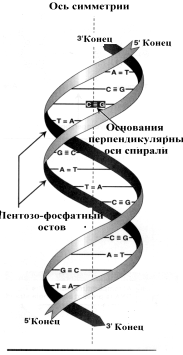 торичная
структура ДНК
(1953 г., Д. Уотсон, Ф. Крик) — двойная
спираль, построенная по принципам
комплементарности (А — Т, Г — Ц) и
антипараллельности (3/-концу
одной цепи соответствует 5/-конец
другой).
торичная
структура ДНК
(1953 г., Д. Уотсон, Ф. Крик) — двойная
спираль, построенная по принципам
комплементарности (А — Т, Г — Ц) и
антипараллельности (3/-концу
одной цепи соответствует 5/-конец
другой).
С илы,
стабилизирующие двойную спираль: 1)
горизонтальные водородные связи между
АО (А = Т, Г ≡ Ц); 2) вертикальные
«стейкинг»-взаимодействия между АО; 3)
гидрофобные взаимодействия (АО обращены
внутрь, к оси спирали, а полярные пентозы
и фосфаты — наружу).
илы,
стабилизирующие двойную спираль: 1)
горизонтальные водородные связи между
АО (А = Т, Г ≡ Ц); 2) вертикальные
«стейкинг»-взаимодействия между АО; 3)
гидрофобные взаимодействия (АО обращены
внутрь, к оси спирали, а полярные пентозы
и фосфаты — наружу).
Силы, дестабилизирующие двойную спираль: электро-статические взаимодействия между отрицательно заряженными фосфатами: а) в пределах одной цепи; б) между цепями.
Поверхность двойной спирали имеет две спиральные бороздки — большую и малую. Белки связываются с ДНК в области большой бороздки, куда выступают АО.
Денатурация (плавление) ДНК — процесс расхождения нитей и формирования одноцепочечных молекул. Происходит при повышении температуры (около 70°С), при репликации и транскрипции (в отдельных участках). При постепенном снижении температуры наблюдается ренатурация.
Третичная структура ДНК — формируется только в связи с белками и служит для компактной упаковки ДНК в ядре. Белки, входящие в состав нуклеопротеинов:
Гистоновые: богаты аргинином и лизином, имеют «+» заряд (основные). Связь с НК — ионная.
5 классов гистонов — Н1, Н2А, Н2В, Н3, Н4.
Негистоновые.
Уровни упаковки генетического материала:
Нуклеосомный. Нуклеосома состоит из октамера гистонов (содержит 8 молекул гистонов — по два каждого класса, кроме Н1), вокруг этого ядра молекула ДНК делает 1,5–2 оборота.
Соленоидный — обеспечивается гистоном Н1.
Петлевой — в образовании петель принимают участие негистоновые белки.
Уровень метафазной хромосомы — высший уровень спирализации хроматина.
Модификации гистонов (фосфорилирование, ацетилирование) приводят к уменьшению их заряда, в результате чего гистоны легче отсоединяются от ДНК, и она становится доступна ферментам репликации и транскрипции.
Ф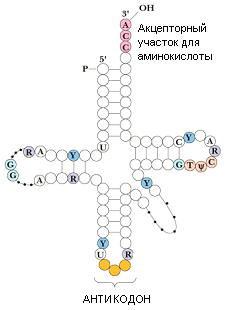 ункции
ДНК: хранение, воспроизводство и передача
по наследству генетического материала,
экспрессия генов.
ункции
ДНК: хранение, воспроизводство и передача
по наследству генетического материала,
экспрессия генов.