
- •«Хімічні пастки для карбенів»
- •Циклопентапіперазиновий карбен. Його внутрішньо- та міжмолекулярне вловлювання.
- •Норборненові карбени, причини їх стабілізації та електрофільні властивості.
- •Дифторкарбен та його іліди з піридином та хіноксаліном. Синтез нових фторвмісних гетероциклічних сполук.
- •Біфенілетилкарбен та його вловлювання метанолом. Електронні спектри інтермедіатів.
- •Цвітер-йон диметоксикарбену та dmad, його реакції з 1,2-дикетосполуками.
- •Карбени 1,2,4-триазолів, їх вловлювання ацетонітрилом та халькогенами
- •Висновок.
- •Список використаної літератури:
Норборненові карбени, причини їх стабілізації та електрофільні властивості.
Досить цікавим типом карбенів є норборненові карбени (foiled carbenes). Класичним прикладом таких карбенів є норборнен-7-ілід:

Вперше цей карбен одержав Мос, після чого 35 років хімія карбонів норборенового типу активно розвивалась. Стабілізація карбенів такого типу забезпечується шляхом перекриванням вільної карбенової р-орбіталі (LUMO) та заповненої р-орбіталі подвійного зв’язку (HOMO). Як результат, утворюється трьохцентровий двохелектронний зв'язок. Це у свою чергу впливає на геометрію карбену. Зокрема, було показано, що карбеновий місток наближається до подвійного зв’язку на 370 у порівнянні з вихідним норборненом. Таким чином, для міжмолекулярних реакцій простір навпроти подвійного зв’язку є більш доступним. Це передбачає стереоспецифічність міжмолекулярних реакцій за участю карбену. Більше того, електронна густина подвійного зв’язку частково передається на карбеновий центр, що підвищує нуклеофільність норборненового карбену. Це у свою чергу звужує ряд реагентів, які можуть використовуватись для вловлювання такого карбену. Проте, є відомості про вловлювання норборненового карбену метанолом після протонування.
Австрійські хіміки вирішили дослідити реакційну здатність трицикло[6.2.1.02,7]ундец-8-ен-11-ілідену (13). У своїй статті3 вчені опублікували реакцію карбену (13), одержаного при термолізі сполуки (12), з діетиламіном:
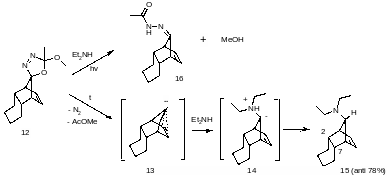
Будову продукту термолізу (15) було доведено на основі NOESY спектрів, а найбільш характеристичним сигналом при цьому була взаємодія H(2), H(7) та СН2 етильної групи. Ці результати підтверджують амбідентну природу карбену (13), який, незважаючи на високу нуклеофільність, все ще здатний реагувати як електрофіл з сильними донорами електронів. В даному випадку діетиламін виступає в якості хімічної пастки для кабену (13).
Дифторкарбен та його іліди з піридином та хіноксаліном. Синтез нових фторвмісних гетероциклічних сполук.
В останні роки досить поширеним стало використання хіміками розрахункових програм, що значно полегшує роботу у лабораторії. Для прикладу, минулого року наші колеги із Росії опублікували статтю, в якій вони описують використання розрахункового методу DFT B3LYP/6-31G у підборі пастки для дифторкарбену4. Відомо, що незаміщений піридин реагує з дифторкарбеном оборотньо. Розрахунки DFT B3LYP/6-31G показали, що введення електроноакцепторних замісників у 4-те положення піридину збільшує константу рівноваги цієї реакції. Таким чином, використання 4-ціано, 4-бензоіл та 4-етоксикарбоніл заміщених піридинів в присутності діметилмалеату чи фумаронітрилу дозволило уловити дифторкарбен, генерований дією ультразвуку на суміш свинцю та дибромодифторометану в присутності броміду тетрабутиламіну. В результаті реакції були одержано 3-фтородигідроіндолізини (14), які вступали в реакцію дегідрування під дією Манган (IV) оксиду з утворенням 3-фтороіндолізинів (15):
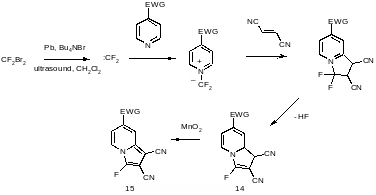
Аналогічно було розраховано і проведено реакцію вловлювання дифторкарбену хіноксаліном (16) у присутності диметилмалеату з утворенням сполуки (17):
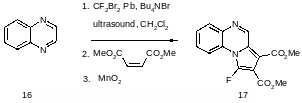
Ця реакція може служити чудовим методом синтезу гетероциклічних сполук типу (15) та (17).
