
- •Теплотехника
- •Введение
- •1. Техническая термодинамика.
- •1.1. Предмет и основные понятия
- •1.2. Параметры состояния
- •1.3. Уравнение состояния и термодинамический процесс
- •1.4 Первый закон термодинамики Теплота и работа
- •Внутренняя энергия
- •Первый закон термодинамики
- •1.5.Теплоемкость газа
- •1.6. Уравнение состояния идеального газа
- •Смесь идеальных газов
- •1.7. Второй закон термодинамики Основные положения второго закона термодинамики
- •1.8. Термодинамические процессы
- •Политропный процесс
- •1.9. Термодинамика потока Первый закон термодинамики для потока
- •Критическое давление и скорость. Сопло Лаваля
- •Дросселирование
- •1.10. Сжатие газов Объемный компрессор
- •17.2. Лопаточный компрессор
- •3.10.Реальные газы. Водяной пар. Влажный воздух Свойства реальных газов
- •Уравнения состояния реального газа
- •Водяной пар
- •Характеристики влажного воздуха
- •1.12. Термодинамические циклы Циклы паротурбинных установок (пту)
- •Циклы двигателей внутреннего сгорания (двс)
- •Циклы газотурбинных установок (гту)
- •2.Основы теории теплообмена
- •2.1. Основные понятия и определения
- •2.2. Теплопроводность
- •2.3. Теплоотдача
- •2.4. Теплообмен при конденсации насыщенных паров
- •2.5. Теплообмен при кипении жидкостей
- •2.6. Лучистый и сложный теплообмен
- •2.5.Теплопередача Теплопередача через плоскую стенку
- •Теплопередача через цилиндрическую стенку
- •2.6. Теплообменные аппараты
- •Расчет теплообменных аппаратов
- •3.Теплоэнергетические установки
- •3.1. Энергетическое топливо. Состав топлива
- •Характеристика топлива
- •Моторные топлива для поршневых двс
- •3.2. Котельные установки Котельный агрегат и его элементы
- •3.3. Вспомогательное оборудование котельной установки
- •3.4. Тепловой баланс котельного агрегата
- •3.5. Топочные устройства
- •3.6. Сжигание топлива
- •Теплотехнические показатели работы топок
- •Физический процесс горения топлива
- •Определение теоретического и действительного расхода воздуха на горение топлива
- •Количество продуктов сгорания топлива
- •Вопросы экологии при использовании теплоты
- •18.1. Токсичные газы продуктов сгорания
- •18.2. Воздействия токсичных газов
- •18.3. Последствия парникового эффекта
- •4. Холодильные установки лекция № 1
- •Термодинамические основы рабочих тел
- •Лекция № 2
- •Способы получения низких температур
- •Плавление
- •Кипение
- •Охлаждение расширением газов
- •Охлаждение дросселированием
- •Охлаждение вихревым эффектом
- •Термоэлектрический эффект
- •Лекция № 3
- •Термодинамические основы холодильных машин
- •Обратный цикл Карно
- •Лекция № 4
- •Обратимые и необратимые процессы
- •Работа компрессора
- •Лекция № 5
- •2. Структура термодинамической диаграммы состояния. Тепловая диаграмма
- •Лекция № 6
- •Лекция № 7
- •1.Циклы и схемы одноступенчатых компрессионных холодильных машин.
- •Паровая холодильная компрессионная машина работающая по регетативному циклу
- •Лекция № 8
- •Хладагенты и хладаносители
- •Свойства хладагентов
- •Теплопроводность
- •Растворимость хладагента в воде
- •Характеристики хладагентов
- •Применение хладагентов
- •Хладоносители
- •Литература
1.8. Термодинамические процессы
Как сказано выше первый закон термодинамическим устанавливает взаимосвязь между количеством теплоты, внутренней энергией и работой. При этом, количество теплоты подводимое к телу или отводимое от тела зависит от характера процесса.
К основным термодинамическим процессам относятся: изохорный, изотермический, изобарный и адиабатный. Обобщающий процесс политропный, в котором теплоемкость неизменна.
Для всех этих процессов устанавливается общий метод исследования, который заключается в следующем:
– выводится уравнение процесса кривой Pv и TS – диаграммах;
– устанавливается зависимость между основными параметрами рабочего тела в начале и конце процесса;
Для всех процессов идеального газа
изменение внутренней энергии:
u = сvм|0t2·t2 - сvм|0t1·t1. или при постоянной
теплоемкости U = m·сv·(t2 - t1); (1.35)
работа:
l = P·dv; (1.36)
теплота, участвующая в процессе:
q = cx·(t2-t1); (1.37)
изменение энтальпии:
h=(h2–h1)=сpм|0t2·t2–сpм|0t1·t1
или при постоянной теплоемкости h=сp·(t2–t1). (1.38)
изменение энтропии:
s=cv·ln(T2/T1)+R·ln(v2/v1)=cpln(T2/T1)-R·ln(p2/p1)=
=cv·ln(T2/T1)+cp·ln(v2/v1). (1.39)
Все процессы рассматриваются как обратимые.
Политропный процесс
Политропным процессом называется процесс, в котором теплоемкость остается постоянной. Все состояния политропы, согласно первому закону термодинамики удовлетворяются условию:
q=cndT=du+pdv и q=cndT=dh-vdp.
После подстановки значений внутренней энергии и энтальпии, получим:
cndT=cvdT+pdv и cndT=cpdT-vdp или cndT-cvdT=pdv и cndT-cpdT=-vdp.
После деления уравнений друг на друга придем к выражению:
(сn-cp)/(сn-сv)=-pdv/(vdp).
Левая часть последнего выражения для конкретного процесса величина постоянная и называется показателем политропы n=(сn-cp)/(сn-сv).Разделим переменные и, после интегрирования, придем к основному уравнению политропного процесса, для которого теплоемкость процесса cn=cv·(n-k)/(n–1)
P·vn =Const, (1.40)
где n – показатель политропы, величина постоянная для данного процесса.
Изобарный, изохорный, изотермический и адиабатный процессы являются частными случаями политропного процесса (Рис.4.5):
при cn=cv имеем n= и v= Const, (изохорный),
при cn=cз имеем n=0 и P = Const, (изобарный),
при cn= имеем n = 1 и T = Const, (изотермический),
при cn=0 имеем n = k и · s= Const, (адиабатный).
Работа политропного процесса определяется по выражениям:
l=R·(T1–T2)/(n–1)=R·T1·[1–(v1/v2)n-1]/(n–1)=R·T2·[1–(P2/P1)(n-1)/n]/(n–1). (1.41)
Теплота процесса:
q=cn(T2–T1), (1.42)
Для изохорного процесса (рис.1.2) cn=cv и n=(сv-cp)/(сv-сv)= ± , а основное уравнение политропы примет вид P1/·v =Const или
v=Const, v2 =v1, P2/P1 = T2/T1. (1.43)
Так как v 2 = v 1, то l = 0 и уравнение 1-го закона термодинамики имеет вид: q = u =сv·(t2 - t1)
Д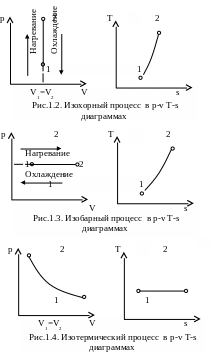 ля
избарного
процесса
(рис.1.3) cn=cp
и n=(сh-cp)/(сh-сv)=0,
а основное уравнение политропы примет
вид P·v0
=Const
или
ля
избарного
процесса
(рис.1.3) cn=cp
и n=(сh-cp)/(сh-сv)=0,
а основное уравнение политропы примет
вид P·v0
=Const
или
P = Const; P2=P1; v2/v1= =T2/T1; l =P(v2-v1); q = u + l = ср·(t2 - t1). (1.44)
Для изотермического процесса (рис.1.4) Теплота процесса: dq=ct dT. При этом dT=0 и dq 0, что возможно лищь в случае ct=. Тогда n=(-cp)/(-сv)=1 и основное уравнение
Т=Const , Т2 = Т1;
P1 v1=v2 P2
Так как Т2 =Т1, то u = 0 и уравнение 1-го закона термодинамическим будет иметь вид:
q=l=RT·ln(v2/v1)=RT·ln(P1/P2),
где R=R/ – газовая постоянная [Дж/(кг·К)].
4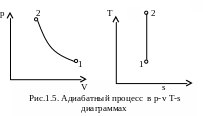 ).
Адиабатный
процесс
(рис.1.5), проходит без теплообмена с
окружающей средой и в процессе тепло
не подводится и не отводится, т.е. q=0. При
этом dT0,
следовательно, сs=0,
n=(0-cp)/(0-сv)=cp/сv=k
и ds=dq/T=0
или s=Const.
Поэтому адиабатный процесс называют
также изэнтропным.
).
Адиабатный
процесс
(рис.1.5), проходит без теплообмена с
окружающей средой и в процессе тепло
не подводится и не отводится, т.е. q=0. При
этом dT0,
следовательно, сs=0,
n=(0-cp)/(0-сv)=cp/сv=k
и ds=dq/T=0
или s=Const.
Поэтому адиабатный процесс называют
также изэнтропным.
Основное уравнение процесса
P·vk = Const, (1.43)
где k=cp/cv – показатель адиабаты.
Уравнение 1-го закона термодинамическим будет иметь вид:
l = -u = -сv·(t2 – t1) = сv·(t1 – t2),
Работа
l=R·(T1–T2)/(k-1)=R·T1[1-(1/2)k-1]/(k-1)=R·T2·[1-(P2/P1)(k-1)/k]/(k-1); (1.44)
С равнительный
анализ процессов, проведенный в
р-v
диаграмме
для одинакового интервала удельных
объемов v1v2
(см. рисунок 1.6), показывает, что максимальная
работа (площадь под линий процесса
наибольшая) совершается в изобарном
процессе. В диаграмме T-s
изобарному процессу также соответствует
наибольшая площадь под линией процесса,
что соответствует наибольшему теплу
процесса (см. рисунок 1.7). Примечателен
политропный процесс с показателем
адиабаты n=1k
(линия 1-5 на рисунке 1.7), в котором тепло
подводится, а температура при этом
снижается. Это явление называют
термодинамическим парадоксом. На
практике с таким процессом встречаемся
при работе с велосипедным насосом. Насос
за счет внешней работы нагревается и
отдает часть тепла в окружающую среду,
т.е тепло от рабочего тела отводится, а
его температура при этом растет.
равнительный
анализ процессов, проведенный в
р-v
диаграмме
для одинакового интервала удельных
объемов v1v2
(см. рисунок 1.6), показывает, что максимальная
работа (площадь под линий процесса
наибольшая) совершается в изобарном
процессе. В диаграмме T-s
изобарному процессу также соответствует
наибольшая площадь под линией процесса,
что соответствует наибольшему теплу
процесса (см. рисунок 1.7). Примечателен
политропный процесс с показателем
адиабаты n=1k
(линия 1-5 на рисунке 1.7), в котором тепло
подводится, а температура при этом
снижается. Это явление называют
термодинамическим парадоксом. На
практике с таким процессом встречаемся
при работе с велосипедным насосом. Насос
за счет внешней работы нагревается и
отдает часть тепла в окружающую среду,
т.е тепло от рабочего тела отводится, а
его температура при этом растет.
