Сфинголипиды - строение, биороль
Сфинголипиды относятся к фосфолипидам и представлены, главным образом, сфингомиэлинами.
Сфингомиэлина много в мембранах, в нервной ткани. Они содержатся в печени, почках и других органах.
На долю сфингомиэлинов приходится от 5 до 25% от общего содержания фосфолипидов.
В состав сфингомиелинов входят:
Ненасыщенный 2-х атомный спирт - сфингозин.
Остаток фосфорной кислоты
Остаток жирной кислоты.
Азотистое основание - холин.
Биороль.
Входит в состав мембран.
Входит в состав нервной ткани.
Участвует в передаче нервного импульса.
Нарушения обмена липидов
К ним относятся:
Ожирение.
Кахексия.
Нарушение переваривания и всасывания.
Жировая инфильтрация печени.
Атеросклероз.
Желчнокаменная болезнь.
Ксантомотоз.
|
|
Глицерол-3-фосфат
АЦИЛ-КоА
Лизофосфатидаты |
|
Дигидроксиацетонфосфат
Фосфатидилинозиты |
|
|
|
АЦИЛ-КоА
Фосфатидаты |
|
ИНОЗИТ
ЦДФ-диглицериды |
|
|
|
Диглицериды |
|
ГЛИЦЕРИН
ДФГ |
|
|
|
|
|
|
|
3 S-АГ
ФХ
ЭТАНОЛАМИН |
ЦДФ-ХОЛИН
3 S-АМ
ХОЛИН |
ЦДФ-ЭТАНОЛАМИН
СЕРИН
ФЭА
|
ЭТАНОЛАМИН
со2 |
ФС |
|
|
|
|
|
|
|
|
|
|
|
|
|
ХОЛЕСТЕРИН - СТРОЕНИЕ, БИОЛОГИЧЕСКАЯ РОЛЬ, СИНТЕЗ.
Строение.
Холестерин является гидроксипроизводным циклопентанпергидрофенантрена. Холестерин - наиболее распространенный стерин животного организма. Он содержится во всех тканях как в свободном состоянии, так и виде эфиров жирных кислот
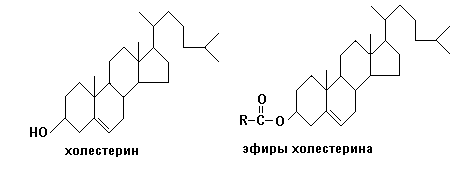
Биологическая роль.
1. Структурная функция.
Практически весь свободный холестерин клетки сосредоточен в ее мембранах. Встраиваясь в липидный биослой, холестерин контролирует подвижность углеводородных хвостов мембранных липидов. Вследствие этого холестерин в известной мере обеспечивает определенное агрегатное состояние, необходимое для нормального функционирования мембраны.
Свободный холестерин служит также важнейшим структурным элементом липопротеинов плазмы крови.
2. Метаболическая функция.
Биологическая роль холестерина заключается также в том, что он является предшественником желчных кислот и стероидных гормонов, а один из интермедиатов синтеза холестерина - 7-дегидрохолестерин - служит предшественником холекальциферола (витамина Д3).
Эфиры холестерина.
В то время, как свободный холестерин служит в клетке важнейшим структурным элементом мембран, эфиры холестерина, локализованные в форме липопротеидных мицелл в цитозоле, являются в основном запасной формой холестерина.
В составе липопротеинов плазмы свободный холестерин служит важнейшим структурным элементом, а эфиры холестерина являются в основном транспортной формой холестерина.
Холестерин крови.
Холестерин является постоянным ингредиентом плазмы крови. Из млекопитающих человек обладает самым высоким уровнем холестерина: 3,64 - 6,76 ммоль/л. Большая часть холестерина плазмы крови (60-80%)находится в этерифицированной форме. Жирнокислотный спектр эфиров холестерина плазмы крови в отличие от такового различных тканей характеризуется высоким содержанием полиненасыщенных жирных кислот.
Холестерин плазмы крови циркулирует в составе липопротеинов. ЛПНП являются транспортной формой холестерина из печени во внепеченочные ткани, а ЛПВП - транспортной формой холестерина из внепеченочных тканей в печень.
Синтез холестерина осуществляется в различных органах и тканях, наиболее интенсивно в печени и тонком кишечнике. Синтез холестерина представляет собой сложный многоступенчатый аэробный необратимый энергозависимый процесс, протекающий в цитоплазме.
В ходе синтеза холестерина различают следующие основные этапы.
Образование мевалоновой кислоты. Исходным продуктом синтеза является ацетил-КоА. В результате конденсации двух ацетил-КоА образуется ацетоацетил-КоА. Последний, взаимодействуя еще с одной молекулой ацетил-КоА превращается в 3-гидрокси-3-метилглутарил-КоА (ГМГ-КоА). Затем ГМГ-КоА восстанавливается до мевалоната под действием ГМГ-КоА-редуктазой. На уровне этой реакции, лимитирующей скорость синтеза холестерина, и осуществляется регуляция холестериногенеза.
Скорость биосинтеза холестерина зависит в норме от количества экзогенного холестерина, т.е. поступающего с пищей. Достаточное для потребностей организма количество экзогенного холестерина (2-3 г) практически полностью подавляет его биосинтез в печени, при отсутствии холестерина в пище интенсивность биосинтеза становится максимальной и может достигать 1 г в сутки. Регуляция и в этом случае основана на принципе ретроингибирования т.е. холестерин является аллостерическим ингибитором ГМГ-КоА-редуктазы.
2. Образование активной изопреновой единицы. Дважды фосфорилируясь с использованием АТФ и декарбоксилируясь, мевалонат превращается в изопентенилпирофосфат - активную изопреновую единицу.
3. Изомеризация изопреновых единиц и последующая их конденсация в сквален.
4. Циклизация сквалена и образование холестерина.
Таким образом, в построении холестерина участвуют 6 активных изопреновых единиц, на образование которых используется 18 ацетил-КоА. Для синтеза холестерина необходимо наличие 17 НАДФН2 и 18 АТФ на одну молекулу холестерина.
Для нормального функционирования синтеза холестерина необходимо наличие следующих витаминов:
В3 (пантотеновая кислота) - составная часть коэнзима А;
РР (никотиновая кислота) - составная часть НАДФ*Н2.
Синтез эфиров холестерина в тканях осуществляется в результате взаимодействия холестерина с ацетил КоА или свободными жирными кислотами.
В кровеносном русле синтез эфиров холестерина осуществляется в ЛПВП при участии плазмоспецифического фермента - фосфатидилхолинхолестеринацилтрансферазы Сущность этой реакции заключается в переносе остатка жирной кислоты с молекулы фосфатидилхолина у С-2 на молекулу холестерина.
Гидролиз эфиров холестерина на составные части осуществляется холестеролэстеразой.
Регуляция синтеза холестерина. ГМГ-КоА-редуктаза ингибируется а печени ХС по принципу обратной связи. Поскольку прямого ингибирования фермента не наблюдается, поскольку ХС или его метаболиты действуют опосредованно т.е. подавляют синтез редуктазы.
Синтез ХС ингибируется также ЛПНП. При введении инсулина или тироидного гормона активность ГМГ-КоА-редуктазы увеличивается, а при введении глюкагона уменьшается
Катаболизм холестерина. В процессе катаболизма холестерина не происходит деградации структуры циклопентанпергидрофенантрена. Возможности животного организма метаболизировать холестерин весьма ограничены. Метаболические превращения холестерина заключаются главным образом во введении атома кислорода в различные положения системы колец и в боковую цепь, ступенчатом отщеплении боковой цепи, а также гидрировании и дегидрировании.
Количественно наиболее важными продуктами трансформации холестерина являются желчные кислоты, синтез которых осуществляется в печени. Образующиеся в печени желчные соли вместе с определенным количеством холестерина (исключительно в свободном состоянии) выделяются в составе желчи в просвет кишечника. Снижение растворимости холестерина в мицеллах желчных солей желчи, обусловленное изменением соотношения различных желчных кислот и холестерина, особенно в сочетании с воспалительным процессом в желчном пузыре создает предпосылки для выпадения холестерина в осадок и образования желчных камней. Большая часть холестерина желчи подвергается в кишечнике реабсорбции и может быть вновь использована организмом. Энтерогепатическая циркуляция холестерина протекает менее эффективно и с меньшей скоростью, чем круговорот желчных кислот.
Не всосавшийся холестерин, а также холестерин десквамированных клеток кишечника метаболизируется микрофлорой толстого кишечника. Продукты микробной трансформации экскретируются с фекалиями.
Необходимо подчеркнуть, что нарушениям метаболизма холестерина принадлежит важнейшая роль в патогенезе атеросклероза, ксантоматоза и желчно-каменной болезни.




 Глицерин
Глицерин