
Лекция 10. Химия воды.
Вода
самое распространенное в природе
химическое соединение. Она покрывает
почти
 площади земной поверхности.
площади земной поверхности.
Вода играет исключительно важную роль в природе и технике. Жизнедеятельность человека, животных, растений связана с процессами, которые происходят в водных средах. Организм взрослого человека на 65% состоит из воды. Вода является регулятором температуры на Земле.
Вода участвует во многих технологических процессах в различных отраслях народного хозяйства. Она применяется как реагент, растворитель, хладагент, теплоноситель, рабочее тело в паровых машинах, в гидрометаллургии, в производстве продуктов питания, лекарств.
10.1 Свойства воды
Фазовая диаграмма воды. Равновесие между различными фазами чистого вещества удобно представлять в виде фазовой диаграммы в координатах р - Т. Отдельные участки фазовой диаграммы соответствуют условиям термодинамической устойчивости какой-либо одной фазы, эти участки разграничиваются кривыми, которые соответствуют областям равновесия между двумя фазами. Каждая кривая - плавления, кипения, сублимации - дает пары значений р и Т, при которых в равновесии находятся: твердое - жидкость, жидкость - пар, твердое - пар. . Совокупность условий одновременного сосуществования трех фаз определяется точкой, где сходятся три кривые, и которая называется тройной точкой (см. рис.19).

Особенностью воды является понижение температуры плавления льда с ростом давления. Вследствие этого, кривая равновесия - твердая фаза - жидкая фаза - у воды, поднимаясь вверх, отклоняется влево (кривая ОВ). Тройная точка воды, в которой ее пары, жидкая и твердая фазы могут сосуществовать в равновесии, характеризуется температурой 0,0098 °С и давлением 0,0060 атм. Поскольку нормальное атмосферное давление превышает указанную величину, мы привыкли видеть, что лед плавится. Пересечение горизонтальной прямой, соответствующей давлению р = 1 атм., с кривой равновесия твердая фаза - жидкая фаза, дает Т плавления льда (0°С), а пересечение этой горизонтали с кривой равновесия жидкость - пар дает температуру кипения воды (100°С). Различие между жидкой и газообразной водой исчезают только при давлениях, выше критических (выше 218 атм.).
Физические свойства воды. В природе распространена вода, соответствующая формуле Н20; в результате длительного электролиза обычной воды можно получить «тяжелую» воду D20, образованную стабильным изотопом водорода - дейтерием; существует радиоактивный изотоп водорода тритий, образующий Т20.
При давлении 101кПа температура кипения воды 100°С, плавления 0°С; она имеет максимальную плотность при 4°С; ее теплоемкость равна 4,17 дж/г-К, диэлектрическая проницаемость 78,5.
Свойства воды существенно отличаются от свойств водородных соединений ее аналогов (H2S, H2Se, H2Te). Вода является жидкостью, остальные водородные соединения - газы. Основные физико-химические свойства также отличаются.
Необычные свойства воды обусловлены как строением ее молекул, так и образованием водородных связей. Атом кислорода в молекуле Н20 находится в состоянии sp3 - гибридизации, угол между связями составляет 105°, близок к тетраэдрическому. При этом две пары электронов образуют связи О-Н, а две другие пары электронов кислорода остаются неподеленными. Общая электронная плотность смещена к кислороду и молекула воды полярна. Вследствие полярности ее молекул, вода является хорошим растворителем.
Наличие неподеленных пар электронов у кислорода и смещение обобществленных электронов к атому кислорода обусловливают образование водородных связей между Н и О соседних молекул
О-Н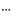 О-Н
О-Н
О-Н
О-Н
| | |
Н Н Н
Возникновение водородных связей между молекулами воды приводит к ассоциации молекул в жидком и твердом состояниях. Этим объясняются аномальные свойства воды в частности высокие температуры кипения, плавления, высокая диэлектрическая проницаемость, а также особая структура льда.
Молекулы воды во льду удерживаются на определенных расстояниях друг от друга водородными связями, обуславливающими каркасную структуру льда, этим и объясняется низкая плотность льда. При таянии льда водородные связи частично разрушаются, расстояние между молекулами воды уменьшается, поэтому плотность воды растет.
При нагревании воды, с одной стороны, увеличивается ее объем, а с другой разрушаются водородные связи, что приводит к уменьшению объема воды. Вследствие этих причин вода имеет минимальный молярный объем и максимальную плотность при температуре 4°С. При увеличении температуры ассоциаты разрушаются и водяной пар состоит из свободных молекул Н20.
Химические свойства. С химической точки зрения вода является термодинамически устойчивым соединением. Стандартная энергия Гиббса образования жидкой воды при температуре 298К равна -237,5 кДж/-моль, водяного пара -228,8 кДж/моль. Диссоциация водяного пара на водород и кислород происходит при температурах выше 1500°С.
В тоже время вода химически активное вещество. Она реагирует с металлами с выделением водорода
2К + 2Н20 = 2КОН + Н2
Взаимодействует с оксидами многих металлов и неметаллов с образованием соответственно оснований и кислот
N02 + Н20 = HN03
Вступает в окислительно-восстановительные реакции, как окислитель, так и восстановитель
Сl2 + Н20 = НСl + НСlO
Под воздействием молекул воды протекают реакции гидролиза
MgC03 + Н20 = Mg(OH)2 + С02
