- •Основы кристаллографии и дефекты кристаллического строения
- •Лекция 1. Основные понятия о кристаллах План лекции
- •1.1. Закон постоянства гранных углов
- •Контрольные вопросы
- •Лекция 2. Структура кристаллов и пространственная
- •План лекции
- •2.1. Элементарная ячейка, её выбор, метрика
- •2.2. Кристаллическая структура
- •2.3. Кристаллографические символы узлов, плоскостей и направлений в кристаллах кубической сингонии
- •2.4. Символы узлов
- •2.5. Символы рядов (ребер, направлений)
- •2.6. Символы плоскостей (граней)
- •Контрольные вопросы
- •3.2. Определение символа атомной плоскости по координатам трёх узлов пространственной решётки
- •3.4. Кристаллографическая символика в гексагональной сингонии
- •Контрольные вопросы
- •Лекция 4. Элементы симметрии конечных фигур План лекции
- •4.1. Понятие о симметрии
- •4.2. Элементы симметрии кристаллических многогранников
- •Обозначение элементов симметрии
- •4.3. Взаимодействие симметрических операций (элементов симметрии)
- •4.4. Осевая теорема Эйлера
- •4.5. Теоремы сложения элементов симметрии
- •4.6. Точечные группы симметрии
- •Контрольные вопросы
- •5.2. Правила кристаллографической установки кристаллов для различных сингоний.
- •5.3. Кристаллографические проекции
- •5.4. Сферическая проекция
- •5.5. Стереографическая проекция
- •5.6. Гномостереографическая проекция
- •Контрольные вопросы
- •План лекции
- •6.1. Классы симметрии
- •6.2. Виды симметрии кристаллов, обладающих единичных направлением
- •6.3. Элементы симметрии бесконечных фигур
- •6.4. Винтовые оси симметрии
- •6.5. Плоскость скользящего отражения
- •6.6 Решетки Бравэ
- •6.7. Условия выбора ячеек Бравэ
- •6.8 Характеристика решеток Бравэ
- •Тип ячейки Бравэ.
- •6.9. Трансляционная группа, базис ячейки
- •6.10. Пример Выбора элементарной ячейки Бравэ
- •Контрольные вопросы
- •Лекция 7. Задачи, решаемые кристаллохимией План лекции
- •7.1 Координационное число, координационный полиэдр, число формульных единиц
- •7. 2. Плотнейшие шаровые упаковки в кристаллах
- •7.3. Основные типы структур
- •7.4. Основные категории кристаллохимии
- •Контрольные вопросы
- •Лекция 8. Точечные дефекты План лекции
- •8.1. Понятие об идеальном и реальном кристалле
- •8.2. Классификация дефектов кристаллической решетки
- •8.3. Точечные дефекты
- •8.4. Искажение решетки вокруг точечных дефектов
- •8.5. Термодинамика точечных дефектов
- •8.6. Миграция точечных дефектов
- •8.6.1.Миграция вакансий
- •8.6.2. Миграция межузельных атомов
- •8.6.3.Миграция примесных атомов
- •Контрольные вопросы
- •Лекция 9. Основные типы дислокаций и их движение План лекции
- •9.2. Скольжение краевой дислокации
- •9.3.Переползание краевой дислокации
- •9.6. Смешанные дислокации и их движение
- •Контрольные вопросы
- •Лекция 10. Количественные характеристики дислокаций План лекции
- •10.2 Вектор Бюргерса
- •10.3. Плотность дислокаций
- •Контрольные вопросы
- •Лекция 11. Упругие свойства дислокаций План лекции
- •11.1. Энергия дислокации
- •11.2. Силы, действующие на дислокацию
- •11.3. Упругое взаимодействие параллельных краевых дислокаций
- •11.4. Упругое взаимодействие параллельных винтовых дислокации
- •Контрольные вопросы
- •Лекция 13. Пересечение дислокаций План лекции
- •13.1. Пересечение краевых дислокаций
- •13.2. Пересечение краевой и винтовой дислокаций
- •13.3. Пересечение винтовых дислокаций
- •13.4. Движение дислокации с порогами
- •13.5. Пересечение растянутых дислокаций
- •Контрольные вопросы
- •14.1.2 Атмосферы Снука
- •14.1.3. Атмосферы Сузуки
- •1.4.2. Взаимодействие дислокаций с вакансиями и межузельными атомами
- •Контрольные вопросы
- •Лекция 15. Образование дислокаций План лекции
- •15.1. Происхождение дислокаций
- •15.2. Размножение дислокаций при пластической деформации Источник Франка — Рида
- •Контрольные вопросы
- •Лекция 16. Границы зерен и субзерен План лекции
- •16.1.Границы кручения и наклона
- •16.2. Малоугловые границы
- •16.3. Высокоугловые границы
- •16.4. Специальные и произвольные границы
- •16.5. Зернограничные дислокации
- •План лекции
- •17.2. Торможение дислокаций при их взаимодействии с другими дислокациями и границами зерен
- •17.3. Торможение дислокаций дисперсными частицами
- •17.4. Выгибание дислокаций между дисперсными частицами
- •17.5. Локальное поперечное скольжение
- •17.6. Перерезание дислокациями дисперсных частиц
- •17.7.2. Торможение дислокаций в твердых растворах
7.3. Основные типы структур
Структура кристалла — это конкретное расположение частиц в пространстве. Описывая структуру, надо указать вид и размер частиц и расстояния между ними. Но так как многие структуры сходны, можно иногда указать лишь относительное расположение частиц (атомов или атомных групп) в кристалле, а не абсолютные расстояния между ними. Так определяется структурный тип. Структуры кристаллов, принадлежащих к одному структурному типу, одинаковы с точностью до подобия. Чтобы описать конкретную структуру, надо указать структурный тип и параметры структуры. Рассмотрим некоторые основные типы структур.
В Международном структурном справочнике принята классификация по группам структур, которая в дальнейшем указывается в скобках при названии типа:
А — элементы;
В — соединения типа АВ (например, NаС1, СsСl)
С—соединения типа АВ2 (СаF2, ТiO2);
D— соединения типа АmВn (Аl2 Oз);
Е — соединения, образованные больше чем двумя сортами атомов без радикалов или комплексные ионов (например, СuFeS);
Р — структуры соединений с двух- или трeхатомными ионами (KCNS,NaHF2);
О — соединения с четырехатомными ионами (СаСОз, NaClO3);
Н—соединения с пятиатомными ионами (CaSO4*2H2O,CaWO4);
L — сплавы;
S — силикаты.
Разновидности типов внутри групп различаются номерами.
Кристаллическая структура меди (тип А).
В структурном типе меди кристаллизуются очень многие металлы: золото, серебро, никель, алюминий, кальций, торий, свинец, α-кобальт и др. Все эти металлы сравнительно мягкие, пластичные, легко обрабатываются. Многие из них образуют непрерывные ряды твердых растворов, например Аg-Аu, Сu-Аu. Структурой типа меди обладают также интерметаллические соединения: АuSb, Au2Bi, Аu2РЬ, Сu2 Мg, и др.
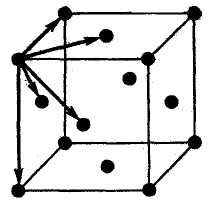
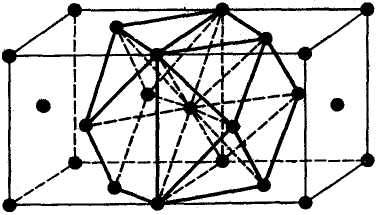
Элементарная ячейка меди—кубическая, гранeцентрированная (ГЦК) (рис. 7.11, а). Атомы располагаются в вершинах и центрах граней F-ячейки. На элементарную ячейку приходится 4 атома. Каждый атом окружен 12 ближайшими атомами, к. ч. = 12. Координационный многогранник — кубооктаэдр (рис. 7.11,б).
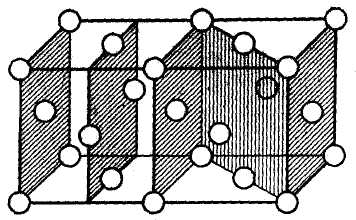
Плоскости зеркального отражения т проходят параллельно грани элементарной ячейки и диагоналям граней (рис. 7.12). Пространственная группа FтЗт.
В структуре имеется одна правильная система точек с кратностью 4. Координаты всех атомов в ячейке, т. е. базис: [[000]], [[1/2, 1/2, 1/2]], [[1/2, 0, 1/2]], [{0, 1/2, 1/2]].
|
|
а |
б |
|
|
в |
|
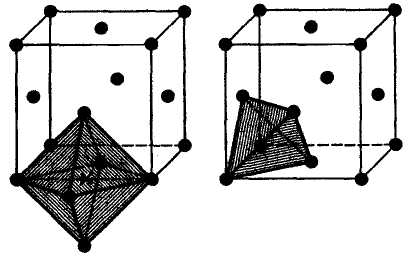
Рис. 7.11 Структура меди: а — элементарная ячейка с выделенными злементарными трансляциями; б —две элементарные ячейки с выделенным координационным кубооктаэдром; в — положение октаэдричетких и тетраэдрическнх пустот |
|
Плотнейшие слои {111} перпендикулярны осям 3, т. е. направлениям <111>; каждый атом в слое окружен шестью атомами. Эти слои сочетаются между собой тоже плотнейшим образом: атом одного слоя ложится в лунку между тремя атомами предыдущего слоя. Плотнейшая упаковка—кубическая, трехслойная АВСАВС... . Все пустоты между шарами не заполнены (рис. 7.11,в). Центры октаэдрических пустот находятся на серединах ребер и в центре кубической элементарной ячейки, а центры тетраэдрических пустот—в серединах каждого из восьми октантов, на которые мысленно можно разделить кубическую ячейку.
Кристаллическая структура магния (тип А3)
В структурном типе магния кристаллизуются гексагональные металлы: кадмий, бериллий, таллий, титан, никель, хром и др.
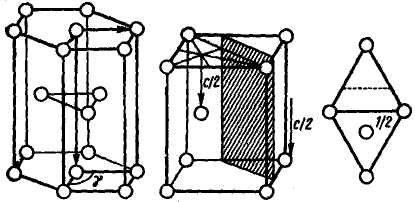
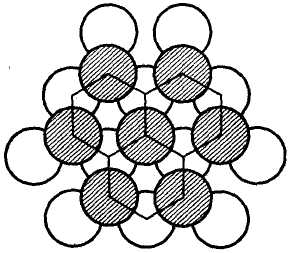
Элементарная ячейка магния—гексагональная примитивная (рис 7.13). На рис. 7.14 представлена структура магния в проекции на плоскость (0001) (атомы верхнего слоя заштрихованы) Центры атомов располагаются по вершинам правильных шестиугольников: в трех вершинах, через одну, —атомы верхнего слоя, в трех других вершинах — атомы нижнего слоя.
|
Рис. 7.12. Две элементарные структуры меди |
Элементарная ячейка построена на трех трансляциях, две из которых лежат в плотноупакованном слое атомов и составляют между собой угол γ=120°, третья – перпендикулярна этому слою.
Элементарную ячейку можно разделить плоскостью на две тригональные призмы. В центре одной из призм расположен атом, другая «не заселена», «заселенные» и пустые призмы чередуются между собой. На элементарную ячейку приходится два атома магния.
Каждый атом магния окружен двенадцатью ближайшими атомами: шестью в том же слое, тремя в соседнем слое сверху и тремя в соседнем слое снизу, т. е. к. ч. =12, что служи; признаком плотнейшей упаковки. Координационный многогранник — гексагональный кубооктаэдр. Плотные слои— плоскости базиса (0001)— перпендикулярны оси 6з. В этой плоскости имеется шесть плотно упакованных направлений <1120> Упаковка гексагональная, двухслойная ...АВАВАВАВ... . Все пустоты не заняты.
|
||
а |
б |
в |
Рис 7.13. Структура магния: а— гексагональная призма из трех элементарных ячеек; б — элементарная ячейка с заштрихованной плоскостью скользящего отражения типа с, в — проекция элементарной ячейки на плоскость базиса (0001) |
||
Кристаллы металлов с плотно упакованной гексагональной структурой легче всего деформируются по плоскостям (0001) и направлениям <1120>, соответствующим наиболее плотной упаковке атомов. Атомы магния образуют одну правильную систему точек с кратностью 2. Атомы, расположенные в вершинах ячейки, связаны друг с другом трансляциями, а с атомом внутри ячейки— либо осью 6з, либо плоскостью с. Координаты атомов базиса ячейки: [[000]], [[1/3, 2/3, 1/4]], [[2/3, 1/3, 3/4]].
|
Рис.7.14. Структура магния в проекции на плоскость базиса (0001) . |
В идеальных плотноупакованных гексагональных металлах отношение высоты элементарной ячейки с к расстоянию а между соседними атомами в базисной плоскости, т; е. с/а, равно 1,633. хотя сами параметры с и а для разных веществ различны.
В тех гексагональных металлах, где с/а== 1,633, ближайшие атомы подразделяются на две координационные сферы: 6+6. Шесть атомов расположены в горизонтальном слое на расстоянии а друг от друга, а по три атома — сверху и снизу на расстоянии:
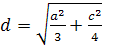 .
.